Kas yra Tracleer?
Tracleer yra vaistas, kurio sudėtyje yra veikliosios medžiagos bosentano. Tiekiamos oranžinės ir baltos plėvele dengtos tabletės (apvalios: 62,5 mg; ovalios: 125 mg) ir šviesiai geltonos dobilo formos disperguojamosios tabletės (32 mg).
Kam vartojamas Tracleer?
Tracleer vartojamas pacientams, sergantiems III klasės plaučių arterine hipertenzija (PAH), siekiant pagerinti fizinį krūvį (gebėjimą sportuoti) ir simptomus. PAH yra patologinė būklė, kai padidėja slėgis plaučių arterijose. „Klasė“ atspindi ligos sunkumą: „III klasė“ apima stiprų fizinio aktyvumo apribojimą. PAH gali būti:
- pirminis (be nustatytos ar žinomos priežasties);
- sukelia sklerodermija (dar vadinama sistemine skleroze, liga, kuriai būdingas nenormalus jungiamojo audinio augimas, palaikantis odą ir kitus organus);
- sukeltas įgimto širdies nepakankamumo (nuo gimimo) su šuntas (nenormalūs ryšiai), kurie sukelia nenormalų kraujo tekėjimą tarp širdies ir plaučių.
Kai kurie pagerėjimai buvo pastebėti pacientams, sergantiems II klasės PAH. „II klasė“ apima nedidelį fizinio aktyvumo apribojimą.
Tracleer taip pat galima vartoti suaugusiesiems, sergantiems sistemine skleroze, kuriems dėl ligos sukeltos prastos kraujotakos išsivystė „skaitmeninės opos“ (rankų ir kojų pirštų uždegimas). „Tracleer“ tikslas yra sumažinti naujų skaitmeninių opų skaičių.
Atsižvelgiant į ribotą pacientų, sergančių PAH ir sistemine skleroze, skaičių, šios ligos laikomos retomis, o 2001 m. Vasario 14 d. Ir 2003 m. Kovo 17 d.
Vaisto galima įsigyti tik pateikus receptą.
Kaip vartoti Tracleer?
Gydymą Tracleer turi pradėti ir stebėti gydytojas, turintis PAH ar sisteminės sklerozės gydymo patirties.
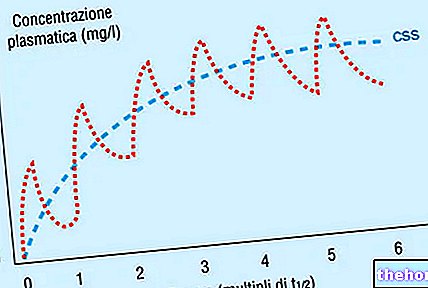
Tracleer skiriamas ryte ir vakare, tuščiu skrandžiu arba pilnu skrandžiu. Suaugusiesiems gydymą reikia pradėti nuo 62,5 mg dozės du kartus per parą keturias savaites, o po to padidinti iki įprastos 125 mg dozės du kartus per parą. Vaikams, sergantiems PAH, dozė priklauso nuo kūno svorio ir paprastai prasideda nuo 2 mg kilogramui du kartus per parą.
Plėvele dengtas tabletes pacientai turi nuryti, užgerdami vandeniu. Disperguojamosios tabletės skirtos tik tiems pacientams, kurie negali išgerti plėvele dengtų tablečių. Prieš vartojimą jie turi būti ištirpinti šaukštelyje šiek tiek „d“ vandens. Disperguojamosios tabletės turi plyšius, leidžiančius jas lengvai padalyti į keturias dalis, kurių kiekvienoje yra 8 mg bozentano. Daugiau informacijos rasite pakuotės lapelyje.
Gydytojas turėtų įvertinti paciento atsaką į Tracleer ir įvertinti tolesnio gydymo poreikį po aštuonių savaičių pacientams, sergantiems PAH, kurie nepranešė apie pagerėjimą, taip pat reguliariai pacientams, sergantiems sistemine skleroze ir besitęsiančiomis skaitmeninėmis opomis.
Pacientams, gydomiems Tracleer, turi būti pateiktas specialus memorandumas, kuriame apibendrinta pagrindinė informacija apie vaisto saugumą.
Kaip veikia Tracleer?
Veiklioji Tracleer medžiaga bosentanas slopina natūraliai atsirandantį hormoną, vadinamą endotelinu-1 (ET-1), dėl kurio susiaurėja kraujagyslės. Todėl „Tracleer“ sukelia „kraujagyslių išsiplėtimą“.
PAH yra sekinanti liga, kurios metu labai susiaurėja plaučių kraujagyslės. Tai sukelia labai didelį slėgį induose, kuriais kraujas iš dešinės širdies pusės patenka į plaučius. Šis slėgis sumažina deguonies kiekį, kurį kraujas gali patekti į plaučius, apsunkindamas fizinį aktyvumą.Plečiant šias kraujagysles sumažėja kraujospūdis ir pagerėja simptomai.
Pacientams, sergantiems sistemine skleroze ir besitęsiančiomis skaitmeninėmis opomis, bosentanas pagerina pirštų ir pirštų kraujotaką, neleidžia atsirasti naujų skaitmeninių opų.
Kaip buvo tiriamas Tracleer?
Su PAH Tracleer plėvele dengtos tabletės buvo tirtos keturiuose pagrindiniuose tyrimuose: dviejuose tyrimuose, kuriuose iš viso dalyvavo 245 suaugusieji, sergantys III ar IV klasės liga, kuri buvo pirminė arba kurią sukėlė sklerodermija, viename tyrime dalyvavo 54 suaugusieji, sergantys III klasės PAH. įgimtas širdies nepakankamumas ir 185 pacientų, sergančių II klasės liga, tyrimas. Tyrimuose Tracleer buvo lyginamas su placebu (gydomojo poveikio neturinčiu preparatu), kurie abu buvo pridėti prie standartinio gydymo. Pagrindinis veiksmingumo rodiklis buvo tai, kiek toli pacientai galėjo nueiti per šešias minutes (būdas įvertinti fizinį krūvį), tačiau II klasės tyrime taip pat buvo vertinamas atsparumo pokyčiai plaučių kraujagyslėse ( Vienas tyrimas taip pat buvo atliktas su plėvele dengtomis tabletėmis, kuriose dalyvavo 19 vaikų nuo 3 iki 15 metų. Tolesniame tyrime buvo tiriamas Tracleer disperguojamųjų tablečių poveikis 36 vaikams, sergantiems PAH ir nuo 2 iki 2 metų amžiaus. 11 metų.
Sisteminės sklerozės ir skaitmeninių opų atveju dviejuose tyrimuose Tracleer plėvele dengtos tabletės buvo lyginamos su placebu, iš viso dalyvavo 312 suaugusiųjų. Pagrindinis veiksmingumo rodiklis buvo pagrįstas naujų skaitmeninių opų, atsiradusių per tyrimus, skaičiumi. Viename iš tyrimų taip pat buvo vertinamas Tracleer poveikis 190 pacientų gijimui, įvertinant laiką, kurio prireikė visiškai išgydyti. kiekvienam pacientui pasirenkama konkreti skaitmeninė opa.
Kokia Tracleer nauda atsiskleidė tyrimų metu?
III ar IV klasės PAH, kuris buvo pirminis arba kurį sukėlė sklerodermija, du tyrimai parodė, kad Tracleer gydomi pacientai po 16 savaičių galėjo vaikščioti ilgiau nei pacientai, vartoję placebą (pagrindiniame tyrime - 44 metrais daugiau), tačiau nedaugelis pacientų, sergančių IV klasės liga, patvirtino narkotikų vartojimą šioje grupėje. Panašūs rezultatai buvo gauti pacientams, sergantiems įgimtu širdies nepakankamumu.
Pacientams, sergantiems II klasės liga, Tracleer po šešių gydymo mėnesių sumažino kraujagyslių pasipriešinimą 23%, palyginti su placebu, tačiau atstumas, kurį pacientai galėjo nueiti per šešias minutes, abiejose grupėse buvo panašus.
Pagerėjimas buvo pastebėtas ir tiriant vaikus, vartojančius plėvele dengtas tabletes. Disperguojamųjų tablečių tyrimo metu bosentano koncentracija buvo mažesnė, nei tikėtasi, nei kitų tyrimų rezultatai, ir jo negalima padidinti vartojant didesnę Tracleer dozę. Tačiau PAH išliko stabilus beveik visiems vaikams per 12 gydymo savaičių, o daugumos vaikų PAH išliko stabilus mažiausiai 18 mėnesių.
Sisteminės sklerozės ir skaitmeninių opų atveju Tracleer veiksmingiau mažino naujų skaitmeninių opų atsiradimą nei placebas. Pirmojo tyrimo metu Tracleer vartojantiems pacientams po 16 savaičių vidutiniškai atsirado 1,4 naujos skaitmeninės opos, palyginti su 2,7 pacientų, vartojusių placebą. Panašūs rezultatai buvo pastebėti ir antrajame tyrime po 24 savaičių, tačiau „Tracleer“ neturėjo įtakos skaitmeniniam opų gijimui.
Kokia rizika siejama su Tracleer?
PAH atveju dažniausiai pasitaikantis Tracleer šalutinis poveikis (pastebėtas daugiau nei 1 iš 10 pacientų) yra galvos skausmas ir nenormalūs kepenų tyrimai.Pacientams, sergantiems skaitmeninėmis opomis, dauguma šalutinių reiškinių (pasireiškę daugiau nei 1 iš 10 pacientų) yra nenormalūs kepenų tyrimai, edema (patinimas) ir skysčių susilaikymas. Atsižvelgdamas į kepenų sutrikimų išsivystymo riziką, gydytojas įvertins kepenų fermentų kiekį prieš gydymą ir kiekvieną mėnesį gydymo Tracleer metu. Išsamų visų šalutinių reiškinių, apie kuriuos pranešta gydant Tracleer, sąrašą galima rasti pakuotės lapelyje.
Kai kurių vaistų (pvz., Kontraceptinių tablečių) veiksmingumą gali paveikti Tracleer vartojimas vienu metu. Daugiau informacijos rasite pakuotės lapelyje.
Tracleer negalima vartoti žmonėms, kurie gali būti itin jautrūs (alergiški) bosentanui ar bet kuriai kitai medžiagai. Tracleer negalima vartoti pacientams, sergantiems kepenų ligomis, nėščioms ar galinčioms pastoti moterims, arba pacientams, vartojantiems ciklosporiną A (vaistą, veikiantį imuninę sistemą).
Kodėl Tracleer buvo patvirtintas?
Žmonėms skirtų vaistinių preparatų komitetas (CHMP) nusprendė, kad gydant PAH sergančius pacientus ir mažinant naujų skaitmeninių opų skaičių pacientams, sergantiems sistemine skleroze ir besitęsiančiomis skaitmeninėmis opomis, Tracleer nauda yra didesnė už keliamą riziką. Komitetas rekomendavo suteikti Tracleer rinkodaros teisę.
Iš pradžių Tracleer buvo suteiktas leidimas „išskirtinėmis aplinkybėmis“, nes, kadangi PAH yra reta liga, pirminio patvirtinimo metu turėta nedaug informacijos. Kadangi farmacijos bendrovė pateikė prašomą papildomą informaciją, sąlyga nurodyta „išskirtinėmis aplinkybėmis“. buvo pašalintas 2004 m. lapkričio 30 d.
Kokių priemonių imamasi siekiant užtikrinti saugų Tracleer vartojimą?
Bendrovė, gaminanti „Tracleer“, kiekvienoje valstybėje narėje pateiks informacijos rinkinius, skirtus vaistą skiriantiems vaistams, ir informacinį lapelį pacientams, kuriame bus paaiškinta „Tracleer“ sauga (ypač jos poveikis kepenims ir nėštumo metu) ir susijusi sąveika. Bendrovė taip pat atidžiai stebės vaisto platinimą kiekvienoje valstybėje narėje ir rinks informaciją apie jo vartojimą pacientams, sergantiems sistemine skleroze ir besitęsiančiomis skaitmeninėmis opomis.
Kita informacija apie „Tracleer“:
2002 m. Gegužės 15 d. Europos Komisija suteikė „Actelion Registration Ltd“ visoje Europos Sąjungoje galiojantį „rinkodaros leidimą“. Šis leidimas buvo atnaujintas 2007 m. Gegužės 15 d.
Retųjų vaistų komiteto Tracleer nuomonės santraukos yra prieinamos čia (PAH) e čia (sisteminė sklerozė).
Pilną Tracleer EPAR versiją rasite čia.
Paskutinis šios santraukos atnaujinimas: 2009 m.
Šiame puslapyje paskelbta informacija apie „Tracleer - bosentan“ gali būti pasenusi arba neišsami. Norėdami teisingai naudoti šią informaciją, žr. Atsakomybės apribojimo ir naudingos informacijos puslapį.