Veikliosios medžiagos: Eltrombopag
Revolade 12,5 mg plėvele dengtos tabletės
Revolade 25 mg plėvele dengtos tabletės
Revolade 50 mg plėvele dengtos tabletės
Revolade 75 mg plėvele dengtos tabletės
Kodėl vartojamas Revolade? Kam tai?
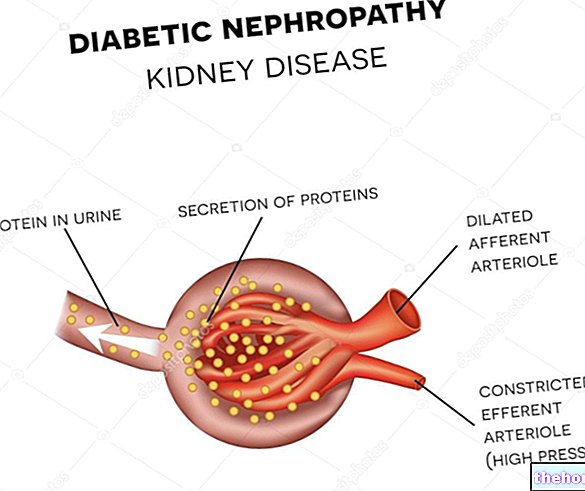
Revolade sudėtyje yra eltrombopago, kuris priklauso vaistų, vadinamų trombopoetino receptorių agonistais, grupei. Jis vartojamas siekiant padidinti trombocitų skaičių kraujyje. Trombocitai yra kraujo ląstelės, kurios padeda sumažinti arba užkirsti kelią kraujavimui.
- Revolade gydomas „kraujo krešėjimo sutrikimas, vadinamas autoimunine (idiopatine) trombocitopenine purpura (ITP) pacientams (vyresniems nei 1 metų), kurie jau vartojo kitus neveiksmingus vaistus (kortikosteroidus ar imunoglobulinus).
ITP sukelia mažas trombocitų kiekis kraujyje (trombocitopenija). Žmonėms, sergantiems ITP, yra didesnė kraujavimo rizika. Pacientams, sergantiems ITP, simptomai gali būti petechijos (mažos plokščios raudonos apvalios dėmės ant odos), mėlynės, kraujavimas iš nosies (kraujavimas iš nosies), kraujavimas iš dantenų ir nesugebėjimas kontroliuoti kraujavimo įpjovimų ar žaizdų atveju.
- Revolade taip pat gali būti vartojamas mažam trombocitų skaičiui (trombocitopenijai) gydyti pacientams, sergantiems hepatito C virusu (HCV), jei jiems pasireiškė nepageidaujamų reakcijų vartojant interferoną. Daugeliui žmonių, sergančių hepatitu C, trombocitų skaičius yra mažas. dėl pačios ligos, bet ir dėl kai kurių antivirusinių vaistų, naudojamų jai gydyti.
- Revolade taip pat galima gydyti suaugusius pacientus, kurių kraujo ląstelių skaičius sumažėjęs dėl sunkios aplastinės anemijos (SAS).
Kontraindikacijos Kai Revolade vartoti negalima
Revolade vartoti negalima
- jeigu yra alergija eltrombopagui arba bet kuriai pagalbinei šio vaisto medžiagai (Revolade sudėtis).
- Pasitarkite su gydytoju, jei manote, kad tai tinka jums.
Atsargumo priemonės Vartojant prieš vartojant Revolade
Pasitarkite su gydytoju, prieš pradėdami vartoti Revolade:
- jeigu sergate kepenų liga. Žmonėms, kuriems yra mažas trombocitų skaičius ir lėtinė (ilgai trunkanti) pažengusi kepenų liga, yra didesnė rizika patirti šalutinį poveikį, įskaitant kepenų pažeidimą ir gyvybei pavojingus kraujo krešulius. Jei gydytojas mano, kad Revolade vartojimo nauda yra didesnė už riziką, gydymo metu būsite atidžiai stebimi.
- jeigu Jums yra kraujo krešulių susidarymo venose ar arterijose rizika arba žinote, kad kraujo krešuliai yra dažni jūsų šeimoje.
- Jums gali būti padidėjusi kraujo krešulių susidarymo rizika:
- jeigu esate vyresnio amžiaus
- jei ilgą laiką turėjote gulėti lovoje
- jeigu sergate naviku
- jeigu vartojate kontraceptines tabletes ar pakeičiamąją hormonų terapiją
- jei neseniai atlikote operaciją arba patyrėte fizinę traumą - jei turite labai antsvorio (nutukę)
- jeigu esate rūkalius
- jeigu sergate pažengusia lėtine kepenų liga
- Jei kuris nors iš šių punktų tinka Jums, prieš pradėdami gydymą, pasakykite gydytojui. Revolade vartoti negalima, nebent gydytojas mano, kad laukiama nauda yra didesnė už krešulių susidarymo riziką.
- jeigu sergate katarakta (akies lęšio drumstumu)
- jeigu sergate kitu kraujo sutrikimu, pvz., mielodisplastiniu sindromu (MDS). Prieš pradėdamas vartoti Revolade, gydytojas atliks tyrimus, kad įsitikintų, jog neturite šio kraujo sutrikimo. Jei sergate MDS ir vartojate Revolade, MDS gali pablogėti.
- Pasakykite gydytojui, jei kuri nors iš šių būklių tinka Jums.
Akių tyrimas
Gydytojas rekomenduos patikrinti kataraktą. Jei neatliekate įprastų akių egzaminų, gydytojas suplanuos reguliarų egzaminą. Jis taip pat gali būti patikrintas dėl bet kokio kraujavimo tinklainėje arba aplink ją (šviesai jautrių ląstelių sluoksnis akies gale).
Jam reikės reguliarių egzaminų
Prieš pradėdamas vartoti Revolade, gydytojas atliks kraujo tyrimus, kad patikrintų jūsų kraujo ląsteles, įskaitant trombocitus. Šie tyrimai bus kartojami kas tam tikrą laiką, kol vartojate vaistą.
Kraujo tyrimai kepenų funkcijai
Revolade gali pakeisti kraujo tyrimų rezultatus, kurie gali rodyti kepenų pažeidimą - kai kurių kepenų fermentų, ypač bilirubino ir alanino / aspartato transaminazių, padidėjimą. Jei esate gydomas interferonu kartu su Revolade, kad sumažėtų trombocitų skaičius dėl hepatito C, kai kurie kepenų sutrikimai gali pablogėti.
Prieš pradėdami vartoti Revolade ir gydymo metu, turėsite atlikti kraujo tyrimus kepenų funkcijai patikrinti. Jums gali tekti nutraukti Revolade vartojimą, jei šių fermentų kiekis padidėja per daug arba atsiranda fizinių kepenų pažeidimo požymių.
- Perskaitykite šio lapelio 4 skyriuje pateiktą informaciją „Kepenų problemos“
Kraujo tyrimai trombocitų skaičiui nustatyti
Nustojus vartoti Revolade, trombocitų skaičius greičiausiai vėl sumažės per kelias dienas. Jūsų trombocitų skaičius bus stebimas ir gydytojas jums pasakys apie tinkamas atsargumo priemones.
Labai didelis trombocitų skaičius gali padidinti kraujo krešulių riziką, tačiau kraujo krešuliai taip pat gali susidaryti esant normaliam ar net mažam trombocitų skaičiui. Gydytojas koreguos Revolade dozę, kad užtikrintų, jog trombocitų skaičius per daug nepadidėtų.
Nedelsdami kreipkitės medicininės pagalbos, jei turite kokių nors iš šių kraujo krešulio požymių:
- patinimas, skausmas ar jautrumas vienoje kojoje
- staigus dusulys, ypač kartu su aštriu krūtinės skausmu ar greitu kvėpavimu
- pilvo (skrandžio) skausmas, pilvo patinimas, kraujas išmatose.
Testai kaulų čiulpams patikrinti
Žmonėms, kuriems gali kilti kaulų čiulpų problemų, tokie vaistai kaip Revolade gali pabloginti problemas. Kaulų čiulpų pokyčių požymiai gali pasireikšti kaip kraujo tyrimų rezultatų nukrypimai. Gydydamas Revolade, gydytojas gali atlikti tyrimus, kad patikrintų jūsų kaulų čiulpus.
Kraujavimo iš virškinimo tyrimai
Jei esate gydomas interferono vaistais kartu su Revolade, nutraukus Revolade vartojimą, jums bus patikrinta, ar nėra kraujavimo skrandyje ar žarnyne požymių.
Širdies patikrinimas
Gydytojas gali manyti, kad gydymo Revolade metu būtina patikrinti jūsų širdį ir atlikti elektrokardiogramą (EKG).
Vaikai ir paaugliai
Revolade nerekomenduojama vartoti jaunesniems nei 1 metų vaikams, sergantiems ITP. Taip pat nerekomenduojama vartoti jaunesniems nei 18 metų žmonėms, kurių trombocitų skaičius yra mažas dėl hepatito C ar sunkios aplazinės anemijos.
Sąveika Kokie vaistai ar maistas gali pakeisti Revolade poveikį
Jeigu vartojate arba neseniai vartojote kitų vaistų arba dėl to nesate tikri, apie tai pasakykite gydytojui arba vaistininkui.
Kai kurie įprasti vaistai sąveikauja su Revolade, įskaitant receptinius ir nereceptinius vaistus bei mineralus. Jie apima:? antacidiniai vaistai virškinimo sutrikimams, rėmeniui ar skrandžio opoms gydyti Kada vartoti)
- vaistų, vadinamų statinais, cholesterolio kiekiui mažinti
- kai kurie vaistai ŽIV infekcijai gydyti, pvz., lopinaviras ir (arba) ritonaviras
- ciklosporinas, naudojamas persodinant ir sergant imuninėmis ligomis
- mineralų, tokių kaip geležis, kalcis, magnis, aliuminis, selenas ir cinkas, kurių galima rasti vitaminų ir mineralų papilduose (kada vartoti)
- vaistų, tokių kaip metotreksatas ir topotekanas, vėžiui gydyti
- Pasakykite gydytojui, jei vartojate kurį nors iš šių vaistų. Kai kurių iš jų negalima vartoti kartu su Revolade, arba gali reikėti koreguoti vartojamą dozę arba keisti vartojimo laiką. Gydytojas peržiūrės visus vartojamus vaistus ir prireikus pasiūlys juos pakeisti.
Kraujavimo rizika yra didesnė, jei kartu vartojate vaistų nuo kraujo krešulių. Jūsų gydytojas tai aptars su jumis.
Jei vartojate kortikosteroidų, danazolo ir (arba) azatioprino, vartojant Revolade, gali tekti vartoti mažesnę dozę arba nutraukti jų vartojimą.
Revolade vartojimas su maistu ir gėrimais
Nevartokite Revolade su gėrimais, pieno produktais ir sūriu, nes pieno produktuose esantis kalcis turi įtakos vaisto absorbcijai.
Įspėjimai Svarbu žinoti, kad:
Nėštumas ir žindymo laikotarpis
Nenaudokite Revolade, jei esate nėščia, nebent gydytojas to specialiai rekomenduoja. Revolade poveikis nėštumo metu nežinomas.
- Pasakykite gydytojui, jei esate nėščia, manote, kad galbūt esate nėščia arba planuojate pastoti.
- Vartodami Revolade, naudokite patikimą kontracepcijos metodą, kad išvengtumėte nėštumo
- Jeigu pastojote vartodama Revolade, pasakykite gydytojui.
Nevartokite krūties, kol vartojate Revolade. Nežinoma, ar Revolade patenka į motinos pieną.
- Jeigu maitinate krūtimi ar planuojate žindyti kūdikį, pasakykite gydytojui.
Vairavimas ir mechanizmų valdymas
- Revolade gali svaigti galva ir sukelti kitokį šalutinį poveikį, dėl kurio mažiau dėmesio.
- Nevairuokite transporto priemonių ir nevaldykite mechanizmų, nebent esate tikri, kad nesate paveikti.
Dozė, vartojimo būdas ir laikas Kaip vartoti Revolade: Dozavimas
Visada vartokite šį vaistą tiksliai kaip nurodė gydytojas. Jei abejojate, pasitarkite su gydytoju arba vaistininku. Nekeiskite Revolade dozės ar tvarkaraščio, nebent gydytojas arba vaistininkas patars tai padaryti. Kol vartojate Revolade, jus gydys gydytojas, turintis specialios patirties gydant jūsų būklę.
Kiek vartoti
Dėl ITP
Suaugusiesiems ir vaikams (nuo 6 iki 17 metų) - rekomenduojama pradinė ITP dozė yra viena Revolade 50 mg tabletė per parą. Jei esate Rytų Azijos kilmės (kinų, japonų, taivaniečių, tailandiečių ar korėjiečių), gali tekti pradėti nuo mažesnės 25 mg dozės.
Vaikams (nuo 1 iki 5 metų) - rekomenduojama pradinė ITP dozė yra viena 25 mg Revolade tabletė per parą.
Sergant hepatitu C.
Suaugusieji - Rekomenduojama pradinė hepatito C dozė yra viena 25 mg Revolade tabletė per parą. Jei esate Rytų Azijos kilmės (kinų, japonų, taivaniečių, tajų ar korėjiečių), pradėsite vartoti tą pačią 25 mg dozę.
Dėl SAA
Suaugusiesiems - rekomenduojama pradinė AAS dozė yra viena Revolade 50 mg tabletė per parą. Jei esate Rytų Azijos kilmės (kinų, japonų, taivaniečių, tailandiečių ar korėjiečių), gali tekti pradėti nuo mažesnės 25 mg dozės.
Revolade gali veikti 1–2 savaites. Atsižvelgdamas į Jūsų atsaką į Revolade, gydytojas gali rekomenduoti keisti paros dozę.
Kaip gerti tabletes
Nurykite visą tabletę, užsigerdami vandeniu.
Kada jį paimti
Įsitikinti, kad-
- likus 4 valandoms iki Revolade vartojimo
- ir per 2 valandas po Revolade vartojimo
Jūs nevartojate nė vieno iš šių:
- maisto produktai, tokie kaip sūris, sviestas, jogurtas ar ledai
- pieno ar pieno pagrindo kokteiliai, gėrimai, kurių sudėtyje yra pieno, jogurto ar grietinėlės
- antacidiniai vaistai, vaistai nuo virškinimo ir rėmens
- kai kurie vitaminų ir mineralų papildai, įskaitant geležį, kalcį, magnį, aliuminį, seleną ir cinką.
Jei taip atsitiks, vaistas nebus tinkamai absorbuojamas į organizmą.
Jei reikia daugiau patarimų dėl tinkamo maisto ir gėrimų, kreipkitės į gydytoją.
Pamiršus pavartoti Revolade
Kitą dozę gerkite įprastu laiku. Nevartokite daugiau kaip vienos Revolade dozės per dieną.
Nustojus vartoti Revolade
Nenutraukite Revolade vartojimo nepasitarę su gydytoju. Jei gydytojas patars nutraukti gydymą, trombocitų skaičius bus tikrinamas kiekvieną savaitę keturias savaites.
Jeigu kiltų daugiau klausimų dėl šio vaisto vartojimo, kreipkitės į gydytoją arba vaistininką.
Perdozavimas Ką daryti pavartojus per didelę Revolade dozę
Nedelsdami kreipkitės į gydytoją arba vaistininką. Jei įmanoma, parodykite jiems dėžutę arba šį lapelį. Bet kokie šalutinio poveikio požymiai ar simptomai bus patikrinti ir nedelsiant tinkamai gydomi.
Šalutinis poveikis Koks yra Revolade šalutinis poveikis
Šis vaistas, kaip ir visi kiti, gali sukelti šalutinį poveikį, nors jis pasireiškia ne visiems žmonėms.
Simptomai, į kuriuos reikia atkreipti dėmesį: kreipkitės į gydytoją
Žmonėms, vartojantiems Revolade dėl ITP ar mažo trombocitų kiekio kraujyje dėl hepatito C, gali atsirasti galimai rimto šalutinio poveikio požymių. Svarbu pasakyti gydytojui, jei atsiranda šie simptomai.
Didesnė kraujo krešulių rizika
Kai kuriems žmonėms gali būti didesnė kraujo krešulių rizika, o tokie vaistai kaip Revolade gali pabloginti šią problemą. Staigus kraujagyslių užsikimšimas kraujo krešuliu yra nedažnas šalutinis poveikis ir gali pasireikšti ne daugiau kaip 1 iš 100 žmonių.
Nedelsdami kreipkitės į gydytoją, jei atsiranda kraujo krešulio požymių ir simptomų, tokių kaip:
- patinimas, skausmas, šiluma, paraudimas ar jautrumas vienoje kojoje
- staigus dusulys, ypač kartu su aštriu krūtinės skausmu ar greitu kvėpavimu
- pilvo (skrandžio) skausmas, pilvo patinimas, kraujas išmatose.
Kepenų problemos
Revolade gali sukelti kraujo tyrimų pokyčius ir būti kepenų pažeidimo požymių. Kepenų sutrikimai (fermentų kiekio padidėjimas, nustatytas kraujo tyrimuose) yra dažni ir gali pasireikšti ne daugiau kaip 1 iš 10 žmonių. Kiti kepenų sutrikimai (netinkama tulžies nutekėjimas) yra nedažni ir gali pasireikšti ne daugiau kaip 1 iš 10 žmonių.
Jei turite kokių nors iš šių kepenų sutrikimo požymių:
- odos arba akių baltymų pageltimas (gelta)
- neįprastai tamsios spalvos šlapimas
- Nedelsdami pasakykite gydytojui.
Kraujavimas ar kraujosruvos nutraukus gydymą
Per dvi savaites nutraukus Revolade vartojimą, trombocitų skaičius paprastai sumažės iki to, koks buvo prieš pradedant vartoti Revolade.Mažesnis trombocitų skaičius gali padidinti kraujavimo ar kraujosruvų riziką. Nustojus vartoti Revolade, gydytojas tikrins trombocitų skaičių mažiausiai 4 savaites.
- Pasakykite savo gydytojui, jei nutraukus Revolade vartojimą atsiranda kraujavimas ar kraujosruvos.
Kai kuriems žmonėms, nutraukus peginterferono, ribavirino ir Revolade vartojimą, kraujavimas iš virškinimo sistemos. Simptomai:
- tamsios išmatos, išmatų spalvos pasikeitimas yra nedažnas šalutinis poveikis, kuris gali pasireikšti ne daugiau kaip 1 iš 100 žmonių)
- kraujas išmatose
- išmesti kraują ar kažką panašaus į kavos tirščius
- Nedelsdami pasakykite gydytojui, jei pasireiškė kuris nors iš šių simptomų.
Kitas galimas šalutinis poveikis suaugusiesiems, sergantiems ITP
Dažnas šalutinis poveikis Gali pasireikšti ne daugiau kaip 1 iš 10 žmonių:
- pykinimas
- viduriavimas
- katarakta (akies lęšio drumstimas)
- sausa akis
- neįprastas plaukų slinkimas ar retėjimas
- bėrimas
- niežulys
- raumenų skausmas, raumenų spazmai
- nugaros skausmas
- kaulų skausmas
- dilgčiojimas ir tirpimas rankose ar kojose
- sunkus menstruacinis ciklas
- burnos opos.
Dažnas šalutinis poveikis, kuris gali pasireikšti atliekant kraujo tyrimą:
- padidėjęs kepenų fermentų kiekis
- padidėjęs bilirubino kiekis (kepenų gaminama medžiaga)
- padidėjęs kai kurių baltymų kiekis.
Nedažnas šalutinis poveikis
Tai gali pasireikšti ne daugiau kaip 1 iš 100 žmonių:
- kraujo tiekimo į širdies dalį nutraukimas
- staigus dusulys, ypač kartu su aštriu krūtinės skausmu ir (arba) greitu kvėpavimu, kuris gali būti kraujo krešulio plaučiuose požymis (žr. „Didesnė kraujo krešulių rizika“ 4 skyriaus pradžioje).
- dalies plaučių funkcijos praradimas dėl plaučių arterijos užsikimšimo
- kepenų sutrikimai, įskaitant akių ir odos pageltimą
- greitas širdies plakimas, nereguliarus širdies plakimas, melsva odos spalva
- širdies ritmo sutrikimai (QT intervalo pailgėjimas)
- venų uždegimas
- sumušimai
- gerklės skausmas ir diskomfortas ryjant, plaučių, sinusų, tonzilių, nosies ir gerklės uždegimas
- įtaką
- plaučių uždegimas
- apetito praradimas
- skausmingas sąnarių patinimas, kurį sukelia šlapimo rūgštis (podagra)
- miego sutrikimas, depresija, susidomėjimo praradimas, nuotaikų kaita
- mieguistumas, pusiausvyros, kalbos ir nervų funkcijos sutrikimai, migrena, drebulys
- akių problemos, įskaitant neryškų ir ne tokį aiškų regėjimą
- ausų skausmas, galvos svaigimas
- nosies, gerklės ir sinusų problemos, kvėpavimo sutrikimai miego metu
- virškinimo sistemos sutrikimai, įskaitant: vėmimą, vidurių pūtimą, dažną tuštinimąsi, pilvo skausmą ir jautrumą, apsinuodijimą maistu
- tiesiosios žarnos vėžys
- burnos problemos, įskaitant burnos sausumą ar skausmą, liežuvio jautrumą, dantenų kraujavimą,
- odos pokyčiai, įskaitant gausų prakaitavimą, pūslėtas ir niežtintis bėrimas, raudonos dėmės, išvaizdos pokyčiai
- saulės nudegimas
- paraudimas ar patinimas aplink žaizdą
- kraujavimas aplink kateterį (jei yra)
- svetimkūnio pojūtis injekcijos vietoje
- raumenų silpnumas
- inkstų sutrikimai, įskaitant: inkstų uždegimą, gausų šlapinimąsi naktį, inkstų nepakankamumą, šlapimo takų infekciją, baltųjų kraujo ląstelių kiekį šlapime
- negalavimas, karščiavimas, karščio pojūtis, krūtinės skausmas
- šaltas prakaitas
- dantenų uždegimas
- odos infekcija.
Nedažnas šalutinis poveikis, kuris gali pasireikšti atliekant kraujo tyrimą:
- raudonųjų kraujo kūnelių (anemija), baltųjų kraujo kūnelių ir trombocitų kiekio sumažėjimas
- padidėjęs raudonųjų kraujo kūnelių skaičius
- kraujo morfologijos pokyčiai
- šlapimo rūgšties, kalcio ir kalio kiekio pokyčiai.
Kitas galimas šalutinis poveikis vaikams, sergantiems ITP
Labai dažnas šalutinis poveikis
Jie gali pasireikšti daugiau nei 1 iš 10 vaikų:
- gerklės skausmas, sloga, nosies užgulimas ir čiaudulys
- nosies, sinusų, gerklės ir viršutinių kvėpavimo takų infekcija, peršalimas (viršutinių kvėpavimo takų infekcija)
- viduriavimas.
Dažnas šalutinis poveikis
Tai gali pasireikšti ne daugiau kaip 1 iš 10 vaikų:
- sunku užmigti (nemiga)
- pilvo skausmas
- dantų skausmas
- kosulys
- skausmas nosyje ir gerklėje
- nosies niežulys, sloga ar nosies užgulimas
- aukštos temperatūros.
Kitas galimas šalutinis poveikis žmonėms, sergantiems hepatitu C.
Labai dažnas šalutinis poveikis
Jie gali pasireikšti daugiau kaip 1 iš 10 žmonių:
- galvos skausmas
- sumažėjęs apetitas
- nemiga
- kosulys
- pykinimas, viduriavimas
- raumenų skausmas, niežulys, energijos trūkumas, aukšta temperatūra, neįprastas plaukų slinkimas, silpnumo jausmas, į gripą panaši liga, rankų ir kojų patinimas, šaltkrėtis.
Labai dažnas šalutinis poveikis, kuris gali pasireikšti atliekant kraujo tyrimą:
- raudonųjų kraujo kūnelių skaičiaus sumažėjimas (anemija).
Dažnas šalutinis poveikis
Tai gali pasireikšti ne daugiau kaip 1 iš 10 žmonių:
- šlapimo sistemos infekcijos
- nosies ertmės, gerklės ir burnos uždegimas, į gripą panašūs simptomai, burnos džiūvimas, burnos skausmas ar danties skausmas
- svorio metimas
- miego sutrikimai, nenormalus mieguistumas, sumišimas, depresija, nerimas, susijaudinimas
- galvos svaigimas, koncentracijos ir atminties problemos
- dilgčiojimas ar tirpimas rankose ar kojose
- uždegimas smegenyse
- akių sutrikimai, įskaitant kataraktą (akies lęšio drumstimą); akių sausumą, mažas geltonas nuosėdas tinklainėje, akių baltymų pageltimą.
- kraujavimas tinklainėje arba aplink ją (yra akies gale)
- galvos svaigimas, širdies plakimas, dusulys
- kosulys su skrepliu
- virškinimo sistemos sutrikimai, įskaitant: vėmimą, skrandžio skausmą, nevirškinimą, vidurių užkietėjimą, skrandžio patinimą, skonio sutrikimą, skrandžio uždegimą, hemorojus, kraujagyslių patinimą ir kraujavimą iš stemplės (ezofagitą), žarnyno sudirginimą
- kepenų sutrikimai, įskaitant: kraujo krešulių susidarymą, akių arba odos pageltimą (gelta), kepenų vėžį
- odos pokyčiai, įskaitant: bėrimą, sausą odą, egzemą, odos paraudimą, niežulį, gausų prakaitavimą, neįprastą odos augimą? sąnarių skausmas, nugaros skausmas, kaulų skausmas, rankų ar kojų skausmas, raumenų spazmai
- dirglumas, bendras negalavimas, krūtinės skausmas ir diskomfortas
- reakcijos injekcijos vietoje
- širdies ritmo sutrikimai (QT intervalo pailgėjimas).
Dažnas šalutinis poveikis, kuris gali pasireikšti atliekant kraujo tyrimą:
- padidėjęs cukraus kiekis kraujyje (hiperglikemija)
- baltųjų kraujo ląstelių skaičiaus sumažėjimas
- kraujo baltymų sumažėjimas
- raudonųjų kraujo kūnelių irimas (hemolizinė anemija)
- padidėjęs bilirubino kiekis (kepenų gaminama medžiaga)
- kraujo krešėjimą kontroliuojančių fermentų pokyčiai.
Nedažnas šalutinis poveikis
Tai gali pasireikšti ne daugiau kaip 1 iš 100 žmonių:
- skausmas šlapinantis.
Nedažnas šalutinis poveikis
Dažnis negali būti įvertintas pagal turimus duomenis
- odos spalvos pasikeitimas
Gydant Revolade, pacientams, sergantiems sunkia aplazine anemija (SAS), pasireiškė toks šalutinis poveikis.
Labai dažnas šalutinis poveikis
Tai gali pasireikšti ne daugiau kaip 1 iš 10 žmonių:
- kosulys
- galvos skausmas
- švokštimas (dusulys)
- skausmas nosyje ir gerklėje
- bėganti nosis
- pilvo skausmas
- viduriavimas
- pykinimas
- sumušimai
- sąnarių skausmas
- raumenų spazmai
- rankų, kojų, rankų ir kojų skausmas
- galvos svaigimas
- jaučiasi labai pavargęs
- karščiavimas
- nemiga
Labai dažnas šalutinis poveikis, kuris gali pasireikšti atliekant kraujo tyrimą:
- padidėjęs kepenų fermentų (transaminazių) kiekis. Kraujo tyrimai gali parodyti nenormalius kaulų čiulpų ląstelių pokyčius.
Dažnas šalutinis poveikis
Tai gali pasireikšti ne daugiau kaip 1 iš 10 žmonių:
- nerimas
- depresija
- Jaučiasi šalta
- bendras negalavimas
- akių problemos, įskaitant: neryškus ir ne toks aiškus regėjimas, katarakta, dėmių matymas akyje dėl netobulo stiklakūnio skaidrumo, sausos akys, niežtinčios akys, odos ar akių baltymų pageltimas
- kraujavimas iš nosies
- kraujavimas iš dantenų
- pūslės burnoje
- virškinimo sistemos sutrikimai, tokie kaip: vėmimas, apetito pokyčiai (padidėjimas ar sumažėjimas), skrandžio skausmas / diskomfortas, pilvo pūtimas, vėjas, išmatų spalvos pasikeitimas
- alpimas
- odos problemos, įskaitant: mažas raudonas arba purpurines dėmeles, kurias sukelia kraujavimas iš odos (petechijos), bėrimas, niežėjimas, odos pažeidimai
- nugaros skausmas
- skausmas raumenyse
- kaulų skausmas
- silpnumas
- audinių, dažniausiai apatinių galūnių, patinimas dėl vandens susilaikymo
- nenormaliai pasikeitęs šlapimas
- blužnies kraujo tiekimo sutrikimas (blužnies infarktas).
Dažnas šalutinis poveikis, kuris gali pasireikšti atliekant kraujo tyrimą:
- padidėjęs fermentų kiekis dėl raumenų sužalojimo (kreatino fosfokinazė)
- geležies kaupimasis kraujyje
- sumažėjęs baltųjų kraujo kūnelių skaičius (neutropenija)
- sumažėjęs cukraus kiekis kraujyje (hipoglikemija)
- padidėjęs bilirubino kiekis (kepenų gaminama medžiaga)
Nedažnas šalutinis poveikis
Dažnis negali būti įvertintas pagal turimus duomenis
- odos spalvos pasikeitimas
Pranešimas apie šalutinį poveikį
Jeigu pasireiškė šalutinis poveikis (net jeigu jis šiame lapelyje nenurodytas), kreipkitės į gydytoją, vaistininką arba slaugytoją. Apie šalutinį poveikį taip pat galite pranešti tiesiogiai naudodamiesi nacionaline pranešimo sistema. Pranešdami apie šalutinį poveikį galite padėti suteikti daugiau informacijos informacija apie šio vaisto saugumą.
Galiojimo laikas ir išlaikymas
Šį vaistą laikykite vaikams nepastebimoje ir nepasiekiamoje vietoje.
Ant dėžutės ir lizdinės plokštelės po „Tinka iki“ nurodytam tinkamumo laikui pasibaigus, šio vaisto vartoti negalima. Vaistas tinkamas vartoti iki paskutinės nurodyto mėnesio dienos.
Šiam vaistui specialių laikymo sąlygų nereikia.
Nemeskite vaistų į kanalizaciją ar buitines atliekas. Paklauskite vaistininko, kaip išmesti nebenaudojamus vaistus. Tai padės apsaugoti aplinką.
Kita informacija
Revolade sudėtis
Veiklioji Revolade medžiaga yra eltrombopagas.
12,5 mg plėvele dengtos tabletės
Kiekvienoje plėvele dengtoje tabletėje yra eltrombopago olamino, atitinkančio 12,5 mg eltrombopago.
25 mg plėvele dengtos tabletės
Kiekvienoje plėvele dengtoje tabletėje yra eltrombopago olamino, atitinkančio 25 mg eltrombopago.
50 mg plėvele dengtos tabletės
Kiekvienoje plėvele dengtoje tabletėje yra eltrombopago olamino, atitinkančio 50 mg eltrombopago.
75 mg plėvele dengtos tabletės
Kiekvienoje plėvele dengtoje tabletėje yra eltrombopago olamino, atitinkančio 75 mg eltrombopago.
Pagalbinės medžiagos yra hipromeliozė, makrogolis 400, magnio stearatas, manitolis (E421), mikrokristalinė celiuliozė, povidonas, natrio krakmolo glikolatas, titano dioksidas (E171).
Revolade 50 mg plėvele dengtose tabletėse taip pat yra raudonojo geležies oksido (E172) ir geltonojo geležies oksido (E172).
Revolade 75 mg plėvele dengtose tabletėse taip pat yra raudonojo geležies oksido (E172) ir geltonojo geležies oksido (E172).
Revolade išvaizda ir kiekis pakuotėje
Revolade 12,5 mg plėvele dengtos tabletės yra apvalios, abipus išgaubtos, baltos, vienoje pusėje įspausta „GS MZ1“ ir „12.5“.
Revolade 25 mg plėvele dengtos tabletės yra apvalios, abipus išgaubtos, baltos, vienoje pusėje įspausta „GS NX3“ ir „25“.
Revolade 50 mg plėvele dengtos tabletės yra apvalios, abipus išgaubtos, rudos, vienoje pusėje įspausta „GS UFU“ ir „50“.
Revolade 75 mg plėvele dengtos tabletės yra apvalios, abipus išgaubtos, rausvos, vienoje pusėje įspausta „GS FFS“ ir „75“.
Jie tiekiami aliuminio lizdinėse plokštelėse pakuotėje, kurioje yra 14 arba 28 plėvele dengtos tabletės, ir sudėtinėje pakuotėje, kurioje yra 84 (3 pakuotės po 28) plėvele dengtų tablečių.
Jūsų šalyje gali būti tiekiamos ne visų dydžių pakuotės.
Šaltinio pakuotės lapelis: AIFA (Italijos vaistų agentūra). Turinys paskelbtas 2016 m. Sausio mėn. Pateikta informacija gali būti neatnaujinta.
Norint pasiekti naujausią versiją, patartina apsilankyti AIFA (Italijos vaistų agentūra) svetainėje. Atsisakymas ir naudinga informacija.
01.0 VAISTINIO PREPARATO PAVADINIMAS
PERKELTI TABLETES, Dengtas plėvele
02.0 KOKYBINĖ IR KIEKYBINĖ SUDĖTIS
Revolade 12,5 mg plėvele dengtos tabletės
Kiekvienoje plėvele dengtoje tabletėje yra eltrombopago olamino, atitinkančio 12,5 mg eltrombopago.
Revolade 25 mg plėvele dengtos tabletės
Kiekvienoje plėvele dengtoje tabletėje yra eltrombopago olamino, atitinkančio 25 mg eltrombopago.
Revolade 50 mg plėvele dengtos tabletės
Kiekvienoje plėvele dengtoje tabletėje yra eltrombopago olamino, atitinkančio 50 mg eltrombopago.
Revolade 75 mg plėvele dengtos tabletės
Kiekvienoje plėvele dengtoje tabletėje yra eltrombopago olamino, atitinkančio 75 mg eltrombopago.
Išsamų pagalbinių medžiagų sąrašą žr. 6.1 skyriuje.
03.0 FARMACINĖ FORMA
Plėvele dengta tabletė.
Revolade 12,5 mg plėvele dengtos tabletės
Apvali, abipus išgaubta, balta plėvele dengta tabletė (maždaug 7,9 mm skersmens) su įspaudu „GS MZ1“ ir „12,5“ vienoje pusėje.
Revolade 25 mg plėvele dengtos tabletės
Apvali, abipus išgaubta, balta plėvele dengta tabletė (maždaug 10,3 mm skersmens), vienoje pusėje įspausta „GS NX3“ ir „25“.
Revolade 50 mg plėvele dengtos tabletės
Apvali, abipus išgaubta, ruda plėvele dengta tabletė (maždaug 10,3 mm skersmens) su įspaudu „GS UFU“ ir „50“ vienoje pusėje.
Revolade 75 mg plėvele dengtos tabletės
Apvali, abipus išgaubta, rožinė plėvele dengta tabletė (maždaug 10,3 mm skersmens), vienoje pusėje įspausta „GS FFS“ ir „75“.
04.0 KLINIKINĖ INFORMACIJA
04.1 Terapinės indikacijos
Revolade skiriamas vyresniems nei 1 metų pacientams, sergantiems lėtine autoimunine (idiopatine) trombocitopenine purpura (ITP), kurie yra atsparūs kitiems gydymo būdams (pvz., Kortikosteroidams, imunoglobulinams) (žr. 4.2 ir 5.1 skyrius).
Revolade skirtas suaugusiems pacientams, sergantiems lėtine hepatito C viruso infekcija (Hepatito C virusas(HCV), skirtų trombocitopenijai gydyti, kai trombocitopenijos laipsnis yra pagrindinis veiksnys, neleidžiantis pradėti arba ribojantis galimybę išlaikyti optimalų gydymą interferonu (žr. 4.4 ir 5.1 skyrius).
Revolade skiriamas suaugusiems pacientams, sergantiems sunkia įgyta aplazine anemija (SAA), neatspariais ankstesniam imunosupresiniam gydymui arba stipriai gydytiems ir netinkamiems kraujodaros kamieninių ląstelių transplantacijai (žr. 5.1 skyrių).
04.2 Dozavimas ir vartojimo metodas
Gydymą eltrombopagu reikia pradėti ir tęsti prižiūrint gydytojui, turinčiam hematologinių ligų gydymo ar lėtinio hepatito C ir jo komplikacijų gydymo patirties.
Dozavimas
Reikiamą eltrombopago dozę reikia parinkti individualiai, atsižvelgiant į paciento trombocitų skaičių. Gydymo eltrombopagu tikslas neturėtų būti trombocitų skaičiaus normalizavimas.
Milteliai geriamajai suspensijai gali sukelti didesnį eltrombopago poveikį nei tabletės (žr. 5.2 skyrių). Keičiant geriamąją suspensiją iš tablečių ir miltelių, trombocitų skaičius turi būti stebimas kas savaitę 2 savaites.
Lėtinė autoimuninė (idiopatinė) trombocitopenija
Norint pasiekti ir išlaikyti trombocitų skaičių ≥ 50 000 / μl, reikia naudoti mažiausią eltrombopago dozę. Dozės koregavimas pagrįstas trombocitų skaičiaus atsaku.
Eltrombopago negalima vartoti trombocitų skaičiui normalizuoti. Klinikinių tyrimų metu trombocitų skaičius paprastai padidėjo per 1–2 savaites nuo eltrombopago pradžios ir sumažėjo per 1–2 savaites po gydymo nutraukimo.
Suaugusieji ir 6–17 metų vaikai
Rekomenduojama pradinė eltrombopago dozė yra 50 mg vieną kartą per parą. Rytų Azijos (pvz., Kinų, japonų, taivaniečių, korėjiečių ar tajų) pacientams eltrombopagą reikia pradėti gydyti mažesne 25 mg doze vieną kartą per parą (žr. 5.2 skyrių).
Vaikų populiacija nuo 1 iki 5 metų
Rekomenduojama pradinė eltrombopago dozė yra 25 mg vieną kartą per parą.
Dozės stebėjimas ir keitimas
Pradėjus gydymą eltrombopagu, dozę reikia koreguoti, kad būtų pasiektas ir palaikomas ≥ 50 000 / μl trombocitų skaičius, būtinas kraujavimo rizikai sumažinti. Negalima viršyti 75 mg paros dozės.
Gydant eltrombopagu, reikia reguliariai tikrinti kraujo chemiją ir kepenų funkcijos rodiklius, o eltrombopago dozavimo režimą koreguoti atsižvelgiant į trombocitų skaičių, kaip nurodyta 1 lentelėje. Gydymo eltrombopagu metu reikia kas savaitę tirti visą kraujo kiekį, įskaitant trombocitų skaičių ir periferinį kraujo tepinėlis, kol bus pasiektas stabilus trombocitų skaičius (≥ 50 000 / μl mažiausiai 4 savaites).
Vėliau kas mėnesį reikia atlikti išsamų kraujo tyrimą, įskaitant trombocitų skaičių ir periferinio kraujo tepinėlį.
1 lentelė Eltrombopago dozės keitimas ITP sergantiems pacientams
* - Pacientams, vartojantiems 25 mg eltrombopago kartą per dvi dienas, dozę padidinkite iki 25 mg vieną kartą per parą.
? - Pacientams, vartojantiems 25 mg eltrombopago vieną kartą per parą, reikia apsvarstyti 12,5 mg dozę vieną kartą per parą arba 25 mg dozę kartą per dvi dienas.
Eltrombopagą galima vartoti kartu su kitais ITP vaistais. Kartu vartojamų vaistų, skirtų ITP gydyti, dozavimo režimą reikia keisti, jei tai kliniškai tinkama, kad išvengtumėte per didelio trombocitų skaičiaus padidėjimo gydymo eltrombopagu metu.
Prieš svarstant kitą dozės koregavimą, reikia palaukti mažiausiai 2 savaites, kad pamatytumėte bet kokių dozės pakeitimų poveikį paciento trombocitų atsakui.
Standartinė eltrombopago dozės keitimas mažinant arba didinant turi būti 25 mg vieną kartą per parą.
Gydymo nutraukimas
Gydymą eltrombopagu reikia nutraukti, jei trombocitų skaičius nepadidėja iki tokio lygio, kad būtų išvengta kliniškai svarbaus kraujavimo po keturių gydymo savaičių 75 mg eltrombopago kartą per parą gydymo.
Pacientai turi būti periodiškai ištirti, o dėl tolesnio gydymo gydytojas turi nuspręsti individualiai. Pacientams, kuriems nebuvo atlikta blužnies pašalinimas, tai turėtų apimti splenektomijos įvertinimą. Nutraukus gydymą, trombocitopenija gali pasikartoti (žr. 4.4 skyrių).
Trombocitopenija, susijusi su lėtiniu HCV hepatitu
Kai eltrombopagas skiriamas kartu su antivirusiniais vaistais, reikia perskaityti atitinkamų kartu vartojamų vaistinių preparatų charakteristikų santrauką, kurioje pateikiama išsami informacija apie saugumą ir kontraindikacijas.
Klinikinių tyrimų metu trombocitų skaičius paprastai pradėjo didėti per 1 savaitę nuo eltrombopago pradžios. Gydymo eltrombopagu tikslas turėtų būti pasiekti minimalų trombocitų skaičių, būtiną antivirusiniam gydymui pradėti, laikantis klinikinės praktikos rekomendacijų. gydymo tikslas turėtų būti palaikyti tokį trombocitų skaičių, kuris apsaugo nuo kraujavimo komplikacijų rizikos, paprastai apie 50 000–75 000 / μl. Reikia vengti trombocitų skaičiaus> 75 000 / μl. Turi būti naudojama mažiausia eltrombopago dozė, reikalinga tikslams pasiekti Dozės keitimas grindžiamas trombocitų skaičiaus atsaku.
Pradinė dozavimo schema
Eltrombopagą reikia pradėti gydyti 25 mg doze vieną kartą per parą. Pacientams, sergantiems lėtiniu Rytų Azijos hepatito HCV hepatitu ar lengvu kepenų funkcijos sutrikimu, dozės keisti nereikia (žr. 5.2 skyrių).
Dozės stebėjimas ir keitimas
Eltrombopago dozę reikia keisti po 25 mg kas 2 savaites, kad būtų pasiektas tikslinis trombocitų skaičius, būtinas antivirusiniam gydymui pradėti. Prieš pradedant antivirusinį gydymą, trombocitų skaičių reikia tikrinti kas savaitę. Pradėjus antivirusinį gydymą, trombocitų skaičius gali sumažėti, todėl reikia vengti nedelsiant keisti eltrombopago dozę (žr. 2 lentelę).
Antivirusinio gydymo metu eltrombopago dozę reikia keisti, kad būtų išvengta peginterferono dozės mažinimo dėl trombocitų skaičiaus sumažėjimo, dėl kurio pacientas gali patirti kraujavimą (žr. 2 lentelę). Antivirusinio gydymo metu trombocitų skaičius turi būti stebimas kas savaitę, kol bus pasiektas stabilus trombocitų skaičius, paprastai apie 50 000–75 000 / mikrolitras. Vėliau kas mėnesį reikia atlikti išsamų kraujo tyrimą, įskaitant trombocitų skaičių ir periferinio kraujo tepinėlį. Jei trombocitų skaičius viršija reikalaujamą tikslą, reikia apsvarstyti galimybę sumažinti 25 mg paros dozę. Patartina palaukti 2 savaites, kol bus įvertintas šio ir bet kurio tolesnio dozės koregavimo poveikis.
Negalima viršyti 100 mg eltrombopago dozės vieną kartą per parą.
2 lentelė Eltrombopago dozės keitimas lėtiniu HCV hepatitu sergantiems pacientams antivirusinio gydymo metu
* - Pacientams, vartojantiems 25 mg eltrombopago vieną kartą per parą, reikia apsvarstyti galimybę atnaujinti gydymą 25 mg kas antrą dieną.
? - Pradėjus antivirusinį gydymą, trombocitų skaičius gali sumažėti, todėl reikia vengti nedelsiant mažinti eltrombopago dozę.
Gydymo nutraukimas
Gydymą eltrombopagu reikia nutraukti, jei po 2 savaičių gydymo 100 mg trombocitų skaičiaus, reikalingo antivirusiniam gydymui pradėti, nepasiekta.
Jei nenurodyta kitaip, gydymą eltrombopagu reikia nutraukti nutraukus antivirusinį gydymą. Dėl per didelio trombocitų skaičiaus atsako ar didelių kepenų funkcijos tyrimų sutrikimų taip pat reikia nutraukti gydymą.
Sunki aplastinė anemija
Pradinis dozavimo režimas
Gydymą eltrombopagu reikia pradėti nuo 50 mg dozės vieną kartą per parą. Rytų Azijos pacientams gydyti eltrombopagu reikia pradėti mažesne 25 mg doze vieną kartą per parą (žr. 5.2 skyrių). Gydymo negalima pradėti, kai pacientai jau turi 7 chromosomos citogenetinių sutrikimų.
Dozės stebėjimas ir keitimas
Dėl hematologinio atsako reikia titruoti dozę, paprastai iki 150 mg, ir tai gali užtrukti iki 16 savaičių nuo gydymo eltrombopagu pradžios (žr. 5.1 skyrių). Norint pasiekti tikslą, eltrombopago dozę reikia keisti kas 50 mg. trombocitų skaičius ≥ 50 000 / μl. Pacientams, vartojantiems 25 mg vieną kartą per parą, dozę reikia padidinti iki 50 mg per parą prieš didinant 50 mg. Ji neturėtų būti viršyta. 150 mg per parą dozė Klinikiniai hematologiniai ir kepenų tyrimai stebimas gydymo eltrombopagu ir modifikuoto eltrombopago dozavimo režimo, atsižvelgiant į trombocitų skaičių, kaip nurodyta 3 lentelėje.
3 lentelė Eltrombopago dozės keitimas pacientams, sergantiems sunkia aplastine anemija
Sumažėjimas pacientams, kuriems trilinearinis atsakas (baltųjų kraujo kūnelių, raudonųjų kraujo kūnelių ir trombocitų)
Pacientams, kurie pasiekia trilinearinį atsaką, įskaitant nepriklausomą nuo perpylimo, trunkantį mažiausiai 8 savaites: eltrombopago dozę galima sumažinti 50%.
Jei vartojant sumažintą dozę kraujo kiekis išlieka stabilus po 8 savaičių, eltrombopago vartojimą reikia nutraukti ir stebėti kraujo skaičių. Jei trombocitų skaičius nukristų nuo hemoglobino lygio iki neutrofilų lygio iki lygio
Pertraukimas
Jei po 16 gydymo eltrombopago savaičių hematologinio atsako nepasireiškė, gydymą reikia nutraukti. Jei nustatomi nauji citogenetiniai sutrikimai, reikia apsvarstyti, ar tinkamas tęsti gydymą eltrombopagu (žr. 4.4 ir 4.8 skyrius). Dėl per didelio trombocitų skaičiaus atsako (kaip nurodyta 3 lentelėje) arba dėl didelių kepenų tyrimų rodmenų pakitimų taip pat reikia nutraukti eltrombopago vartojimą (žr. 4.8 skyrių).
Specialios populiacijos
Inkstų nepakankamumas
Pacientams, sergantiems inkstų nepakankamumu, dozės koreguoti nereikia. Pacientams, kurių inkstų funkcija sutrikusi, eltrombopagą reikia vartoti atsargiai ir atidžiai prižiūrint, pavyzdžiui, atliekant kreatinino koncentraciją serume ir (arba) šlapimą (žr. 5.2 skyrių).
Kepenų nepakankamumas
Eltrombopago negalima vartoti ITP sergantiems pacientams, sergantiems kepenų nepakankamumu (Child-Pugh rodiklis ≥ 5), nebent laukiama nauda yra didesnė už nustatytą vartų venų trombozės riziką (žr. 4.4 skyrių).
Jei ITP sergantiems pacientams, sergantiems kepenų nepakankamumu, eltrombopagą vartoti būtina, pradinė dozė turi būti 25 mg vieną kartą per parą. Pradėjus eltrombopago dozę pacientams, sergantiems kepenų nepakankamumu, reikia laikytis dozės. 3 savaičių intervalas prieš didinant dozę .
Trombocitopenija sergantiems pacientams, sergantiems lėtiniu HCV hepatitu ir lengvu kepenų nepakankamumu (Child-Pugh rodiklis ≤ 6), dozės koreguoti nereikia. Pacientams, sergantiems lėtiniu HCV hepatitu ir sunkia aplastine anemija, pasireiškiančia kepenų nepakankamumu, eltrombopagą reikia pradėti gydyti 25 mg doze vieną kartą per parą (žr. 5.2 skyrių). Pradėjus gydyti eltrombopagu pacientams, sergantiems kepenų nepakankamumu, prieš didinant dozę, reikia laikytis 2 savaičių pertraukos.
Padidėjusi nepageidaujamų reiškinių, įskaitant kepenų dekompensaciją ir tromboembolinius reiškinius, rizika pacientams, sergantiems trombocitopenija, sergantiems pažengusia lėtine kepenų liga, gydoma eltrombopagu, ruošiantis invazinėms procedūroms, arba pacientams, sergantiems lėtiniu HCV hepatitu, gydomiems antivirusiniais vaistais (žr. 4.8).
Vyresnio amžiaus piliečiai
Duomenų apie eltrombopago vartojimą 65 metų ir vyresniems ITP sergantiems pacientams yra nedaug, o klinikinės patirties pacientams, sergantiems ITP, vyresniems nei 85 metų, nėra. Klinikinių eltrombopago tyrimų metu klinikinių skirtumų nepastebėta. Reikšmingas eltrombopago saugumas tarp ne jaunesniems kaip 65 metų asmenims. Kituose klinikiniuose tyrimuose nenustatyta vyresnio amžiaus ir jaunesnių pacientų atsakų skirtumų, tačiau negalima atmesti didesnio kai kurių vyresnio amžiaus asmenų jautrumo (žr. 5.2 skyrių).
Duomenų apie eltrombopago vartojimą pacientams, sergantiems lėtiniu HCV hepatitu ir AAS, vyresniems nei 75 metų, yra nedaug. Šiems pacientams reikia būti atsargiems (žr. 4.4 skyrių).
Rytų Azijos pacientai
Pacientams, kilusiems iš Rytų Azijos (pvz., Kinų, japonų, taivaniečių, korėjiečių ar tajų), įskaitant pacientus, kurių kepenų funkcija sutrikusi, eltrombopagą reikia pradėti gydyti 25 mg doze vieną kartą per parą (žr. 5.2 skyrių).
Reikia toliau stebėti paciento trombocitų skaičių ir laikytis standartinių tolesnio dozės keitimo kriterijų.
Vaikų populiacija
Revolade nerekomenduojama vartoti jaunesniems nei 1 metų vaikams, sergantiems lėtine ITP, nes nepakanka duomenų apie saugumą ir veiksmingumą. Eltrombopago saugumas ir veiksmingumas vaikams ir paaugliams (
Vartojimo metodas
Vartoti per burną.
Tabletes reikia gerti mažiausiai dvi valandas prieš arba keturias valandas po bet kokio produkto, pvz., Antacidinių vaistų, pieno produktų (ar kitų maisto produktų, kurių sudėtyje yra kalcio), arba mineralinių papildų, kurių sudėtyje yra daugiasluoksnių katijonų (pvz., Geležies, kalcio, magnio, aliuminio, seleno ir cinko). ) (žr. 4.5 ir 5.2 skyrius).
04.3 Kontraindikacijos
Padidėjęs jautrumas eltrombopagui arba bet kuriai 6.1 skyriuje nurodytai pagalbinei medžiagai.
04.4 Specialūs įspėjimai ir tinkamos atsargumo priemonės
Padidėjusi nepageidaujamų reakcijų, įskaitant gyvybei pavojingą kepenų dekompensaciją ir tromboembolinius reiškinius, rizika pacientams, sergantiems trombocitopeniniu lėtiniu hepatitu HCV, sergantiems pažengusia lėtine kepenų liga, kurią lemia mažas ≤ 35 g / l albuminas arba pagal balų modelį. Liga (MELD) ≥ 10, kai gydoma eltrombopagu kartu su gydymu interferonu. Be to, gydymo nauda, palyginti su pacientų, pasiekusių ilgalaikį virusologinį atsaką (SVR), santykiu, palyginti su placebu, buvo nedidelė šiems pacientams (ypač tiems, kurių pradinis albuminas ≤ 35 g / l), palyginti su visa grupe. Šiems pacientams eltrombopagą pradėti gali tik gydytojai, turintys pažengusio lėtinio HCV hepatito gydymo patirties, ir tik tada, kai reikia įsikišti dėl trombocitopenijos rizikos arba nutraukti antivirusinį gydymą. Jei manoma, kad gydymas yra kliniškai pagrįstas, būtina atidžiai stebėti šiuos pacientus.
Derinys su tiesioginio veikimo antivirusiniais vaistais
Saugumas ir veiksmingumas nebuvo nustatytas kartu su tiesioginio veikimo antivirusiniais vaistais, patvirtintais lėtiniam HCV hepatitui gydyti.
Kepenų toksiškumo rizika
Vartojant eltrombopagą, gali sutrikti kepenų veikla ir pasireikšti sunkus toksinis poveikis kepenims, o tai gali būti pavojinga gyvybei. Kontroliuojamuose klinikiniuose eltrombopago tyrimuose su lėtiniu ITP buvo pastebėtas alanino aminotransferazės (ALT), aspartato aminotransferazės (AST) ir bilirubino koncentracijos serume padidėjimas (žr. 4.8 skyrių).
Šie pokyčiai dažniausiai buvo lengvi (1–2 laipsnio), grįžtami ir nebuvo lydimi kliniškai reikšmingų simptomų, kurie būtų rodę „kepenų funkcijos sutrikimą“. ir 1 eltrombopago grupės pacientui buvo nustatytas 4 laipsnio kepenų funkcijos rodiklių sutrikimas. Dviejuose placebu kontroliuojamuose tyrimuose, kuriuose dalyvavo vaikai (nuo 1 iki 17 metų), sergantys lėtiniu ITP, ALT reikšmė ≥ 3 kartus viršijo viršutinę normos ribą ( x VNR) buvo pastebėtas atitinkamai 4,7% ir 0% eltrombopago ir placebo grupių.
Dviejuose kontroliuojamuose klinikiniuose tyrimuose, kuriuose dalyvavo pacientai, sergantys lėtiniu HCV hepatitu, ALT arba AST ≥ 3 kartus viršijo viršutinę normos ribą (VNR), atitinkamai 34% ir 38% eltrombopago ir placebo grupių. Daugumai pacientų, kurie buvo gydyti eltrombopagu kartu su peginterferonu / ribavirinu, pasireikš netiesioginė hiperbilirubinemija. Apskritai, bendras bilirubino kiekis, ≥ 1,5 karto viršijantis VNR, buvo nustatytas atitinkamai 76% ir 50% eltrombopago ir placebo grupėse.
Prieš pradedant gydyti eltrombopagu, kas 2 savaites dozės koregavimo fazėje ir kas mėnesį, kai pasiekiama stabili dozė, reikia išmatuoti ALT, AST ir bilirubino koncentraciją serume.
Eltrombopagas slopina UDP gliukozilo transferazę (UGT) 1A1 ir organinį anijonų transporterio polipeptidą (OATP) 1B1, o tai gali sukelti netiesioginę hiperbilirubinemiją. Padidėjus bilirubino kiekiui, reikia atlikti frakcionavimą. Serumo kepenų funkcijos tyrimų sutrikimai turi būti įvertinti pakartotinai tiriant 3-5 dienos Jei patvirtinami nukrypimai, reikia stebėti kepenų funkcijos tyrimus serume, kol sutrikimai išnyks, stabilizuosis arba grįš į pradinį lygį.
Eltrombopago vartojimą reikia nutraukti, jei ALT koncentracija padidėja (≥ 3 kartus viršija viršutinę normos ribą pacientams, kurių kepenų funkcija normali, arba ≥ 3 kartus didesnė už pradinę vertę arba> 5 kartus viršija viršutinę normos ribą, atsižvelgiant į tai, kas yra mažesnė, pacientams, kuriems prieš gydymą padidėja transaminazių kiekis) ir yra:
- progresyvus, arba
- išlieka ≥ 4 savaites, arba
- kartu yra padidėjęs tiesioginis bilirubino kiekis, arba
- kartu yra klinikinių kepenų pažeidimo simptomų arba kepenų dekompensacijos požymių.
Pacientams, sergantiems kepenų liga, eltrombopagą reikia skirti atsargiai. Pacientams, sergantiems ITP ir SAA, reikia skirti mažesnę pradinę eltrombopago dozę. Vartojant pacientus, kuriems yra kepenų nepakankamumas, reikia atidžiai stebėti (žr. 4.2 skyrių).
Kepenų nepakankamumas (vartojamas kartu su interferonu)
Kepenų dekompensacija sergantiems lėtiniu HCV hepatitu
Pacientams, sergantiems lėtiniu HCV hepatitu ir ciroze, gydant alfa interferonu, gali kilti kepenų dekompensacijos rizika. Dviejuose kontroliuojamuose klinikiniuose tyrimuose, kuriuose dalyvavo trombocitopenija sergantys pacientai, sergantys lėtiniu HCV hepatitu, kepenų dekompensacija (ascitas, kepenų encefalopatija, varikozinis kraujavimas, savaiminis bakterinis peritonitas) eltrombopago grupėje (11%) pasireiškė dažniau nei placebo grupėje (6%). Pacientams, kurių pradinis albumino kiekis (≤ 35 g / l) arba MELD balas buvo ≥ 10, buvo trigubai didesnė kepenų dekompensacijos rizika ir didesnė mirtinų nepageidaujamų reiškinių rizika, palyginti su pacientais, kurių kepenų liga yra mažiau pažengusi. Be to, gydymo nauda, palyginti su SVR pasiekimo rodikliu, palyginti su placebu, buvo nedidelė šiems pacientams (ypač tiems, kurių pradinis albuminas ≤ 35 g / l), palyginti su visa grupe. Eltrombopagą šiems pacientams galima skirti tik gerai įvertinus laukiamą naudą ir riziką. Pacientus, kuriems būdingos šios savybės, reikia atidžiai stebėti, ar neatsiranda kepenų dekompensacijos požymių ir simptomų. Nutraukimo kriterijus reikia nurodyti atitinkamoje interferono preparato charakteristikų santraukoje. Eltrombopago vartojimą reikia nutraukti, jei antivirusinis gydymas nutraukiamas dėl kepenų dekompensacijos.
Trombozinės / tromboembolinės komplikacijos
Kontroliuojamų klinikinių tyrimų, kuriuose dalyvavo trombocitopenija sergantys pacientai, sergantys lėtiniu HCV hepatitu, gydomi interferonu (n = 1439), 38 iš 955 (4%) tiriamųjų, gydytų eltrombopagu, ir 6 iš 484 (1%) tiriamųjų placebo grupėje parodė tromboembolinius reiškinius. (TEE). Pranešimuose apie trombozines / tromboembolines komplikacijas buvo ir venų, ir arterijų. Dauguma TEE buvo nerimtos ir iki tyrimo pabaigos išsprendė. Portalo venų trombozė buvo dažniausia TEE abiejose gydymo grupėse (2% eltrombopagu gydytų pacientų, palyginti su TEE požymiais ir simptomais).
TEE rizika padidėjo pacientams, sergantiems lėtine kepenų liga (lėtinė kepenų liga, CLD), gydomas 75 mg eltrombopago vieną kartą per parą dvi savaites, ruošiantis invazinėms procedūroms.
Šeši iš 143 (4%) suaugusių pacientų, sergančių CLD, vartoję eltrombopagą, patyrė TEE (visi susiję su portalo venų sistema), o du iš 145 tiriamųjų (1%) placebo grupėje patyrė TEE (vienas susijęs su portalo venų sistema ir miokardo infarktu). . Penki iš 6 pacientų, gydytų eltrombopagu, patyrė trombozinių komplikacijų, kai trombocitų skaičius> 200 000 / mikrolitras, ir per 30 dienų nuo paskutinės eltrombopago dozės. .
Klinikinių eltrombopago ITP tyrimų metu buvo nustatyti tromboemboliniai reiškiniai, kai trombocitų skaičius buvo mažas ir normalus. Eltrombopagą reikia skirti atsargiai pacientams, kuriems yra žinomi tromboembolijos rizikos veiksniai, įskaitant, bet tuo neapsiribojant, paveldimus (pvz., Leideno faktorius) ar įgytus (pvz., ATIII trūkumas, antifosfolipidinis sindromas) rizikos veiksnius, vyresnį amžių, pacientus, kurių imobilizacija užsitęsusi. , piktybiniai navikai, kontracepcija ar pakaitinė hormonų terapija, operacija / trauma, nutukimas ir rūkymas. Trombocitų skaičių reikia atidžiai stebėti ir, jei trombocitų skaičius viršija reikalaujamą lygį, sumažinti dozę arba nutraukti eltrombopago vartojimą (žr. 4.2 skyrių). Pacientams, kuriems yra bet kokios etiologijos TEE reiškinių rizika, reikia atsižvelgti į naudos ir rizikos santykį.
Eltrombopago negalima vartoti ITP sergantiems pacientams, sergantiems kepenų nepakankamumu (Child-Pugh rodiklis ≥ 5), nebent laukiama nauda yra didesnė už nustatytą vartų venų trombozės riziką. Kai gydymas laikomas tinkamu, eltrombopagą reikia skirti atsargiai pacientams, kurių kepenų funkcija sutrikusi (žr. 4.2 ir 4.8 skyrius).
Kraujavimas nutraukus eltrombopago vartojimą
Nutraukus gydymą eltrombopagu, trombocitopenija gali atsinaujinti. Nutraukus eltrombopago vartojimą, trombocitų skaičius daugumoje pacientų per 2 savaites grįžta į pradinę vertę, o tai padidina kraujavimo riziką ir kai kuriais atvejais gali sukelti kraujavimą. Ši rizika padidėja, jei gydymas eltrombopagu nutraukiamas, kai yra antikoaguliantų ir nutraukus gydymą eltrombopagu, rekomenduojama atnaujinti ITP gydymą pagal galiojančias gaires. Be to, medicininis gydymas gali apimti antikoaguliantų ir (arba) antikoaguliacinio gydymo nutraukimą. nutraukus eltrombopago vartojimą, jų skaičius turi būti stebimas kas savaitę 4 savaites.
Klinikinių lėtinio HCV hepatito tyrimų metu buvo pranešta apie didesnį kraujavimą iš skrandžio, įskaitant sunkius ir mirtinus atvejus, nutraukus peginterferono, ribavirino ir eltrombopago vartojimą.
Nutraukus gydymą, pacientus reikia stebėti, ar neatsirado kraujavimo iš skrandžio požymių ar simptomų.
Kaulų čiulpų retikulino susidarymas ir kaulų čiulpų fibrozės rizika Eltrombopagas gali padidinti retikulino skaidulų vystymosi ar progresavimo kaulų čiulpuose riziką.
Prieš pradedant gydyti eltrombopagu, reikia atidžiai ištirti periferinio kraujo tepinėlį, kad būtų nustatytas pradinis ląstelių morfologinių sutrikimų lygis. Nustačius stabilią eltrombopago dozę, kas mėnesį reikia atlikti išsamų kraujo tyrimą ir diferencijuotą baltųjų kraujo kūnelių skaičių. Jei pastebimos nesubrendusios ar displazinės ląstelės, reikia ištirti periferinio kraujo tepinėlį, ar nėra naujų morfologinių sutrikimų (pvz., Ašarinių raudonųjų kraujo kūnelių) (dakriocitų) ir branduolių, nesubrendusių baltųjų kraujo kūnelių) arba pablogėja ar citopenija. Jei pacientui atsiranda naujų ar pablogėja morfologinių sutrikimų ar citopenija, gydymą eltrombopagu reikia nutraukti ir imtis. Apsvarstykite kaulų čiulpų biopsiją, įskaitant fibrozės įvertinimą.
Esamo mielodisplastinio sindromo (MDS) progresavimas
TPO-R agonistai yra augimo faktoriai, skatinantys trombopoetinių kamieninių ląstelių dauginimąsi ir diferenciaciją bei trombocitų gamybą. TPO-R daugiausia ekspresuojamas mieloidinių linijų ląstelių paviršiuje. TPO-R agonistų atveju yra rizika, kad jie gali paskatinti jau esančių neoplastinių hemopatijų, tokių kaip mielodisplastinis sindromas, progresavimą.
Klinikinių tyrimų su TPO-R agonistu metu pacientams, sergantiems MDS, buvo pastebėta trumpalaikio blastinių ląstelių skaičiaus padidėjimo atvejų ir pranešta apie ligos progresavimo iš MDS iki ūminės mieloidinės leukemijos (AML) atvejus.
Suaugusiems ir senyviems pacientams ITP arba SAA diagnozė turi būti patvirtinta, neįtraukiant kitų patologijų, kurioms būdingas trombocitopenija, ypač MDS diagnozė. Ligos ir gydymo metu reikia atsižvelgti į kaulų čiulpų aspiraciją ir biopsiją, ypač vyresniems nei 60 metų pacientams, turintiems sisteminių simptomų ar nenormalių požymių, pvz., Padidėjusių periferinių sprogimo ląstelių.
Eltrombopago veiksmingumas ir saugumas nenustatytas esant kitoms trombocitopeninėms ligoms, įskaitant chemoterapijos sukeltą trombocitopeniją ar MDS.
Eltrombopago negalima naudoti ne klinikinių tyrimų metu, siekiant gydyti trombocitopeniją, kurią sukelia MDS ar kitos trombocitopenijos priežastys, išskyrus patvirtintas indikacijas.
Citogenetiniai sutrikimai ir MDS / AML progresavimas pacientams, sergantiems AAS
Yra žinoma, kad pacientams, sergantiems AAS, išsivysto citogenetiniai sutrikimai. Nežinoma, ar eltrombopagas padidina citogenetinių sutrikimų riziką pacientams, sergantiems AAS. II fazės klinikinio tyrimo metu, kai AAS buvo naudojamas eltrombopagas, naujų citogenetinių anomalijų dažnis buvo pastebėtas 19% pacientų [8/43 (iš kurių 5 turėjo 7 chromosomos sutrikimų)]. Tyrimo metu vidutinis citogenetinių anomalijų atsiradimo laikas buvo 2,9 mėnesio.
Klinikinių tyrimų su eltrombopagu gydant ASS metu 4% pacientų (5/133) buvo diagnozuota MDS. Vidutinis laikas iki diagnozės nustatymo nuo gydymo eltrombopagu pradžios buvo trys mėnesiai.
Pacientams, kuriems yra atsparus ugniai ar stipriai išgydytas SAS ir kuriems anksčiau buvo taikomas imunosupresinis gydymas, prieš pradedant eltrombopagą, 3 gydymo mėnesius ir vėliau kas 6 mėnesius rekomenduojama ištirti kaulų čiulpų aspiraciją dėl citogenetikos. Jei aptinkama naujų. Citogenetinių sutrikimų, reikia apsvarstyti, ar tikslinga tęsti eltrombopago vartojimą.
Akių pakitimai
Katarakta pastebėta atliekant eltrombopago toksikologinius tyrimus su graužikais (žr. 5.3 skyrių). Kontroliuojamų klinikinių tyrimų, kuriuose dalyvavo trombocitopenija sergantys pacientai, sergantys lėtiniu HCV hepatitu, gydomi interferonu (n = 1439), buvusios pradinės kataraktos progresavimas arba naujos kataraktos atsiradimas pasireiškė 8% grupės pacientų. Eltrombopagas ir 5% Buvo pranešta apie tinklainės kraujavimą, dažniausiai 1 ar 2 laipsnio, pacientams, sergantiems lėtiniu HCV hepatitu, vartojantiems interferoną, ribaviriną ir eltrombopagą (2% eltrombopago grupės ir 2% placebo grupėje). Kraujavimai atsirado ant tinklainė (preretinalinė), po tinklaine (subretinal) arba tinklainės audiniuose. Rekomenduojama reguliariai stebėti pacientus oftalmologiškai.
QT / QTc plėtinys
QTc tyrimas su sveikais savanoriais, skiriant 150 mg eltrombopago paros dozę, kliniškai reikšmingo poveikio širdies repolarizacijai neparodė. Pranešta apie QTc intervalo pailgėjimą klinikinių tyrimų metu, kuriuose dalyvavo ITP pacientai ir trombocitopenija sergantys pacientai, sergantys lėtiniu HCV hepatitu. Šių QTc pailgėjimo atvejų klinikinė reikšmė nežinoma.
Atsakymo į eltrombopagą praradimas
Atsakymo praradimas arba trombocitų atsako palaikymas gydant eltrombopagu neviršijant rekomenduojamo terapinio intervalo, turėtų paskatinti ieškoti priežastinių veiksnių, įskaitant kaulų čiulpų retikulino kiekio padidėjimą.
Vaikų populiacija
Pirmiau minėti ITP įspėjimai ir atsargumo priemonės taip pat taikomi vaikų populiacijai.
04.5 Sąveika su kitais vaistiniais preparatais ir kitos sąveikos formos
Eltrombopago poveikis kitiems vaistiniams preparatams
HMG CoA reduktazės inhibitoriai
Švietimas in vitro parodė, kad eltrombopagas nėra organinio anijonų pernešėjo polipeptido OATP1B1 substratas, bet yra šio transporterio inhibitorius. Švietimas in vitro taip pat parodė, kad eltrombopagas yra atsparumo krūties vėžiui baltymo (BCRP) substratas ir inhibitorius. 39 sveikiems suaugusiems tiriamiesiems po 75 mg eltrombopago vieną kartą per parą 5 dienas su viena 10 mg rozuvastatino doze, OATP1B1 ir BCRP substratu, rozuvastatino C plazma padidėjo 103% (90% patikimumo intervalas [PI]: 82 %, 126%) ir AUC0-? 55% (90% PI: 42%, 69%). Taip pat tikėtina sąveika su kitais HMG-CoA reduktazės inhibitoriais, įskaitant atorvastatiną, fluvastatiną, lovastatiną, pravastatiną ir simvastatiną. Vartojant kartu su eltrombopagu, reikia apsvarstyti galimybę sumažinti statinų dozę ir atidžiai stebėti, ar neatsiranda nepageidaujamų reakcijų į statinus (žr. 5.2 skyrių).
OATP1B1 ir BCRP substratai
Eltrombopagą kartu su OATP1B1 substratais (pvz., Metotreksatu) ir BCRP (pvz., Topotekanu ir metotreksatu) reikia vartoti atsargiai (žr. 5.2 skyrių).
Citochromo P450 substratai
Tiriant žmogaus kepenų mikrosomas, eltrombopagas (iki 100 mcM) neslopino. in vitro CYP450 fermentų 1A2, 2A6, 2C19, 2D6, 2E1, 3A4 / 5 ir 4A9 / 11 ir buvo CYP2C8 ir CYP2C9 inhibitorius, išmatuotas naudojant paklitakselį ir diklofenaką kaip zondo substratus. Vartojant 75 mg eltrombopago vieną kartą per parą 7 dienas 24 sveikiems vyrams neslopino ir nesukėlė 1A2 (kofeino), 2C19 (omeprazolo), 2C9 (flurbiprofeno) ar 3A4 (midazolamo) substratų metabolizmo žmogaus organizme. Skiriant eltrombopagą ir CYP450 substratus, kliniškai reikšmingos sąveikos nesitikima (žr. 5.2 skyrių).
HCV proteazės inhibitoriai
Eltrombopagą vartojant kartu su telapreviru arba bocepreviru, dozės keisti nereikia.
Kartu vartojant vieną 200 mg eltrombopago dozę ir 750 mg telapreviro kas 8 valandas, telapreviro ekspozicija plazmoje nepasikeitė.
Kartu vartojant vieną 200 mg eltrombopago dozę ir 800 mg bocepreviro kas 8 valandas, bocepreviro AUC (0-?) Plazmoje nepasikeitė, tačiau C padidėjo 20%, o C sumažėjo 32%. Klinikinė reikšmė Cmin sumažėjimas nenustatytas: norint atidžiau slopinti HCV, rekomenduojama atidžiau stebėti klinikinius ir laboratorinius tyrimus.
Kitų vaistinių preparatų poveikis eltrombopagui
Ciklosporinas
Tyrimai in vitro parodė, kad eltrombopagas yra BCRP substratas ir inhibitorius. Pastebėta, kad eltrombopago ekspozicija sumažėja, kai kartu vartojama 200 mg ir 600 mg ciklosporino (BCRP inhibitorius) (žr. 5.2 skyrių). Gydymo metu eltrombopago dozę galima keisti atsižvelgiant į paciento trombocitų skaičių (žr. 4.2 skyrių). Trombocitų skaičius turi būti stebimas bent kartą per savaitę 2–3 savaites, kai eltrombopagas vartojamas kartu su ciklosporinu. Remiantis trombocitų skaičiaus rezultatais, gali reikėti padidinti eltrombopago dozę.
Daugiavalenčiai katijonai (chelatai)
Eltrombopagas chelatina polivalentinius katijonus, tokius kaip geležis, kalcis, magnis, aliuminis, selenas ir cinkas. Pavartojus vieną 75 mg eltrombopago dozę kartu su antacidiniais vaistais, turinčiais daugiavalentį katijoną (1524 mg aliuminio hidroksido ir 1425 mg magnio karbonato), sumažėja AUC0-? plazmos eltrombopago iki 70% (90% PI: 64%, 76%) ir Cmax iki 70% (90% PI: 62%, 76%).
Eltrombopagą reikia gerti mažiausiai 2 valandas prieš arba 4 valandas po bet kurio antacidinio tipo produkto, pieno produkto ar mineralinio papildo, kuriame yra daugiakomponentių katijonų, kad būtų išvengta reikšmingo eltrombopago absorbcijos sumažėjimo dėl chelacijos (žr. 4.2 ir 5.2 skyrius).
Sąveika su maistu
Eltrombopago tablečių ar geriamosios suspensijos miltelių vartojimas kartu su maistu, kuriame yra daug kalcio (pvz., Valgio, kuriame buvo pieno produktų), žymiai sumažino AUC0-? ir eltrombopago Cmax plazmoje. Priešingai, eltrombopago vartojimas 2 valandas prieš valgį arba 4 valandos po valgio, kuriame yra daug kalcio ar mažai kalcio.
Lopinaviras / ritonaviras
Eltrombopagą vartojant kartu su lopinaviru / ritonaviru, gali sumažėti eltrombopago koncentracija. Tyrimas, kuriame dalyvavo 40 sveikų savanorių, parodė, kad skiriant vieną 100 mg eltrombopago dozę ir kartotinę 400/100 mg lopinaviro / ritonaviro dozę du kartus per parą, eltrombopago AUC (0-?) Sumažėjo 17% (90 %PI: 6,6%; 26,6%). Todėl reikia atsargiai skirti eltrombopagą kartu su lopinaviru / ritonaviru. Trombocitų skaičius turi būti atidžiai stebimas, kad būtų užtikrintas tinkamas klinikinis eltrombopago dozės valdymas, kai gydymas lopinaviru / ritonaviru pradedamas arba nutraukiamas.
CYP1A2 ir CYP2C8 inhibitoriai ir induktoriai
Eltrombopagas metabolizuojamas keliais būdais, įskaitant CYP1A2, CYP2C8, UGT1A1 ir UGT1A3 (žr. 5.2 skyrių). Mažai tikėtina, kad vaistiniai preparatai, kurie slopina arba indukuoja vieną fermentą, reikšmingai paveiks eltrombopago koncentraciją plazmoje; tuo tarpu vaistai, kurie slopina arba indukuoja kelis fermentus, gali padidinti (pvz., Fluvoksamino) arba sumažinti (pvz., Rifampicino) eltrombopago koncentraciją.
HCV proteazės inhibitoriai
Vaistų sąveikos farmakokinetikos tyrimo rezultatai rodo, kad kartotinė 800 mg bocepreviro dozė kas 8 valandas arba 750 mg telapreviro dozė kas 8 valandas su vienkartine 200 mg eltrombopago doze nepakito eltrombopago ekspozicijai plazmoje. kliniškai reikšmingo lygio.
Vaistai ITP gydymui
Klinikinių tyrimų metu gydant ITP kartu su eltrombopagu buvo naudojami kortikosteroidai, danazolas ir (arba) azatioprinas, intraveninis imunoglobulinas (IVIG) ir anti-D imunoglobulinas. Trombocitų skaičių reikia stebėti skiriant eltrombopagą kartu su kitais vaistiniais preparatais ITP gydyti, kad trombocitų skaičius neviršytų rekomenduojamos ribos (žr. 4.2 skyrių).
04.6 Nėštumas ir žindymo laikotarpis
Nėštumas
Duomenų apie eltrombopago vartojimą nėščioms moterims nėra arba yra nedaug .. Tyrimai su gyvūnais parodė toksinį poveikį reprodukcijai (žr. 5.3 skyrių). Galima rizika žmonėms nežinoma.
Nėštumo metu Revolade nerekomenduojama.
Vaisingo amžiaus moterys / Kontracepcija vyrams ir moterims
Revolade nerekomenduojama vaisingoms moterims, kurios nenaudoja kontraceptikų.
Maitinimo laikas
Nežinoma, ar eltrombopagas / jo metabolitai išsiskiria į motinos pieną. Tyrimai su gyvūnais parodė, kad eltrombopagas tikriausiai patenka į pieną (žr. 5.3 skyrių); todėl negalima atmesti rizikos slaugančiam kūdikiui. Reikia nuspręsti, ar nutraukti maitinimą krūtimi, ar tęsti / susilaikyti nuo gydymo Revolade, įvertinant naudą. žindymo kūdikiui ir terapijos naudos moteriai.
Vaisingumas
Žiurkių patinų ir patelių vaisingumas nepaveikė, kai ekspozicija buvo panaši į žmonių, tačiau negalima atmesti pavojaus žmonėms (žr. 5.3 skyrių).
04.7 Poveikis gebėjimui vairuoti ir valdyti mechanizmus
Eltrombopagas gebėjimą vairuoti ir valdyti mechanizmus veikia nereikšmingai. Vertinant paciento gebėjimą atlikti užduotis, reikalaujančias sprendimo, motorinių ir pažinimo įgūdžių, reikia atsižvelgti į klinikinę paciento būklę ir eltrombopago nepageidaujamų reakcijų pobūdį, įskaitant galvos svaigimą ir budrumo stoką.
04.8 Nepageidaujamas poveikis
Saugos profilio santrauka
4 kontroliuojamuose ir 2 nekontroliuojamuose klinikiniuose tyrimuose 530 suaugusių pacientų, sergančių lėtine ITP, buvo gydyti eltrombopagu. Vidutinė eltrombopago ekspozicijos trukmė buvo 260 dienų.Svarbiausios sunkios nepageidaujamos reakcijos buvo toksinis poveikis kepenims ir tromboziniai / tromboemboliniai reiškiniai. Dažniausios nepageidaujamos reakcijos, pasireiškusios mažiausiai 10% pacientų, buvo: galvos skausmas, anemija, sumažėjęs apetitas, nemiga, kosulys, pykinimas, viduriavimas, alopecija, niežulys, mialgija, karščiavimas, nuovargis, į gripą panaši liga, astenija, šaltkrėtis ir periferinė edema.
Dviejuose kontroliuojamuose klinikiniuose tyrimuose 171 pediatrinis pacientas, sergantis lėtine ITP, buvo gydomas eltrombopagu. Vidutinė ekspozicijos trukmė buvo 171 diena. Nepageidaujamų reakcijų profilis buvo panašus į suaugusiųjų, kuriems pasireiškė kai kurios papildomos nepageidaujamos reakcijos, pažymėtos „Lentelėje“.
Dažniausios nepageidaujamos reakcijos 1 metų ir vyresniems vaikams, sergantiems ITP (≥ 3% ir daugiau nei placebas), buvo pagrindinės kvėpavimo takų infekcijos, nazofaringitas, kosulys, viduriavimas, karščiavimas, rinitas, pilvo skausmas, burnos ir ryklės skausmas, dantų skausmas, odos bėrimas, padidėjęs AST ir rinorėja.
2 kontroliuojamų klinikinių tyrimų metu eltrombopagu buvo gydomi 955 pacientai, sergantys trombocitopenija, sergančiais HCV infekcija. Vidutinė ekspozicijos trukmė buvo 183 dienos. Svarbiausios nustatytos sunkios nepageidaujamos reakcijos buvo toksinis poveikis kepenims ir trombozės / tromboembolijos reiškiniai. Dažniausios nepageidaujamos reakcijos, pasireiškusios mažiausiai 10% pacientų, buvo: galvos skausmas, anemija, sumažėjęs apetitas, nemiga, kosulys , pykinimas, viduriavimas, alopecija, niežėjimas, mialgija, karščiavimas, nuovargis, į gripą panaši liga, astenija, šaltkrėtis ir periferinė edema.
Eltrombopago saugumas sergant sunkia aplastine anemija buvo įvertintas atvirame vienos rankos klinikiniame tyrime (N = 43), kuriame 12 pacientų (28%) buvo gydomi ilgiau nei 6 mėnesius ir 9 pacientai (21%). > 1 metus. Svarbiausios sunkios nepageidaujamos reakcijos buvo febrilinė neutropenija ir sepsis / infekcijos. Dažniausios nepageidaujamos reakcijos (bent 10% pacientų) buvo: galvos skausmas, galvos svaigimas, nemiga, kosulys, dusulys, burnos ryklės skausmas, rinorėja, pykinimas, viduriavimas, pilvo skausmas, padidėjęs transaminazių kiekis, kraujosruvos, artralgija, raumenų spazmai, galūnių skausmas, nuovargis, febrilinė neutropenija ir karščiavimas.
Nepageidaujamų reakcijų sąrašas
Nepageidaujamos reakcijos suaugusiųjų ITP tyrimuose (N = 550), vaikų ITP tyrimuose (N = 107) ir HCV infekuotuose tyrimuose (N = 955), AAS tyrimuose (N = 43) ir ataskaitos po pateikimo į rinką išvardytos žemiau pagal MedDRA organų sistemų klases ir dažnį .
Labai dažni (≥ 1/10)
Dažni (nuo ≥ 1/100 iki
Nedažni (nuo ≥ 1/1 000 iki
Reti (nuo ≥ 1/10 000 iki
Labai retas (
Nežinomas (negali būti įvertintas pagal turimus duomenis)
ITP klinikinio tyrimo populiacija
Infekcijos ir užkrėtimai
Labai dažnas
Nazofaringitas?, viršutinių kvėpavimo takų infekcijos?
dažnas
Rinitas?
Nedažni
Faringitas, šlapimo takų infekcijos, gripas, burnos pūslelinė, pneumonija, sinusitas, tonzilitas, kvėpavimo takų infekcijos, gingivitas, odos infekcija
Gerybiniai, piktybiniai ir nepatikslinti navikai (įskaitant cistas ir polipus)
Nedažni
Rektosigmoidinio trakto navikas
Kraujo ir limfinės sistemos sutrikimai
Nedažni
Anemija, anizocitozė, eozinofilija, hemolizinė anemija, leukocitozė, mielocitozė, trombocitopenija, padidėjęs hemoglobinas, padidėjęs neutrofilų skaičius, sumažėjęs hemoglobinas, mielocitų buvimas, padidėjęs trombocitų skaičius, sumažėjęs baltųjų kraujo kūnelių skaičius.
Imuninės sistemos sutrikimai
Nedažni
Padidėjęs jautrumas
Metabolizmo ir mitybos sutrikimai
Nedažni
Anoreksija, hipokalemija, sumažėjęs apetitas, podagra, hipokalcemija, padidėjęs šlapimo rūgšties kiekis kraujyje
Psichikos sutrikimai
Nedažni
Miego sutrikimai, depresija, apatija, nuotaikų kaita, lengvas verksmas
Nervų sistemos sutrikimai
dažnas
Parestezijos
Nedažni
Hipestezija, mieguistumas, migrena, drebulys, pusiausvyros sutrikimai, disestezija, hemiparezė, migrena su aura, periferinė neuropatija, periferinė sensorinė neuropatija, kalbos sutrikimai, toksinė neuropatija, kraujagyslių galvos skausmas
Akių sutrikimai
dažnas
Sausa akis
Nedažni
Neryškus matymas, lęšiuko drumstumas, astigmatizmas, žievės katarakta, akių skausmas, padidėjęs ašarojimas, kraujavimas iš tinklainės, tinklainės pigmento epitelioopatija, sumažėjęs regėjimo aštrumas, regos sutrikimas, regėjimo aštrumo tyrimo sutrikimai, blefaritas ir keratokonjunktyvitas
Ausų ir labirintų sutrikimai
Nedažni
Ausų skausmas, galvos svaigimas
Širdies patologijos
Nedažni
Tachikardija, ūminis miokardo infarktas, širdies ir kraujagyslių sistemos sutrikimai, cianozė, sinusinė tachikardija, elektrokardiogramos QT intervalo pailgėjimas
Kraujagyslių patologijos
Nedažni
Giliųjų venų trombozė, embolija, paraudimas, paviršinis tromboflebitas, paraudimas, hematoma
Kvėpavimo sistemos, krūtinės ląstos ir tarpuplaučio sutrikimai
dažnas
Kosulys, ryklės skausmas, rinorėja?
Nedažni
Plaučių embolija, plaučių infarktas, diskomfortas nosyje, pūslės burnos ryklėje, skausmas burnos ryklėje, sinusų sutrikimai, miego apnėjos sindromas
Virškinimo trakto sutrikimai
dažnas
Pykinimas, viduriavimas *, burnos išopėjimas, dantų skausmas?
* Labai dažni ITP sergantiems vaikams
Nedažni
Burnos džiūvimas, vėmimas, pilvo skausmas, glossodynija, kraujavimas iš burnos, pilvo įtampa, išmatų spalvos pasikeitimas, vidurių pūtimas, apsinuodijimas maistu, dažni pilvo judesiai, hematemezė, diskomfortas burnoje
Kepenų ir tulžies pūslės sutrikimai
dažnas
Alanino aminotransferazės * padidėjimas, aspartato aminotransferazės * padidėjimas, hiperbilirubinemija, kepenų funkcijos sutrikimai
Nedažni
Cholestazė, kepenų pažeidimas, hepatitas, vaistų sukeltas kepenų pažeidimas
* Alanino aminotransferazės ir aspartato aminotransferazės koncentracija gali padidėti vienu metu, nors ir rečiau.
Odos ir poodinio audinio sutrikimai
dažnas
Bėrimas, alopecija
Nedažni Hiperhidrozė, bendras niežėjimas, dilgėlinė, dermatozė, petechijos, šaltas prakaitas, eritema, melanozė, pigmentacijos sutrikimai, odos spalvos pasikeitimas, odos lupimasis
Skeleto, raumenų ir jungiamojo audinio sutrikimai
dažnas
Mialgija, raumenų spazmai, raumenų ir kaulų skausmas, kaulų skausmas, nugaros skausmas
Nedažni
Raumenų silpnumas
Inkstų ir šlapimo takų sutrikimai
Nedažni
Inkstų nepakankamumas, leukociturija, lupoidinis nefritas, nokturija, proteinurija, padidėjęs karbamido kiekis kraujyje, padidėjęs kreatinino kiekis kraujyje, padidėjęs baltymų ir kreatinino santykis
Reprodukcinės sistemos ir krūties ligos
dažnas
Menoragija
Bendrieji sutrikimai ir vartojimo vietos pažeidimai
dažnas
Karščiavimas?
Nedažni
Krūtinės skausmas, karščio pojūtis, kraujavimas parenteralinės injekcijos vietoje, astenija, nervingumas, žaizdų uždegimas, negalavimas, karščiavimas, svetimkūnio pojūtis
Diagnostiniai testai
Nedažni
Padidėjęs kraujo albumino kiekis, padidėjęs šarminės fosfatazės kiekis kraujyje, padidėjęs bendras baltymų kiekis, sumažėjęs albumino kiekis kraujyje, padidėjęs šlapimo pH
Sužalojimai, apsinuodijimai ir procedūrinės komplikacijos
Nedažni
Saulės nudegimas
? Papildomos nepageidaujamos reakcijos, pastebėtos vaikų populiacijos tyrimuose (nuo 1 iki 17 metų)
HCV infekuotų klinikinių tyrimų populiacija (kartu su antivirusiniu gydymu interferonu ir ribavirinu)
Infekcijos ir užkrėtimai
dažnas
Šlapimo takų infekcijos, viršutinių kvėpavimo takų infekcijos, bronchitas, nazofaringitas, gripas, burnos pūslelinė, gastroenteritas, faringitas.
Gerybiniai, piktybiniai ir nepatikslinti navikai (įskaitant cistas ir polipus)
dažnas
Piktybinis kepenų navikas
Kraujo ir limfinės sistemos sutrikimai
Labai dažnas
Anemija
dažnas limfocitopenija, hemolizinė anemija
Metabolizmo ir mitybos sutrikimai
Labai dažnas
Sumažėjęs apetitas
dažnas
Hiperglikemija, nenormalus svorio kritimas
Psichikos sutrikimai
Labai dažnas
Nemiga
dažnas
Depresija, nerimas, miego sutrikimai, sumišimas, susijaudinimas
Nervų sistemos sutrikimai
Labai dažnas
Galvos skausmas
dažnas
Galvos svaigimas, dėmesio sutrikimas, disgeuzija, kepenų encefalopatija, mieguistumas, atminties sutrikimas, parestezija
Akių sutrikimai
dažnas
Katarakta, tinklainės eksudatai, akių sausumas, sklerinė gelta, tinklainės kraujavimas
Ausų ir labirintų sutrikimai
dažnas
Galvos svaigimas
Širdies patologijos
dažnas
Palpitacijos
Kvėpavimo sistemos, krūtinės ląstos ir tarpuplaučio sutrikimai
Labai dažnas
Kosulys
dažnas
Dusulys, burnos ir ryklės skausmas, dusulys krūvio metu, produktyvus kosulys
Virškinimo trakto sutrikimai
Labai dažnas
Pykinimas, viduriavimas
dažnas
Vėmimas, ascitas, pilvo skausmas, viršutinės pilvo dalies skausmas, dispepsija, burnos džiūvimas, vidurių užkietėjimas, pilvo pūtimas, dantų skausmas, stomatitas, stemplės refliukso liga, hemorojus, diskomfortas pilve, gastritas, stemplės varikozė, aftinis stomatitas, stemplės varikozė
Kepenų ir tulžies pūslės sutrikimai
dažnas
Hiperbilirubinemija, gelta, vartų venų trombozė, kepenų nepakankamumas, vaistų sukeltas kepenų pažeidimas
Odos ir poodinio audinio sutrikimai
Labai dažnas
Niežėjimas, alopecija
dažnas
Bėrimas, sausa oda, egzema, niežtintis bėrimas, eritema, hiperhidrozė, bendras niežėjimas, prakaitavimas naktį, odos pažeidimai
Nedažni
Odos spalvos pasikeitimas, odos hiperpigmentacija
Skeleto, raumenų ir jungiamojo audinio sutrikimai
Labai dažnas
Mialgija
dažnas
Artralgija, raumenų spazmai, nugaros skausmas, galūnių skausmas, raumenų ir kaulų skausmas, kaulų skausmas
Inkstų ir šlapimo takų sutrikimai
Nedažni
Disurija
Bendrieji sutrikimai ir vartojimo vietos pažeidimai
Labai dažnas
Karščiavimas, nuovargis, į gripą panaši liga, astenija, šaltkrėtis, periferinė edema
dažnas
Dirglumas, skausmas, negalavimas, reakcijos injekcijos vietoje, ne širdies krūtinės skausmas, edema, bėrimas injekcijos vietoje, diskomfortas krūtinėje, niežulys injekcijos vietoje
Diagnostiniai testai
dažnas
Padidėjęs bilirubino kiekis kraujyje, sumažėjęs svoris, sumažėjęs baltųjų kraujo kūnelių skaičius, sumažėjęs hemoglobino kiekis, sumažėjęs neutrofilų skaičius, padidėjęs tarptautinis normalizuotas santykis (INR), pailgėjęs aktyvuotas dalinis tromboplastino laikas, padidėjęs gliukozės kiekis kraujyje, sumažėjęs albumino kiekis kraujyje, QT intervalo pailgėjimas elektrokardiogramoje
AAS klinikinio tyrimo populiacija
Kraujo ir limfinės sistemos sutrikimai
dažnas
Neutropenija, blužnies infarktas
Metabolizmo ir mitybos sutrikimai
dažnas
Geležies perteklius, apetito praradimas, hipoglikemija, padidėjęs apetitas
Psichikos sutrikimai
Labai dažnas
Nemiga
dažnas
Nerimas, depresija
Nervų sistemos sutrikimai
Labai dažnas
Galvos skausmas, galvos svaigimas
dažnas
Sinkopė
Akių sutrikimai
dažnas
Akių sausumas, akių niežėjimas, katarakta, akių gelta, neryškus matymas, regos sutrikimas, plūdės
Kvėpavimo sistemos, krūtinės ląstos ir tarpuplaučio sutrikimai
Labai dažnas
Kosulys, dusulys, ryklės skausmas, rinorėja
dažnas
Kraujavimas iš nosies
Virškinimo trakto sutrikimai
Labai dažnas
Pilvo skausmas, viduriavimas, pykinimas
dažnas
Kraujavimas iš dantenų, burnos gleivinės pūslės, burnos skausmas, vėmimas, diskomfortas pilve, pilvo skausmas, vidurių užkietėjimas, pilvo pūtimas, disfagija, išmatų spalvos pasikeitimas, liežuvio patinimas, žarnyno judrumo sutrikimai, vidurių pūtimas
Kepenų ir tulžies pūslės sutrikimai
Labai dažnas
Padidėjęs transaminazių kiekis
dažnas
Padidėjęs bilirubino kiekis kraujyje (hiperbilirubinemija), gelta
Nežinomas
Vaistų sukeltas kepenų pažeidimas *
* Buvo pranešta apie vaistų sukeltus kepenų pažeidimo atvejus ITP ir HCV sergantiems pacientams
Odos ir poodinio audinio sutrikimai
Labai dažnas
Mėlynės
dažnas
Petechijos, bėrimas, niežėjimas, dilgėlinė, odos pažeidimai, geltonosios dėmės bėrimas
Nedažni
Odos spalvos pasikeitimas, odos hiperpigmentacija
Skeleto, raumenų ir jungiamojo audinio sutrikimai
Labai dažnas
Artralgija, raumenų spazmai, galūnių skausmas
dažnas
Nugaros skausmas, mialgija, kaulų skausmas
Inkstų ir šlapimo takų sutrikimai
dažnas
Chromaturija
Bendrieji sutrikimai ir vartojimo vietos pažeidimai
Labai dažnas
Nuovargis, karščiavusi neutropenija, karščiavimas
dažnas
Astenija, periferinė edema, šaltkrėtis, negalavimas
Diagnostiniai testai
dažnas
Padidėjęs kreatinino fosfokinazės kiekis kraujyje
Pasirinktų nepageidaujamų reakcijų aprašymas
Tromboziniai / tromboemboliniai reiškiniai (TEE)
3 kontroliuojamuose ir 2 nekontroliuojamuose klinikiniuose tyrimuose tarp suaugusių pacientų, sergančių lėtiniu ITP, vartojusių eltrombopagą (n = 446), 17 tiriamųjų iš viso patyrė 19 tromboembolinių reiškinių, įskaitant (mažėjančio dažnio tvarka) giliųjų venų trombozę (n = 6) , plaučių embolija (n = 6), ūminis miokardo infarktas (n = 2), smegenų infarktas (n = 2), embolija (n = 1) (žr. 4.4 skyrių).
Placebu kontroliuojamo tyrimo metu (n = 288, saugi populiacija) po 2 gydymo savaičių, ruošiantis invazinėms procedūroms, 6 iš 143 (4%) suaugusių pacientų, sergančių lėtine kepenų liga, vartoję 7 eltrombopagą, patyrė 7 TEE. Portalo venų sistema ir 2 iš 145 tiriamųjų (1%) placebo grupėje buvo 3 TEE. Penki iš 6 pacientų, gydytų eltrombopagu, turėjo TEE, kurių trombocitų skaičius> 200 000 / μl.
Tiems asmenims, kuriems pasireiškė TEE, specifinių rizikos veiksnių nenustatyta, išskyrus trombocitų skaičių ≥ 200 000 / μl (žr. 4.4 skyrių).
Kontroliuojamuose tyrimuose, kuriuose dalyvavo pacientai, sergantys trombocitopenija, užsikrėtusiais HCV (n = 1439), 38 iš 955 (4%) eltrombopagu gydytų asmenų turėjo TEE, o 6 iš 484 tiriamųjų (1%) placebo grupėje-TEE. Portalo venų trombozė buvo dažniausia TEE abiejose gydymo grupėse (2% eltrombopagu gydytų pacientų) prieš
Kepenų nepakankamumas (vartojamas kartu su interferonu)
Lėtiniu HCV hepatitu sergantiems pacientams, sergantiems ciroze, gali kilti kepenų dekompensacijos rizika gydant alfa interferonu. Dviejuose kontroliuojamuose klinikiniuose tyrimuose, kuriuose dalyvavo pacientai, sergantys trombocitopenija, sergančiais HCV infekcija, kepenų dekompensacija (ascitas, kepenų encefalopatija, varikozinis kraujavimas, spontaniškas bakterinis peritonitas) eltrombopago grupėje (11%) pasireiškė dažniau nei placebo grupėje (6%). Pacientams, kurių pradinis albumino kiekis (≤ 35 g / l) arba MELD balas buvo ≥ 10, buvo tris kartus didesnė kepenų dekompensacijos rizika ir didesnė mirtinų nepageidaujamų reiškinių rizika, palyginti su pacientais, sergančiais mažiau kepenų liga. Eltrombopagą tokiems pacientams galima skirti tik gerai įvertinus laukiamą naudą ir riziką. Šias charakteristikas turinčius pacientus reikia atidžiai stebėti, ar neatsiranda kepenų dekompensacijos požymių ir simptomų (žr. 4.4 skyrių).
Trombocitopenija nutraukus gydymą
Trijų ITP kontroliuojamų klinikinių tyrimų metu, nutraukus gydymą, trombocitų skaičius laikinai sumažėjo žemiau pradinio lygio, atitinkamai 8% eltrombopago ir 8% placebo grupės (žr. 4.4 skyrių).
Padidėjęs retikulino kiekis kaulų čiulpuose
Programoje nė vienas pacientas neturėjo kliniškai reikšmingų kaulų čiulpų anomalijų ar klinikinių požymių, rodančių kaulų čiulpų funkcijos sutrikimą. Nedideliam skaičiui ITP sergančių pacientų gydymas eltrombopagu buvo nutrauktas dėl kaulų čiulpų retikulino kaulų (žr. 4.4 skyrių).
Citogenetinės anomalijos
Atliekant vienos grupės atvirą klinikinį AAS tyrimą, pacientams buvo atlikti kaulų čiulpų aspiracijos, siekiant įvertinti citogenetinius sutrikimus.Buvo pranešta apie naują citogenetinę anomaliją aštuoniems (19%) pacientams, įskaitant 5 pacientus, kuriems buvo nustatytas 7 chromosomos pakitimas. Dviejuose vykstančiuose tyrimuose (ELT116826 ir ELT116643) citogenetiniai sutrikimai buvo nustatyti 4/28 (14%) ir Atitinkamai 4/62 (6%) tiriamųjų.
Hematologiniai navikai
Trijų (7%) pacientų, atliktų vienos grupės, atviro AAS klinikinio tyrimo metu, MDS buvo diagnozuotas po gydymo eltrombopagu, dviejuose vykstančiuose tyrimuose (ELT116826 ir ELT116643) MDS arba AML diagnozuota 1 /28 (4) %) ir 1/62 (2%) tiriamųjų kiekviename tyrime.
Pranešimas apie įtariamas nepageidaujamas reakcijas
Svarbu pranešti apie įtariamas nepageidaujamas reakcijas, atsiradusias po vaistinio preparato registravimo, nes tai leidžia nuolat stebėti vaisto naudos ir rizikos santykį. Sveikatos priežiūros specialistų prašoma pranešti apie bet kokias įtariamas nepageidaujamas reakcijas per Italijos vaistų agentūrą. , svetainė: www.agenziafarmaco.gov.it/it/responsabili.
04.9 Perdozavimas
Perdozavus, trombocitų skaičius gali labai padidėti ir sukelti trombozines / tromboembolines komplikacijas. Perdozavimo atveju reikia apsvarstyti geriamojo preparato, kuriame yra metalo katijono, pvz., Kalcio, aliuminio ar magnio preparatų, vartojimą, kad chelatuotų eltrombopagą ir taip sumažėtų jo absorbcija. Reikia atidžiai stebėti trombocitų skaičių. vaistą reikia atnaujinti pagal dozavimo ir vartojimo rekomendacijas (žr. 4.2 skyrių).
Klinikinių tyrimų metu buvo pranešta apie perdozavimą, kai tiriamasis išgėrė 5000 mg eltrombopago. Nepageidaujamos reakcijos, apie kurias pranešta, buvo lengvas bėrimas, laikina bradikardija, ALT ir AST padidėjimas ir nuovargis. Kepenų fermentų, išmatuotų nuo 2 iki 18 dienos po nurijimo, didžiausias AST rodiklis buvo 1,6 karto l VNR, o ALT - 3,9 karto didesnis už viršutinę ribą, o bendras bilirubinas - 2,4 karto didesnis. Trombocitų skaičius buvo 672 000 / μl 18 dieną po nurijimo, o didžiausias - 929 000 / μl. Visi įvykiai po gydymo išnyko be pasekmių.
Kadangi eltrombopagas reikšmingai neišsiskiria per inkstus ir stipriai jungiasi su plazmos baltymais, manoma, kad hemodializė nebus veiksmingas būdas padidinti eltrombopago eliminaciją.
05.0 FARMAKOLOGINĖS SAVYBĖS
05.1 Farmakodinaminės savybės
Farmakoterapinė grupė: hemoraginiai vaistai, kiti sisteminiai hemostaziniai vaistai.
ATC kodas: B02BX 05.
Veiksmo mechanizmas
Trombopoetinas (TPO) yra pagrindinis citokinas, dalyvaujantis reguliuojant megakaripoezę ir trombocitų gamybą, ir yra endogeninis TPO receptorių (TPO-R) ligantas. Eltrombopagas sąveikauja su žmogaus TPO-R transmembraniniu domenu ir inicijuoja signalų kaskadą, panašią į endogeninio TPO, bet ne identišką, sukeldamas proliferaciją ir diferenciaciją nuo kaulų čiulpų kamieninių ląstelių.
Klinikinis veiksmingumas ir saugumas
Lėtinės autoimuninės (idiopatinės) trombocitopenijos (ITP) tyrimai
Dviejuose III fazės atsitiktinių imčių, dvigubai akluose, placebu kontroliuojamuose tyrimuose RAISE (TRA102537) ir TRA100773B bei dviejuose atviruose tyrimuose REPEAT (TRA108057) ir EXTEND (TRA105325) buvo įvertintas eltrombopago saugumas ir veiksmingumas suaugusiems pacientams, anksčiau gydytiems. lėtinis ITP.
Apskritai eltrombopagas buvo skiriamas 277 pacientams, sergantiems ITP, mažiausiai 6 mėnesius ir 202 pacientams mažiausiai 1 metus.
Dvigubai akli placebu kontroliuojami tyrimai
KELIMAS: 197 pacientai, sergantys ITP, buvo atsitiktinai atrinkti santykiu 2: 1 su eltrombopagu (n = 135) ir placebu (n = 62), o atsitiktinės atrankos tvarka buvo suskirstyta pagal splenektomiją, pradinį TPI vartojimą ir trombocitų skaičių. koreguoti per 6 mėnesių gydymo laikotarpį, atsižvelgiant į individualų trombocitų skaičių. Visi pacientai pradėjo vartoti 50 mg eltrombopagą. 29 diena iki gydymo pabaigos, nuo 15 dienos iki gydymo pabaigos. 28% eltrombopagu gydytų pacientų buvo išlaikytas ≤ 25 mg ir 29-53% gavo 75 mg.
Be to, pacientai gali palaipsniui mažinti kartu vartojamus ITP vaistus ir gauti gelbėjimo gydymą, kaip nurodyta vietinėse gydymo gairėse. Daugiau nei pusė visų pacientų kiekvienoje gydymo grupėje anksčiau vartojo ≥ 3 ITP, o 36% - splenektomiją.
Vidutinis pradinis trombocitų skaičius abiejose gydymo grupėse buvo 16 000 / μl, o eltrombopago grupėje jis buvo didesnis nei 50 000 / μl visuose gydymo metu, pradedant nuo 15 dienos; tačiau placebo grupėje trombocitų skaičiaus mediana išliko
Trombocitų skaičiaus atsakas tarp 50 000–400 000 / μl, jei nebuvo atlikta gelbėjimo terapija, buvo pasiektas žymiai didesniu eltrombopago grupės pacientų skaičiumi per 6 mėnesių gydymo laikotarpį, p
4 lentelė. RAISE tyrimo antrinio veiksmingumo rezultatai
logistinės regresijos modelis, pritaikytas atsitiktinių imčių stratifikacijos kintamiesiems
b 21 iš 63 (33%) eltrombopagu gydytų pacientų, vartojusių pagrindinį ITP vaistą, visam laikui nutraukė visų pagrindinių ITP vaistų vartojimą.
Pradžioje daugiau nei 70% ITP pacientų kiekvienoje gydymo grupėje pranešė apie bet kokio tipo kraujavimą (PSO 1-4 laipsnio) ir daugiau nei 20%-atitinkamai kliniškai reikšmingą kraujavimą (PSO 2-4 laipsnio). Eltrombopagu gydytų pacientų, sergančių bet kokio tipo kraujavimu (1–4 laipsniai) ir kliniškai reikšmingo kraujavimo (2–4 laipsniai), dalis nuo gydymo pradžios sumažėjo maždaug 50% nuo 15 dienos iki gydymo pabaigos per visą 6 mėnesių gydymo laikotarpį. .
TRA100773B: L "galutinis taškas pirminis veiksmingumas buvo dalis atsakytojai, buvo laikomi pacientai, sergantys ITP, kuriems trombocitų skaičius padidėjo iki ≥ 50 000 / μl 43 dieną nuo pradinės 200 000 / μl vertės respondentų, buvo svarstomi tie, kurie nutraukė gydymą dėl kitų priežasčių neatsakiusieji nepriklausomai nuo trombocitų skaičiaus. Iš viso 114 pacientų, anksčiau gydytų lėtiniu ITP, atsitiktinės atrankos būdu buvo paskirti eltrombopagu (n = 76) ir placebu (n = 38).
5 lentelė. TRA100773B tyrimo veiksmingumo rezultatai
a - Logistinės regresijos modelis, pritaikytas atsitiktinių imčių stratifikacijos kintamiesiems
Tiek RAISE, tiek TRA100773B atveju atsakas į eltrombopagą, lyginant su placebu, buvo panašus, nepriklausomai nuo naudojamo ITP vaisto, blužnies pašalinimo ir pradinio trombocitų skaičiaus (≤ 15 000 / μl,> 15 000 / μl) atsitiktinės atrankos būdu.
RAISE ir TRA100773B tyrimų ITP pacientų pogrupyje, kurio trombocitų skaičius iš pradžių buvo ≤ 15 000 / μl, vidutinis trombocitų skaičius (> 50 000 / μl) nebuvo pasiektas, nors abiejuose tyrimuose 43% šių pacientų, gydytų eltrombopagu, reagavo pasibaigus 6 savaičių gydymo laikotarpiui. Be to, RAISE tyrimo metu 6% gydymo laikotarpio pabaigoje 42% pacientų, kurių pradinis trombocitų skaičius ≤ 15 000 / μl, buvo gydomi eltrombopagu. Keturiasdešimt du-60% RAISE tyrimo metu eltrombopagu gydytų pacientų nuo 29 dienos iki gydymo pabaigos vartojo 75 mg.
Atviras kartotinių dozių tyrimas (3 6 gydymo savaičių kursai su 4 savaičių be gydymo) parodė, kad epizodinis vartojimas su keliais eltrombopago kursais nesumažino atsako.
Atvirame tęstiniame tyrime EXTEND (TRA105325) Eltrombopag buvo skirtas 302 pacientams, sergantiems ITP, 218 baigė 1 metus, 180 baigė 2 metus, 107 baigė 3 metus, 75 baigė 4 metus, 34 baigė 5 metus ir 18 baigė 6 metus. Prieš vartojant eltrombopagą, trombocitų skaičiaus mediana pradžioje buvo 19 000 / μl. Vidutinis trombocitų skaičius 1, 2, 3, 4, 5, 6 ir 7 tyrimo metais buvo 85 000 / mikrolitras, 85 000 / mikrolitras, 105 000 / mikrolitras, 64 000 / mikrolitras, 75 000 / mikrolitras, 119 000 / mikrolitras ir 76 000 / microliter microliter, atitinkamai.
Nebuvo atlikta jokių klinikinių tyrimų, kuriuose eltrombopagas būtų lyginamas su kitomis terapinėmis galimybėmis (pvz., Splenektomija). Prieš pradedant gydymą, reikia apsvarstyti ilgalaikį eltrombopago saugumą.
Vaikų populiacija (1–17 metų)
Eltrombopago saugumas ir veiksmingumas vaikams buvo vertinamas dviejuose tyrimuose. TRA115450 (PETIT2): Pirminė baigtis buvo ilgalaikis atsakas, apibrėžiamas kaip eltrombopagu gydytų tiriamųjų dalis, palyginti su placebu, kurių trombocitų skaičius buvo ≥ 50 000 / mcl mažiausiai 6 iš 8 savaičių (nesant gelbėjimo terapijos), 5 ir 5 savaites. 12 atsitiktinės atrankos dvigubai aklu laikotarpiu. Tiriamieji, kuriems buvo diagnozuotas lėtinis ITP mažiausiai 1 metus ir kurie buvo atsparūs ugniai arba kuriems pasikartojo bent vienas ankstesnis ITP gydymas arba dėl kokios nors priežasties negalėjo tęsti kitų ITP procedūrų ir turėjo trombocitų skaičių
Apskritai, žymiai didesnė dalis eltrombopago grupės asmenų (40%) pasiekė pirminį rezultatą (šansų santykis: 18,0 [95% PI: 2,3, 140,9] p
6 lentelė. Ilgalaikis trombocitų atsako dažnis pagal kohortos amžių vaikams, sergantiems lėtiniu ITP
Statistiškai mažiau eltrombopagu gydytų asmenų prireikė gelbėjimo gydymo atsitiktinių imčių laikotarpiu nei placebą vartojusių asmenų (19% [12/63] ir 24% [7/29], p = 0,032).
Pradiniame etape 71% eltrombopago grupės ir 69% placebo grupės pacientų pranešė apie kraujavimą (PSO 1–4 laipsniai). 12 savaitę eltrombopagu gydytų asmenų, pranešusių apie kraujavimą, dalis sumažėjo perpus (36%). Palyginimui, 12 savaitę 55% placebą vartojusių asmenų nepranešė apie kraujavimą.
Tiriamiesiems buvo leista sumažinti arba nutraukti foninę ITP terapiją tik atviro tyrimo etapo metu, o 53% (8/15) tiriamųjų galėjo sumažinti (n = 1) arba nutraukti (n = 7) pagrindinį gydymą. ITP, daugiausia kortikosteroidų, be gelbėjimo.
TRA108062 (PETIT): Pirminė vertinamoji baigtis buvo tiriamųjų, kuriems trombocitų skaičius buvo ≥ 50 000 / mcl bent kartą tarp atsitiktinės atrankos laikotarpio 1 ir 6 savaičių, dalis. Tiriamieji buvo atsparūs ugniai arba recidyvavo bent vieną ankstesnę ITP terapiją ir su trombocitais
Apskritai, žymiai didesnis eltrombopago grupės pacientų procentas (62%) pasiekė pirminį rezultatą (šansų santykis: 4,3 [95% PI: 1,4, 13,3] p = 0,011).
Nuolatinis atsakas buvo pastebėtas 50% pradinių respondentų per 20 iš 24 savaičių PETIT 2 tyrime ir 15 iš 24 savaičių PETIT tyrime.
Trombocitopenijos, susijusios su lėtiniu HCV hepatitu, tyrimai
Eltrombopago veiksmingumas ir saugumas gydant trombocitopeniją HCV užsikrėtusiems pacientams buvo įvertintas dviejuose atsitiktinių imčių, dvigubai akluose, placebu kontroliuojamuose tyrimuose. 2b ir ribavirino. Pacientai negavo tiesioginio veikimo antivirusinių vaistų. Abiejuose tyrimuose dalyvavo pacientai, kuriems buvo patikrintas trombocitų skaičius (
Ligos charakteristikos pradžioje buvo panašios abiejuose tyrimuose ir atitiko HCV užsikrėtusių pacientų, kuriems buvo kompensuota cirozė, populiaciją. Dauguma pacientų (1%) turėjo HCV 1 genotipą (64%) ir turėjo tiltinę fibrozę / cirozę. Trisdešimt vienas procentas pacientų anksčiau buvo gydomi nuo HCV infekcijos, daugiausia pegiliuotu interferonu ir ribavirinu. Abiejose gydymo grupėse trombocitų skaičius iš pradžių buvo 59 500 / μl: 0,8%, 28% ir 72% įdarbintų pacientų buvo trombocitų. skaičiuoja
Tyrimus sudarė dvi fazės - priešvirusinis prieš gydymo etapas ir antivirusinis gydymo etapas. Priešvirusinio išankstinio gydymo fazėje tiriamieji gavo atvirą eltrombopagą, kad padidintų trombocitų skaičių iki ≥ 90 000 / mcl ENABLE 1 ir ≥ 100 000 / mcl ENABLE 2. ) arba ≥ 100 000 / mcl (2 ĮJUNGIMAS) buvo 2 savaitės.
L "galutinis taškas abiejų tyrimų pirminis veiksmingumas buvo nuolatinis virusinis atsakas (palaikomas virusologinis atsakas, SVR), apibrėžiamas kaip procentas pacientų, sergančių HCV infekcija ir kurių neaptinkama HCV RNR 24 savaites po planuojamo gydymo laikotarpio pabaigos.
Abiejuose HCV infekuotuose tyrimuose reikšmingai didesnė eltrombopagu gydytų pacientų dalis (n = 201, 21%) pasiekė SVR, palyginti su tais, kurie buvo gydyti placebu (n = 65, 13%) (žr. 7 lentelę). Pacientų, pasiekusių SVR, dalies pagerėjimas buvo nuoseklus visuose pogrupiuose atsitiktinės atrankos sluoksniuose (pradinis trombocitų skaičius (palyginti su> 50 000), virusų kiekis (palyginti su ≥ 800 000 TV / ml) ir genotipas (2/3) vs. 1/4/6).
7 lentelė. Virusinis pacientų, sergančių HCV infekcija, atsakas ENABLE 1 ir ENABLE 2
a) Eltrombopagą, vartojamą kartu su peginterferonu alfa-2a (180 μg kartą per savaitę 48 savaites 1/4/6 genotipams; 24 savaites 2/3 genotipams) ir ribaviriną (nuo 800
1200 mg per parą, padalyta į dvi dozes per burną)
b Eltrombopagas, vartojamas kartu su peginterferonu alfa-2b (1,5 mcg/kg kartą per savaitę 48 savaites 1/4/6 genotipo atveju; 24 savaites 2/3 genotipo atveju) kartu su ribavirinu (800–1400 mg per burną, padalyta į 2 dozes)
c Tikslinis trombocitų skaičius buvo ≥ 90 000 / mcl ENABLE 1 ir ≥ 100 000 / mcl ENABLE 2. 1 ENABLE atveju 682 pacientai buvo atsitiktinai suskirstyti į antivirusinį gydymo etapą; tačiau du tiriamieji atšaukė savo sutikimą prieš skirdami antivirusinį gydymą.
d reikšmė p prieš placebą
ir 64% ENABLE 1 ir ENABLE 2 tyrime dalyvavusių asmenų turėjo 1 genotipą
f Post-hoc analizės
Kiti antriniai tyrimų stebėjimai: vs. 60%, p = 27%). Gydymas eltrombopagu atidėtas ir sumažintas peginterferono dozės mažinimo skaičius.
Sunki aplastinė anemija
Eltrombopagas buvo tirtas vienos rankos vieno centro atvirame klinikiniame tyrime, kuriame dalyvavo 43 pacientai, sergantys sunkia aplastine anemija ir atsparia trombocitopenija po mažiausiai vieno ankstesnio imunosupresinio gydymo (LPI) ir trombocitų skaičiaus ≤ 30 000 / μl.
Dauguma tiriamųjų, 33 (77 proc.), Buvo laikomi „pirminėmis ugniai atspariomis ligomis“, apibrėžtomis kaip „tinkamo pirmojo atsako į imunosupresinį gydymą nebuvimas bet kurioje eilutėje. Likusių 10 tiriamųjų atsakas į trombocitus buvo nepakankamas. Visi 10 pacientų, kuriems buvo atliktas mažiausiai 2 imunosupresinis gydymas, o 50% - mažiausiai 3 ankstesnius imunosupresinius gydymo režimus.
Fanconi, infekcija, nereaguojanti į tinkamą gydymą, PNH klonas ≥ 50%dydžio neutrofiluose, nebuvo įtrauktas į tyrimą.
Iš pradžių vidutinis trombocitų skaičius buvo 20 000 / μl, hemoglobinas-8,4 g / dL, absoliutus neutrofilų skaičius-0,58 x 109 / l, o absoliutus retikulocitų skaičius-24,3 x 109 / 1. Aštuoniasdešimt šeši procentai pacientų buvo priklausomi nuo eritrocitų perpylimų, o 91% priklausė nuo trombocitų perpylimo. Dauguma pacientų (84%) anksčiau buvo gydomi mažiausiai 2 imunosupresantais.Trys pacientai pradžioje turėjo citogenetinių anomalijų.
Pirminis vertinimo kriterijus buvo hematologinis atsakas, įvertintas po 12 gydymo eltrombopagu savaičių. Hematologinis atsakas buvo apibrėžiamas kaip vieno ar kelių iš šių kriterijų pasiekimas: 1) trombocitų skaičiaus padidėjimas iki 20 000 / µl virš pradinio lygio arba trombocitų skaičius stabilus, jei perpylimas nepriklauso mažiausiai 8 savaites; 2) padidėjęs hemoglobino kiekis> 1,5 g / dl arba perpylimas ≥ 4 vienetų raudonųjų kraujo kūnelių (RBC) 8 savaites iš eilės; 3) absoliutaus neutrofilų skaičiaus (ANC) padidėjimas 100% arba ANC padidėjimas> 0,5 x 109 / l.
Hematologinio atsako dažnis buvo 40% (17/43 pacientų; 95% PI 25, 56), o dauguma atsakymų apsiribojo viena linija (13 / 17,76%), o buvo užregistruoti 3 atsakymai. -linijinis atsakas 12 savaitę. Eltrombopago vartojimas buvo nutrauktas po 16 savaičių, jei nepastebėta hematologinio atsako ar nepriklausė nuo perpylimo. Respondentai tęsė gydymą pratęsimo tyrimo fazėje. pratęsimo tyrimo etape iš viso dalyvavo 14 pacientų. iš šių pacientų pasireiškė daugialypis atsakas, 4 iš 9 tęsė gydymą ir 5 palaipsniui mažino gydymą eltrombopagu ir išlaikė atsaką (stebėjimo mediana: 20,6 mėnesio, intervalas: 5,7–22,5 mėnesio). Likę 5 pacientai nutraukė gydymą, trys dėl recidyvas, pastebėtas trečio mėnesio pratęsimo fazės vizito metu.
Gydant eltrombopagu, 59% (23/39) nepriklausė nuo trombocitų perpylimo (28 dienos be trombocitų perpylimo) ir 27% (10/37) nepriklausė nuo raudonųjų kraujo kūnelių perpylimo (56 dienos be raudonųjų kraujo kūnelių perpylimo). Ilgiausias laikotarpis be trombocitų perpylimo nereaguotiems pacientams buvo 27 dienos (vidutiniškai). Ilgiausias laikotarpis be trombocitų perpylimo respondentams buvo 29 dienos (vidutiniškai). Ilgiausias laikotarpis be eritrocitų perpylimo respondentams buvo 266 dienos (vidutiniškai).
Daugiau nei 50% respondentų, kurie buvo priklausomi nuo kraujo perpylimo, pradžioje> 80% sumažėjo trombocitų ir raudonųjų kraujo kūnelių perpylimo poreikis.
Preliminarūs palaikomojo tyrimo (ELT116826 tyrimas), tęstinio neatsitiktinių imčių, II fazės, vienos grupės, atviro tyrimo su ugniai atspariais asmenimis, kuriems buvo AAS, rezultatai parodė nuoseklius rezultatus. Duomenys apsiriboja 21 iš 60 numatytų pacientų, o hematologinis atsakas buvo pastebėtas 52% pacientų per 6 mėnesius. Daugialypis atsakas buvo nustatytas 45% pacientų.
05.2 Farmakokinetinės savybės
Farmakokinetika
Eltrombopago koncentracijos plazmoje duomenys - 88 ITP sergančių pacientų TRA100773A ir TRA100773B metu surinktas laikas buvo derinamas su 111 sveikų suaugusių asmenų duomenimis, atlikus populiacijos farmakokinetinę analizę. Pateikti eltrombopago AUC (0-?) Ir Cmax reikšmės pacientams, sergantiems ITP, įverčiai (8 lentelė).
8 lentelė. Suaugusiųjų, sergančių ITP, geometrinis vidurkis (95% patikimumo intervalas) eltrombopago farmakokinetikos parametrų plazmoje esant pusiausvyrai
a-AUC (0-?) ir Cmax įvertinimai, pagrįsti post-hoc populiacijos farmakokinetikos vertėmis.
Duomenys apie eltrombopago koncentraciją plazmoje laikui bėgant, surinkti 590 HCV infekuotiems asmenims, dalyvavusiems III fazės tyrimuose TPL103922 / ENABLE 1 ir TPL108390 / ENABLE 2, buvo sujungti su duomenimis, gautais iš HCV infekuotų pacientų, įtrauktų į II fazės tyrimą TPL102357. populiacijos farmakokinetikos analizė. Eltrombopago plazmos Cmax ir AUC (0-?) įvertinimai HCV užsikrėtusiems pacientams, įtrauktiems į 3 fazės tyrimus, kiekvienai dozei išvardyti 9 lentelėje.
9 lentelė Geometrinis vidurkis (95% PI) allo pastovi būsena eltrombopago plazmos farmakokinetikos parametrus pacientams, sergantiems lėtine HCV infekcija
Duomenys pateikti kaip geometrinis vidurkis (95% PI).
AUC (0-?) Ir Cmax, pagrįsti įvertinimais post-hoc populiacijos farmakokinetiką, vartojant didžiausią dozę kiekvienam pacientui.
Absorbcija ir biologinis prieinamumas
Eltrombopagas absorbuojamas, didžiausia jo koncentracija susidaro praėjus 2–6 valandoms po geriamojo vaisto. Kartu vartojant eltrombopagą su antacidiniais vaistais ir kitais produktais, kurių sudėtyje yra daugiasluoksnių katijonų, pvz., Pieno produktais ir mineraliniais papildais, žymiai sumažėja eltrombopago ekspozicija (žr. 4.2 skyrių).. Santykinio suaugusiųjų biologinio prieinamumo tyrimo metu eltrombopago milteliai geriamajai suspensijai pasiekė 22% didesnį plazmos AUC (0-?), Palyginti su tabletėmis. Absoliutus geriamasis eltrombopago biologinis prieinamumas, skiriant žmogui, nenustatytas. Atsižvelgiant į išsiskyrimą su šlapimu ir metabolitus, išsiskiriančius su išmatomis, buvo nustatyta, kad išgėrus vienkartinę 75 mg eltrombopago tirpalo dozę, absorbcija per burną yra mažiausiai 52%.
Paskirstymas
Eltrombopagas yra stipriai susijęs su žmogaus plazmos baltymais (> 99,9%), daugiausia su albuminu.
Biotransformacija
Eltrombopagas pirmiausia metabolizuojamas skilimo, oksidacijos ir konjugacijos būdu su gliukurono rūgštimi, glutationu ar cisteinu. Radioaktyviai pažymėto žmogaus tyrimo metu eltrombopagas sudaro maždaug 64% AUC0-? radioaktyviai pažymėtų anglių koncentracija plazmoje. Taip pat buvo rasti nedideli metabolitai dėl gliukuronizacijos ir oksidacijos. Švietimas in vitro rodo, kad CYP1A2 ir CYP2C8 yra atsakingi už eltrombopago oksidacinį metabolizmą. Urido difosfoglukuroniltransferazės UGT1A1 ir UGT1A3 yra atsakingos už gliukuronizaciją, o bakterijos iš apatinio virškinimo trakto gali būti atsakingos už skilimą.
Eliminavimas
Absorbuotas eltrombopagas intensyviai metabolizuojamas. Pagrindinis eltrombopago išsiskyrimo būdas yra su išmatomis (59%), o 31% dozės randama šlapime metabolitų pavidalu. Nepakitusio junginio (eltrombopago) šlapime neaptinkama. Nepakitęs eltrombopagas, išsiskiriantis su išmatomis, sudaro maždaug 20% dozės. Eltrombopago pusinės eliminacijos iš plazmos laikas yra maždaug 21-32 valandos.
Farmakokinetinė sąveika
Remiantis tyrimu su žmonėmis, turinčiais radioaktyviai pažymėtą eltrombopagą, gliukuronizacija vaidina nedidelį vaidmenį eltrombopago metabolizme. Tyrimuose su žmogaus kepenų mikrosoma nustatyta, kad UGT1A1 ir UGT1A3 yra fermentai, atsakingi už eltrombopago gliukuronizaciją. in vitro. Kliniškai reikšmingos vaistų sąveikos, apimančios gliukuronidaciją, nenumatoma, nes atskirų UGT fermentų indėlis į eltrombopago gliukuronizaciją ir galimi kartu vartojami vaistai yra riboti.
Maždaug 21% eltrombopago dozės gali vykti oksidacinis metabolizmas. Tyrimai su žmogaus kepenų mikrosoma nustatė, kad CYP1A2 ir CYP2C8 yra fermentai, atsakingi už eltrombopago oksidaciją. Remiantis duomenimis, eltrombopagas neslopina ir nesukelia CYP fermentų in vitro ir in vivo (žr. 4.5 skyrių)
Švietimas in vitro parodė, kad eltrombopagas yra transporterio OATP1B1 inhibitorius ir yra transporterio BCRP inhibitorius, o eltrombopagas klinikinės sąveikos tyrimo metu padidina rozuvastatino substrato OATP1B1 ir BCRP ekspoziciją (žr. 4.5 skyrių). Klinikinių eltrombopago tyrimų metu Rekomenduojama 50% sumažinti statinų dozę. Kartu vartojant 200 mg ciklosporino (BCRP inhibitoriaus) eltrombopago Cmax ir AUCinf sumažėjo atitinkamai 25% ir 18%. Kartu vartojant 600 mg ciklosporino, eltrombopago Cmax ir AUCinf sumažėjo 39% ir Atitinkamai 24 proc.
Eltrombopagas chelatina polivalentinius katijonus, tokius kaip geležis, kalcis, magnis, aliuminis, selenas ir cinkas (žr. 4.2 ir 4.5 skyrius).
Vartojant vieną 50 mg eltrombopago dozę tabletėse kartu su įprastu kaloringu maistu, riebiais pusryčiais, kuriuose buvo pieno produktų, vidutinis eltrombopago AUC plazmoje sumažėjo 59%, o Cmax-vidutiniškai 65%.
Pavartojus vieną 25 mg eltrombopago miltelių geriamajai suspensijai dozę valgio metu, kuriame gausu kalcio, vidutinio riebumo ir kalorijų, vidutinis eltrombopago AUC0- α plazma sumažėjo 75%, o vidutinė Cmax-79%. Šis ekspozicijos sumažėjimas susilpnėjo, kai vienkartinė 25 mg eltrombopago miltelių dozė geriamajai suspensijai buvo sušvirkšta likus 2 valandoms iki didelio kalcio kiekio valgio (vidutinis AUC0-? sumažėjo 20%, o vidutinis Cmax-14%).
Maisto produktai, kurių sudėtyje nėra kalcio (vaisiai, liesas kumpis, jautiena ir vaisių sultys be pridėto kalcio, magnio ar geležies), sojos pienas be pridėtinio ir kviečiai neturi didelės įtakos eltrombopago ekspozicijai plazmoje, nepriklausomai nuo kalorijų ir riebalų kiekio (žr. 4.2 skyrių). ir 4.5).
Specialios pacientų grupės
Inkstų nepakankamumas
Suaugusiems pacientams, sergantiems inkstų nepakankamumu, eltrombopago farmakokinetika buvo tirta. Išgėrus vieną 50 mg dozę, eltrombopago AUC0- α buvo 32–36% mažesnis asmenims, kuriems buvo lengvas ar vidutinio sunkumo inkstų funkcijos sutrikimas, ir 60% mažesniam asmenims, kuriems buvo sunkus inkstų funkcijos sutrikimas. Palyginti su sveikais savanoriais. inkstų nepakankamumu sergančių pacientų ir sveikų savanorių ekspozicijos kintamumas ir reikšmingas sutapimas. Laisvos (aktyvios) šio didelio baltymų jungimosi vaistinio preparato eltrombopago koncentracijos nebuvo matuojamos. Pacientams, kurių inkstų funkcija sutrikusi, eltrombopagą reikia vartoti atsargiai ir atidžiai stebint, pvz. atliekant kreatinino koncentraciją serume ir (arba) šlapimo tyrimus (žr. 4.2 skyrių). Eltrombopago veiksmingumas ir saugumas nenustatytas.
Kepenų nepakankamumas
Eltrombopago farmakokinetika buvo tiriama pavartojus eltrombopago suaugusiems pacientams, sergantiems kepenų nepakankamumu. Išgėrus vieną 50 mg dozę, eltrombopago AUC0- α buvo 41% didesnis asmenims, kuriems yra lengvas kepenų funkcijos sutrikimas, ir 80–93% didesnis asmenims, kuriems yra vidutinio sunkumo ar vidutinio sunkumo kepenų funkcijos sutrikimas, sunkus, lyginant su sveikais savanoriais. Kepenų nepakankamumu sergančių pacientų ir sveikų savanorių ekspozicija buvo labai įvairi ir labai sutapo. Šio didelio baltymų jungimosi vaistinio preparato laisvosios (aktyviosios) eltrombopago koncentracijos nebuvo išmatuotos.
Kepenų nepakankamumo įtaka eltrombopago farmakokinetikai po pakartotinio vartojimo buvo įvertinta naudojant populiacijos farmakokinetikos analizę, kurioje dalyvavo 28 sveiki suaugusieji ir 714 pacientų, kurių kepenų funkcija sutrikusi (673 pacientai, sergantys HCV infekcija ir 41 pacientas, sergantis lėtine kitos etiologijos kepenų liga). Iš šių 714 pacientų 642 sirgo lengvu kepenų nepakankamumu, 67 - vidutinio sunkumo, 2 - sunkiu kepenų nepakankamumu. Palyginti su sveikais savanoriais, pacientams, kuriems buvo lengvas kepenų funkcijos sutrikimas, eltrombopago AUC (0-?) Koncentracija plazmoje buvo didesnė nei maždaug 111% (95% PI: 45–283%), o pacientams, kuriems buvo vidutinio sunkumo kepenų funkcijos sutrikimas, eltrombopago AUC ( 0-?) Didesnis nei maždaug 183% (95% PI: nuo 90% iki 459%).
Todėl eltrombopago negalima vartoti ITP sergantiems pacientams, kuriems yra vidutinio sunkumo ar sunkus kepenų funkcijos sutrikimas (Child-Pugh rodiklis ≥ 5), nebent laukiama nauda yra didesnė už nustatytą vartų venų trombozės riziką (žr. 4.2 ir 4.4 skyrius). HCV užsikrėtusiems pacientams eltrombopagą reikia pradėti vartoti po 25 mg vieną kartą per parą (žr. 4.2 skyrių).
Lenktynės
Rytų Azijos tautybės įtaka eltrombopago farmakokinetikai buvo įvertinta naudojant populiacijos farmakokinetikos analizę 111 sveikų suaugusiųjų (31 Rytų Azijos) ir 88 pacientų, sergančių ITP (18 Rytų Azijos). pvz., japonų, kinų, taivaniečių ir korėjiečių), buvo maždaug 49% didesnės eltrombopago AUC (0-?) vertės plazmoje, palyginti su ne Rytų Azijos pacientais, kurie daugiausia buvo kaukaziečiai (žr. 4.2 skyrių).
Rytų Azijos tautybės (pvz., Kinų, japonų, taivaniečių, korėjiečių ir tailandiečių) įtaka eltrombopago farmakokinetikai buvo įvertinta naudojant populiacijos farmakokinetikos analizę 635 HCV infekuotiems pacientams (145 rytų azijiečiai ir 69 pietryčių azijiečiai), remiantis gyventojų skaičiavimais. farmakokinetikos analizė, Rytų Azijos tautybės pacientų eltrombopago AUC (0-?) plazmoje buvo maždaug 55% didesnė, palyginti su kitų rasių pacientais, kurių dauguma buvo baltaodžiai (žr. 4.2 skyrių).
Seksas
Lyties įtaka eltrombopago farmakokinetikai buvo įvertinta naudojant populiacijos farmakokinetikos analizę, kurioje dalyvavo 111 sveikų suaugusiųjų (14 moterų) ir 88 ITP pacientai (57 moterys). Remiantis populiacijos farmakokinetikos analizės duomenimis, ITP sergančių moterų eltrombopago AUC (0-?) Plazmos vertės buvo maždaug 23% didesnės, lyginant su vyrais, kūno svorio koregavimo nekeitė.
Lyties įtaka eltrombopago farmakokinetikai buvo įvertinta naudojant populiacijos farmakokinetikos analizę 635 HCV infekuotiems pacientams (260 moterų). Remiantis modelio įverčiais, moterų, sergančių HCV infekcija, eltrombopago AUC (0-?) Plazmos vertės buvo maždaug 41% didesnės nei vyrų vyrų.
Amžius
Amžiaus įtaka eltrombopago farmakokinetikai buvo įvertinta naudojant populiacijos farmakokinetikos analizę 28 sveikiems asmenims, 673 pacientams, sergantiems HCV infekcija, ir 41 pacientui, sergančiam kitos etiologijos lėtine kepenų liga, kurių amžius 19 metų. 74 metai. Farmakokinetinių duomenų apie eltrombopago vartojimas ≥ 75 metų pacientams. Remiantis modelio įverčiais, vyresnio amžiaus (≥ 65 metų) pacientų eltrombopago AUC (0-?) Vertės plazmoje buvo maždaug 41% didesnės nei jaunesnių pacientų (žr. 4.2 skyrių).
Vaikų populiacija (1–17 metų)
Eltrombopago farmakokinetika buvo įvertinta 168 vaikams, sergantiems ITP, atliekant du tyrimus vieną kartą per parą, TRA108062 / PETIT ir TRA115450 / PETIT-2. Tariamas eltrombopago klirensas išgėrus (CL / F) padidėjo didėjant kūno svoriui.
Rasės ir lyties poveikis vaikų ir suaugusių pacientų eltrombopago CL / F įvertinimams plazmoje buvo vienodas. Rytų Azijos vaikų ITP pacientų eltrombopago AUC (0-?) Plazmoje buvo maždaug 43% didesnis, palyginti su ne Rytų Azijos pacientais. ITP sergančių vaikų AUC plazmoje padidėjo maždaug 25%. "Eltrombopago AUC (0-?) lyginant su pacientais vyrais.
Farmakokinetiniai eltrombopago parametrai vaikams, sergantiems ITP, pateikti 10 lentelėje.
10 lentelė. Eltrombopago koncentracijos plazmoje pusiausvyrinės koncentracijos geometrinis vidurkis (95% PI) vaikams, kuriems taikoma ITP (50 mg kartą per parą)
Duomenys pateikti kaip geometrinis vidurkis (95% PI). AUC (0-?) Ir Cmax yra pagrįsti post hoc populiacijos farmakokinetikos įvertinimais.
05.3 Ikiklinikinių saugumo duomenys
Eltrombopagas neskatina trombocitų gamybos pelėms, žiurkėms ar šunims dėl unikalių TPO receptorių specifiškumo. Todėl iš šių gyvūnų gauti duomenys nėra išsamus modelis, leidžiantis įvertinti galimą su farmakologija susijusį eltrombopago poveikį žmonėms, įskaitant reprodukcijos ir kancerogeniškumo tyrimai.
Graužikams buvo nustatyta su gydymu susijusi katarakta, kuri priklausė nuo dozės ir laiko. Kai ekspozicija didesnė nei 6 kartus didesnė už klinikinę žmogaus ekspoziciją suaugusiems ITP sergantiems pacientams, vartojant 75 mg per parą dozę, ir esant ekspozicijai, 3 kartus didesnė už klinikinę ekspoziciją žmonėms, vartojantiems 100 mg per parą HCV infekuotiems suaugusiems pacientams, ekspozicija buvo pagrįsta AUC, katarakta pastebėta pelėms po 6 savaičių, o žiurkėms - po 28 gydymo savaičių. Esant ekspozicijai, kuri yra didesnė arba lygi 4 kartus didesnė už klinikinę ekspoziciją žmogui, skiriant ITP sergančius pacientus, vartojant 75 mg paros dozę, ir ekspoziciją, 2 kartus didesnę už žmogaus klinikinę ekspoziciją sergant HCV pacientų, vartojusių 100 mg paros dozę, ekspozicija, pagrįsta AUC, katarakta, pastebėta pelėms po 13 savaičių ir žiurkėms po 39 gydymo savaičių. Vartojant netoleruojamas dozes jaunoms žiurkėms, kurios buvo nujunkytos prieš atjunkymą, skiriant nuo 4 iki 32 dienos (maždaug 2 žmogaus metai dozavimo laikotarpio pabaigoje), pastebėtas akių drumstumas (histologija neatlikta), skiriant vienodas 75 mg paros dozes. 9 kartus didesnė už didžiausią žmogaus klinikinę ekspoziciją vaikams, sergantiems ITP, remiantis AUC. Tačiau žiurkių jaunikliams kataraktos nepastebėta, skiriant toleruojamas dozes, 5 kartus didesnes už klinikinę ekspoziciją žmonėms, sergantiems ITP vaikams, remiantis AUC.Suaugusiems šunims po 52 gydymo savaičių kataraktos nepastebėta (2 kartus didesnė už klinikinę žmogaus ekspoziciją suaugusiems ar vaikams ITP sergantiems pacientams, vartojant 75 mg paros dozę ir atitinkančią klinikinę žmogaus ekspoziciją infekuotiems pacientams. mg per parą, ekspozicija, pagrįsta AUC).
Atliekant tyrimus su pelėmis ir žiurkėmis iki 14 dienų, toksinis poveikis inkstų kanalėlėms buvo pastebėtas, kai ekspozicija paprastai buvo susijusi su sergamumu ir mirtingumu. Toksiškumas vamzdeliams taip pat buvo pastebėtas per 2 metus trukusį pelių kancerogeniškumo tyrimą, skiriant 25, 75 ir 150 mg / kg per parą dozes. Mažesnėmis dozėmis poveikis buvo silpnesnis ir jam būdingi įvairūs regeneraciniai pakeitimai. Ekspozicija, vartojant mažiausią dozę, buvo 1,2 arba 0,8 karto didesnė už klinikinę ekspoziciją žmogui, remiantis suaugusiųjų ar vaikų ITP sergančių vaikų AUC, vartojant 75 mg per parą, ir 0,6 karto didesnė už klinikinę žmogaus ekspoziciją HCV sergantiems pacientams, vartojant 100 mg per parą dozę, ekspozicija Remiantis AUC. Poveikis inkstams nebuvo pastebėtas žiurkėms po 28 savaičių arba šuniui po 52 savaičių, kai ekspozicija buvo 4 ir 2 kartus didesnė už klinikinę ekspoziciją žmonėms. vartojant ITP 75 mg per parą dozę ir 2 kartus didesnę ekspoziciją ir lygiavertę klinikinei ekspozicijai žmonėms, sergantiems HCV 100 mg per parą doze, ekspozicija pagrįsta AUC.
Kepenų ląstelių degeneracija ir (arba) nekrozė, dažnai lydima padidėjusio kepenų fermentų kiekio serume, buvo pastebėta pelėms, žiurkėms ir šunims, vartojant dozes, kurios buvo susijusios su sergamumu ir mirtingumu arba buvo blogai toleruojamos. Po lėtinio gydymo žiurkėms (28 savaitės) ir šunims (52 savaitės) poveikio kepenims nepastebėta, kai ekspozicija buvo 4 ar 2 kartus didesnė už klinikinę ekspoziciją žmonėms, sergantiems ITP, ir ekspozicija 3 ar 2 kartus didesnė už klinikinę ekspoziciją žmonėms. 75 mg per parą dozę ir 2 kartus arba lygiavertę klinikinei žmogaus ekspozicijai HCV infekuotiems pacientams, vartojantiems 100 mg per parą, ekspozicija pagrįsta AUC.
Trumpalaikių tyrimų metu, kai žiurkėms ir šunims buvo blogai toleruojamos dozės (ekspozicija didesnė nei 10 ar 7 kartus didesnė už klinikinę ekspoziciją žmonėms suaugusiems ar vaikams ITP sergantiems pacientams, vartojant 75 mg per parą dozę ir ekspoziciją daugiau nei 4 kartus l pastebėta 100 mg paros dozė HCV infekuotiems pacientams, ekspozicija pagrįsta AUC), sumažėjęs retikulocitų skaičius ir kaulų čiulpų (tik žiurkių) regeneracinė eritroidinė hiperplazija. Pastebimas poveikis raudonųjų kraujo kūnelių ar retikulocitų masės skaičiui iki 28 savaičių žiurkėms, 52 savaites šunims ir 2 metus pelėms ar žiurkėms, vartojant maksimaliai toleruojamas dozes, kurios atitinka 2–4 kartus didesnę žmogaus klinikinę ekspoziciją suaugusiems ar vaikams ITP sergantiems pacientams, vartojant 75 mg per parą dozę. ir esant ekspozicijai, mažesnei nei 2 kartus didesnė už klinikinę žmogaus ekspoziciją HCV infekuotiems pacientams, vartojant 100 mg per parą dozę, jonų, pagrįstų AUC.
Endostealinė hiperostozė pastebėta 28 savaičių toksiškumo tyrime su žiurkėmis, kai netoleruojama 60 mg / kg per parą dozė (6 kartus arba 4 kartus didesnė už klinikinę ekspoziciją žmonėms suaugusiems ar vaikams ITP sergantiems pacientams, vartojant 75 mg per parą ir 3 dozes). kartų didesnė už klinikinę žmogaus ekspoziciją HCV užsikrėtusiems pacientams, vartojant 100 mg per parą dozę, ekspozicija pagrįsta AUC suaugusiems ar vaikams ITP sergantiems pacientams, vartojantiems 75 mg per parą dozę ir 2 kartus didesnę už klinikinę ekspoziciją žmonėms, sergantiems HCV, vartojant 100 mg per parą dozę, ekspozicija pagrįsta AUC.
Eltrombopagas nebuvo kancerogeninis pelėms, skiriant iki 75 mg / kg per parą, arba žiurkėms, vartojant iki 40 mg / kg per parą (ekspozicija iki 4 ar 2 kartus didesnė už klinikinę ekspoziciją žmonėms suaugusiems ar vaikams, sergantiems ITP, kai 75 mg per parą dozė ir 2 kartus didesnė už klinikinę žmogaus ekspoziciją HCV užsikrėtusiems pacientams, vartojant 100 mg per parą dozę, ekspozicija pagrįsta AUC). Eltrombopagas nebuvo mutageniškas ar klastogeniškas atliekant bakterijų mutaciją arba atliekant du tyrimus. in vivo žiurkėms (mikrobranduoliai ir neplanuota DNR sintezė, 10 ar 8 kartus didesnė už klinikinę žmogaus ekspoziciją suaugusiems ar vaikams ITP sergantiems pacientams, vartojant 75 mg per parą dozę ir 7 kartus didesnę už klinikinę žmogaus ekspoziciją pacientams, sergantiems HCV infekcija, vartojant 100 dozę mg per parą, ekspozicijos, pagrįstos Cmax). Bandyme in vitro pelių limfomos atveju eltrombopagas buvo nežymiai teigiamas (padidėjo mutacijos). Šie pastebėjimai in vitro Ir in vivo rodo, kad eltrombopagas nekelia genotoksinio pavojaus žmonėms.
Eltrombopagas nedaro įtakos žiurkių patelių vaisingumui, ankstyvam embriono vystymuisi ar embriono ir vaisiaus vystymuisi, kai vartojama iki 20 mg / kg per parą dozė (2 kartus didesnė už klinikinę ekspoziciją suaugusiems ar paaugliams (12–17 metų), vartojantiems ITP). 75 mg per parą ir lygiavertė klinikinei žmogaus ekspozicijai pacientams, sergantiems HCV infekcija, vartojant 100 mg per parą dozę (ekspozicija pagrįsta AUC). Be to, poveikio triušiams embriono ir vaisiaus vystymuisi nebuvo, skiriant iki 150 mg / kg per parą dozes, didžiausia tirta dozė (0,3–0,5 karto didesnė už klinikinę žmogaus ekspoziciją ITP sergantiems pacientams, vartojant 75 mg per parą ir HCV) -užsikrėtę pacientai, vartojantys 100 mg per parą dozę, ekspozicija pagrįsta AUC mg per parą, ekspozicija, pagrįsta AUC), gydymas eltrombopagu buvo susijęs su embriono mirtingumu (padidėjusiu nuostoliu prieš ir po implantacijos), sumažėjusiu vaisiaus kūno svoriu ir nėščios gimdos svoriu moterų vaisingumo tyrime ir mažu gimdos kaklelio dažniu. embriono ir vaisiaus vystymosi tyrimas Eltrombopagą nėštumo metu galima vartoti tik tuo atveju, jei laukiama nauda pateisina galimą pavojų vaisiui (žr. 4.6 skyrių). Eltrombopagas neturėjo įtakos žiurkių patinų vaisingumui, kai buvo skiriama iki 40 mg / kg per parą dozė, didžiausia tirta dozė (3 kartus didesnė už klinikinę ekspoziciją žmogui, skiriant ITP sergantiems pacientams, vartojant 75 mg per parą, ir 2 kartus didesnė už žmogaus klinikinę ekspoziciją HCV infekuotiems pacientams. 100 mg paros dozė, ekspozicija pagrįsta AUC mg / kg per parą) ir neturi įtakos palikuonių augimui, vystymuisi, neurologiniam elgesiui ar reprodukcinei funkcijai (F1).
Eltrombopagas buvo aptiktas visų F1 žiurkių palikuonių plazmoje per visą 22 valandų mėginių ėmimo laikotarpį po vaisto skyrimo F0 motinoms, o tai rodo, kad naujagimių žiurkių eksprombopagas buvo veikiamas laktacijos metu.
Švietimas in vitro vartojant eltrombopagą, galima fototoksiškumo rizika; tačiau graužikams nepastebėta odos fototoksiškumo požymių (10 ar 7 kartus didesnė už klinikinę ekspoziciją suaugusiems ar vaikams ITP sergantiems žmonėms, vartojantiems 75 mg per parą ir 5 kartus didesnę už klinikinę ekspoziciją žmonėms, sergantiems HCV infekcija, skiriant 100 mg / d. ekspozicija, pagrįsta AUC) arba akies fototoksiškumu (ekspozicija, didesnė nei 4 kartus didesnė už klinikinę žmogaus ekspoziciją suaugusiems ar vaikams, kuriems ITP skiriama 75 mg per parą dozė ir 3 kartus didesnė už žmogaus klinikinę ekspoziciją HCV infekuotiems pacientams, vartojant 100 dozių mg per parą, ekspozicija, pagrįsta AUC). Be to, klinikinis farmakologinis tyrimas, kuriame dalyvavo 36 tiriamieji, neparodė jokių įrodymų, kad padidėjęs jautrumas šviesai padidėtų pavartojus 75 mg eltrombopago. Tai buvo matuojama pagal uždelstą fototoksiškumo indeksą, tačiau negalima atmesti galimos fotoalergijos rizikos, nes negalima atlikti specifinių ikiklinikinių tyrimų.
Duomenų su žiurkių jaunikliais, rodančių didesnę toksiškumo riziką gydant eltrombopagą vaikams, nėra nei suaugusiesiems, sergantiems ITP.
06.0 FARMACINĖ INFORMACIJA
06.1 Pagalbinės medžiagos
Revolade 12,5 mg plėvele dengtos tabletės
Planšetės šerdis
Magnio stearatas
Manitolis (E421)
Mikrokristalinė celiuliozė
Povidonas (K30)
Natrio krakmolo glikolatas
Tabletės danga
Hipromeliozė
Makrogolis 400
Polisorbatas 80
Titano dioksidas (E171)
Revolade 25 mg plėvele dengtos tabletės
Planšetės šerdis
Magnio stearatas
Manitolis (E421)
Mikrokristalinė celiuliozė
Povidonas
Natrio krakmolo glikolatas
Tabletės danga
Hipromeliozė
Makrogolis 400
Polisorbatas 80
Titano dioksidas (E171)
Revolade 50 mg plėvele dengtos tabletės
Planšetės šerdis
Magnio stearatas
Manitolis (E421)
Mikrokristalinė celiuliozė
Povidonas
Natrio krakmolo glikolatas
Tabletės danga
Hipromeliozė
Raudonasis geležies oksidas (E172)
Geltonasis geležies oksidas (E172)
Makrogolis 400
Titano dioksidas (E171)
Revolade 75 mg plėvele dengtos tabletės
Planšetės šerdis
Magnio stearatas
Manitolis (E421)
Mikrokristalinė celiuliozė
Povidonas
Natrio krakmolo glikolatas
Tabletės danga
Hipromeliozė
Raudonasis geležies oksidas (E172)
Juodasis geležies oksidas (E172)
Makrogolis 400
Titano dioksidas (E171)
06.2 Nesuderinamumas
Nėra svarbus.
06.3 Galiojimo laikas
4 metai.
06.4 Specialios laikymo sąlygos
Šiam vaistui specialių laikymo sąlygų nereikia.
06.5 Pirminės pakuotės pobūdis ir pakuotės turinys
Plėvele dengtos tabletės
Aliuminio lizdinės plokštelės (PA / Alu / PVC / Alu) pakuotėje, kurioje yra 14 arba 28 plėvele dengtos tabletės, ir sudėtinėje pakuotėje, kurioje yra 84 (3 pakuotės po 28) plėvele dengtų tablečių.
Gali būti tiekiamos ne visų dydžių pakuotės.
06.6 Naudojimo ir naudojimo instrukcijos
Nepanaudotą vaistą ir jo atliekas reikia sunaikinti laikantis vietinių taisyklių.
07.0 RINKODAROS TEISĖS TURĖTOJAS
„Novartis Europharm Limited“
„Frimley“ verslo parkas
„Camberley GU16 7SR“
JK
08.0 RINKODAROS TEISĖS NUMERIS
Revolade 12,5 mg plėvele dengtos tabletės
EU/1/10/612/010
039827100
EU/1/10/612/011
039827112
EU/1/10/612/012
039827124
Revolade 25 mg plėvele dengtos tabletės
EU/1/10/612/001
039827011
EU/1/10/612/002
039827023
EU/1/10/612/003
039827035
Revolade 50 mg plėvele dengtos tabletės
EU/1/10/612/004
039827047
EU/1/10/612/005
039827050
EU/1/10/612/006
039827062
Revolade 75 mg plėvele dengtos tabletės
EU/1/10/612/007
039827074
EU/1/10/612/008
039827086
EU/1/10/612/009
039827098
09.0 RINKODAROS TEISĖS SUTEIKIMO AR PATVIRTINIMO DATA
Registravimo data: 2010 m. Kovo 11 d
Paskutinio atnaujinimo data: 2015 m. Sausio 15 d
10.0 TEKSTO PERŽIŪROS DATA
2016 lapkritis