Veikliosios medžiagos: dabigatranas (dabigatrano eteksilatas)
Pradaxa 150 mg kietos kapsulės
Galima įsigyti „Pradaxa“ pakuotės lapelių dydžių:- Pradaxa 75 mg kietos kapsulės
- Pradaxa 110 mg kietos kapsulės
- Pradaxa 150 mg kietos kapsulės
Kodėl vartojamas Pradaxa? Kam tai?
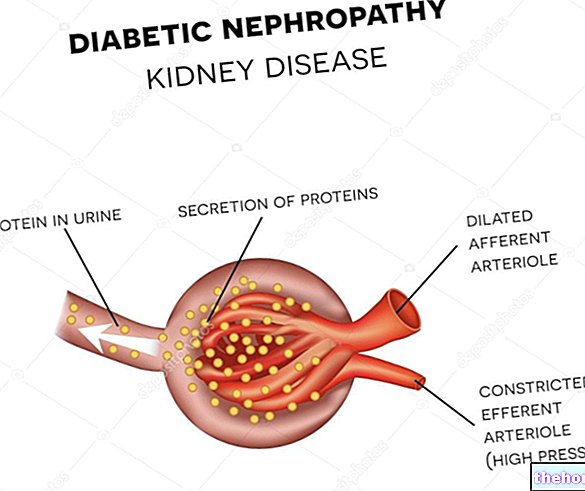
Pradaxa yra vaistas, kurio sudėtyje yra veikliosios medžiagos dabigatrano eteksilato. Jis blokuoja medžiagos, veikiančios kraujo krešuliuose, veikimą organizme.
Pradaxa yra vaistas, vartojamas suaugusiems pacientams, kuriems yra pakitęs širdies plakimas (prieširdžių virpėjimas) ir kuriems yra papildomų rizikos veiksnių, siekiant sumažinti smegenų ar likusio kūno kraujagyslių, užsikimšusių kraujo krešuliais, riziką. Pradaxa yra vaistas, kuris skystina kraują ir mažina kraujo krešulių riziką.
Pradaxa yra vaistas, vartojamas kraujo krešuliams kojų ir plaučių venose gydyti ir neleisti kraujo krešuliams atsinaujinti kojų ir plaučių venose.
Kontraindikacijos Pradaxa vartoti negalima
Pradaxa vartoti negalima
- jeigu yra alergija dabigatrano eteksilatui arba bet kuriai pagalbinei šio vaisto medžiagai (jos išvardytos 6 skyriuje).
- jeigu labai sutrikusi Jūsų inkstų funkcija
- jeigu nuolat kraujuojate.
- jeigu pažeistas organas, dėl kurio padidėja sunkaus kraujavimo rizika.
- jeigu yra padidėjęs polinkis į kraujavimą.Tai gali būti įgimta, dėl nežinomos priežasties arba dėl kitų vaistų.
- jeigu yra labai susilpnėjusi kepenų funkcija arba kepenų liga, kuri tam tikru būdu gali sukelti mirtį.
- jeigu per burną vartojate ketokonazolą arba itrakonazolą - vaistus grybelinėms infekcijoms gydyti.
- jeigu vartojate ciklosporiną - vaistą, kuris apsaugo nuo atmetimo epizodų po organų transplantacijos.
- jeigu vartojate dronedaroną - vaistą, skirtą nereguliaraus širdies plakimo problemai atsinaujinti.
- jeigu vartojate kraujo krešulių prevencijai skirtus vaistus (pvz., varfariną, rivaroksabaną, apiksabaną ar hepariną), išskyrus tuos atvejus, kai pereinate nuo vieno antikoagulianto gydymo prie kito arba kai įdedamas arterinis veninis kateteris ir per jį imate heparino, kad jis būtų atidarytas.
- jeigu Jums buvo implantuotas dirbtinis širdies vožtuvas.
Atsargumo priemonės Vartojant prieš vartojant Pradaxa
Pasitarkite su gydytoju, prieš pradėdami vartoti Pradaxa. Gydymo Pradaxa metu taip pat gali tekti kreiptis į gydytoją, jei atsiranda simptomų arba jums reikia operuoti. Pasakykite gydytojui, jei sergate ar sirgote bet kokia sveikatos būkle ar liga, ypač bet kuria iš šių, įtrauktų į šį sąrašą:
- jeigu sergate kepenų liga, susijusi su nenormaliais kraujo tyrimais, Pradaxa vartoti nerekomenduojama.
- jeigu yra padidėjusi kraujavimo rizika, nes tai gali būti šiose situacijose:
- jeigu neseniai kraujavote.
- jeigu praėjusį mėnesį jums buvo atlikta biopsija (chirurginis audinio pašalinimas).
- jeigu patyrėte sunkių sužalojimų (pvz., kaulų lūžių, galvos traumų ar bet kokių sužalojimų, kuriems prireikė operacijos).
- jeigu sergate stemplės ar skrandžio uždegimu.
- jeigu turite problemų su skrandžio sulčių refliuksu į stemplę.
- jeigu vartojote vaistų, galinčių padidinti kraujavimo riziką, pvz., aspirino (acetilsalicilo rūgšties), klopidogrelio, tikagreloro.
- jeigu vartojate priešuždegiminių vaistų, tokių kaip diklofenakas, ibuprofenas, piroksikamas.
- jeigu sergate širdies infekcija (bakteriniu endokarditu).
- jeigu žinote, kad Jūsų inkstų funkcija sutrikusi arba kenčiate nuo dehidratacijos (simptomai yra troškulys ir šlapinimasis sumažėjus tamsaus (koncentruoto) šlapimo kiekiui).
- jeigu esate vyresnis nei 75 metų.
- jei jis sveria 50 kg ar mažiau.
- jeigu sirgote širdies priepuoliu arba jums buvo diagnozuotos sąlygos, kurios padidina riziką susirgti širdies priepuoliu.
- jeigu Jums atliekama planinė operacija. Dėl padidėjusios kraujavimo rizikos operacijos metu ir netrukus po jos Pradaxa vartojimą reikia laikinai nutraukti. Jei įmanoma, Pradaxa vartojimą reikia nutraukti likus ne mažiau kaip 24 valandoms iki operacijos. Pacientams, kuriems yra padidėjusi kraujavimo rizika, gydytojas gali nuspręsti nutraukti gydymą anksčiau.
- jeigu Jums atliekama neplanuota operacija. Jei įmanoma, operaciją reikia atidėti 12 valandų po paskutinės Pradaxa dozės. Jei operacijos negalima atidėti, gali padidėti kraujavimo rizika. Gydytojas įvertins kraujavimo riziką ir operacijos skubumą.
- jei į nugarą įkištas vamzdelis (kateteris): vamzdelį galima įkišti į nugarą, pvz. operacijos metu arba po jos, jei norite skirti anestetikų ar skausmą malšinančių vaistų.
- jei gydymo metu nukritote ar susižalojote, ypač jei patyrėte smūgį į galvą, nedelsdami kreipkitės į gydytoją. Jūsų gydytojui gali prireikti jus aplankyti, nes jums gali būti didelė kraujavimo rizika.
Vaikai ir paaugliai
Pradaxa negalima vartoti vaikams ir paaugliams iki 18 metų.
Sąveika Kokie vaistai ar maistas gali pakeisti Pradaxa poveikį
Jeigu vartojate arba neseniai vartojote kitų vaistų arba dėl to nesate tikri, apie tai pasakykite gydytojui arba vaistininkui. Pvz .:
- Vaistai, mažinantys kraujo krešėjimą (pvz., Varfarinas, fenprokumonas, heparinas, klopidogrelis, prasugrelis, tikagreloras, rivaroksabanas)
- Priešuždegiminiai ir skausmą malšinantys vaistai (pvz., Aspirinas)
- Jonažolė, vaistažolių preparatas depresijai gydyti
- Antidepresantai, vadinami selektyviais serotonino reabsorbcijos inhibitoriais arba selektyviais serotonino-norepinefrino reabsorbcijos inhibitoriais
- Rifampicinas arba klaritromicinas, du antibiotikai
- Vaistai pakitusiam širdies plakimui gydyti (pvz., Amiodaronas, dronedaronas, chinidinas, verapamilis). Jei vartojate vaistinių preparatų, kurių sudėtyje yra verapamilio, reikia vartoti mažesnę Pradaxa dozę-220 mg, vartojamą po vieną 110 mg kapsulę du kartus per parą, nes gali padidėti kraujavimo rizika. Pradaxa ir verapamilio turinčius vaistus reikia vartoti kartu.
- Vaistai grybelinėms infekcijoms gydyti (pvz., Ketokonazolas, itrakonazolas, posakonazolas), nebent tepami tik ant odos
- Vaistai, skirti išvengti tiesioginių epizodų po organų transplantacijos (pvz., Takrolimuzas, ciklosporinas)
- Virusiniai vaistai nuo AIDS (pvz., Ritonaviras)
- Vaistai epilepsijai gydyti (pvz., Karbamazepinas, fenitoinas)
Įspėjimai Svarbu žinoti, kad:
Nėštumas ir žindymo laikotarpis
Pradaxa poveikis nėštumui ir vaisiui nėra žinomas. Jei esate nėščia, Pradaxa vartoti negalima, nebent gydytojas pasakys, kad tai saugu. Jei esate vaisingo amžiaus moteris, gydymo Pradaxa metu turite vengti pastoti.
Gydymo Pradaxa metu žindyti negalima.
Vairavimas ir mechanizmų valdymas
Pradaxa poveikio gebėjimui vairuoti ir valdyti mechanizmus neveikia.
Pradaxa sudėtyje yra saulėlydžio geltonos spalvos (E110)
Šio vaisto sudėtyje yra dažų, vadinamų saulėlydžio geltonaisiais (E110), kurie gali sukelti alergines reakcijas
Dozė, vartojimo būdas ir laikas Kaip vartoti Pradaxa: Dozavimas
Visada vartokite šį vaistą tiksliai kaip nurodė gydytojas. Jei abejojate, pasitarkite su gydytoju.
Vartokite Pradaxa, kaip rekomenduojama, esant šioms sąlygoms:
Kraujo krešulių susidarymo prevencija po kelio ar klubo sąnario pakeitimo operacijos
Rekomenduojama dozė yra 300 mg vieną kartą per parą (išgeriama po 2 kapsules po 150 mg).
Jei inkstų funkcija susilpnėjusi daugiau nei per pusę arba esate 75 metų ar vyresnė, rekomenduojama dozė yra 220 mg, vartojama po vieną 110 mg kapsulę du kartus per parą.
Jei vartojate vaistų, kurių sudėtyje yra verapamilio, turite išgerti mažesnę Pradaxa dozę-220 mg, vartojamą po vieną 110 mg kapsulę du kartus per parą, nes gali padidėti kraujavimo rizika.
Jei Jums yra padidėjusi kraujavimo rizika, gydytojas gali nuspręsti skirti 220 mg Pradaxa dozę, vartojamą po vieną 110 mg kapsulę du kartus per parą.
Pradaxa galima vartoti valgant arba nevalgius. Norint užtikrinti skrandžio išsiskyrimą, kapsulę reikia nuryti visą, užgeriant stikline vandens. Nesulaužykite, nekramtykite ir nepaimkite kapsulių iš kapsulės, nes tai gali padidinti kraujavimo riziką.
Naudodami „Pradaxa“ supakuotas į lizdines plokšteles, laikykitės šių nurodymų
- išimkite kapsules iš lizdinės plokštelės, pakeldami ant nugaros esančią aliuminio foliją.
- nespauskite kapsulių per lizdinę plokštelę.
- aliuminio foliją iš lizdinės plokštelės galima pakelti tik tada, kai reikia išimti kapsulę.
Naudodami buteliuke supakuotą Pradaxa, laikykitės šių nurodymų
- butelis atidaromas paspaudus ir pasukant dangtelį.
Gydymo antikoaguliantais pakeitimas
- Perėjimas nuo gydymo Pradaxa prie gydymo antikoaguliantais injekcijomis: nepradėkite gydymo injekciniais antikoaguliantais (pvz., Heparinu), kol nepraėjo 12 valandų nuo paskutinio Pradaxa vartojimo.
- Perėjimas nuo gydymo injekciniais antikoaguliantais prie gydymo Pradaxa: Pradėkite vartoti Pradaxa likus 2–2 valandoms iki kitos injekcijos.
- Gydymo Pradaxa keitimas į kraują skystinančius vaistus, kurių sudėtyje yra vitamino K antagonistų (pvz., Fenprokumono): gydytojas turėtų paprašyti atlikti kraujo tyrimus ir nurodyti, kada pradėti gydymą vitamino K antagonistais.
- Perėjimas nuo gydymo kraują skystinančiais vaistais, kurių sudėtyje yra vitamino K antagonistų (pvz., Fenprokumono), į gydymą Pradaxa: Nustokite vartoti vaistų, kurių sudėtyje yra vitamino K antagonisto. Gydytojas turėtų paprašyti atlikti kraujo tyrimus ir pasakyti, kada pradėti gydymą Pradaxa.
Perdozavimas Ką daryti pavartojus per didelę Pradaxa dozę
Pavartojus per didelę Pradaxa dozę
Pavartojus per didelę Pradaxa dozę, gali padidėti kraujavimo rizika. Gydytojas gali atlikti kraujo tyrimą, kad įvertintų kraujavimo riziką.
Jei išgėrėte daugiau Pradaxa, nei nurodyta, nedelsdami pasakykite gydytojui. Jei atsiranda kraujavimo epizodas, gali prireikti operacijos ar gydymo kraujo perpylimu.
Pamiršus pavartoti Pradaxa
Praleistą dozę dar galima išgerti likus 6 valandoms iki kitos dozės.Jei iki kitos dozės liko mažiau nei 6 valandos, praleistą dozę reikia praleisti. Negalima vartoti dvigubos dozės norint kompensuoti praleistą dozę
Nustojus vartoti Pradaxa
Pradaxa vartokite tiksliai taip, kaip nurodyta. Nenustokite vartoti Pradaxa, prieš tai nepasitarę su gydytoju. Nutraukus Pradaxa vartojimą, gali padidėti kraujo krešulių susidarymo rizika pacientams, gydomiems po klubo ar kelio sąnario pakeitimo operacijos.
Jeigu kiltų daugiau klausimų dėl šio vaisto vartojimo, kreipkitės į gydytoją arba vaistininką.
Šalutinis poveikis Koks yra Pradaxa šalutinis poveikis
Šis vaistas, kaip ir visi kiti, gali sukelti šalutinį poveikį, nors jis pasireiškia ne visiems žmonėms.
Pradaxa veikia kraujo krešėjimo sistemą, todėl dauguma šalutinių poveikių yra susiję su tokiais požymiais kaip hematoma ar kraujavimas.
Gali pasireikšti didelis ar sunkus kraujavimas, tai yra pats rimčiausias šalutinis poveikis, kuris, nepaisant vietos, gali būti neįgalus, pavojingas gyvybei ar net sukelti mirtį. Kai kuriais atvejais šis kraujavimas gali būti nepastebimas.
Jei atsiranda kraujavimas, kuris savaime neišnyksta, arba pastebite per didelio kraujavimo simptomus (išskirtinis silpnumas, nuovargis, blyški oda, galvos svaigimas, galvos skausmas ar nepaaiškinamas patinimas), nedelsdami kreipkitės į gydytoją.
Gydytojas gali nuspręsti atidžiai jus patikrinti arba pakeisti gydymą.
Nedelsdami pasakykite gydytojui, jei pasireiškė sunki alerginė reakcija, sukelianti kvėpavimo pasunkėjimą ar galvos svaigimą.
Šalutinis poveikis išvardytas žemiau, sugrupuotas pagal jų pasireiškimo dažnumą.
Smegenų ar likusio kūno kraujagyslių užsikimšimo prevencija dėl kraujo krešulių susidarymo dėl pakitusio širdies plakimo
Dažnas (gali pasireikšti ne daugiau kaip 1 iš 10 žmonių):
- Kraujavimas iš nosies, skrandžio ar žarnyno, varpos / makšties ar šlapimo takų (įskaitant kraują šlapime, dėl kurio jis tampa rausvas arba raudonas) arba po oda
- Raudonųjų kraujo kūnelių kiekio kraujyje sumažėjimas
- Skausmas pilve ar skrandyje
- Nevirškinimas
- Viduriavimas su prastai suformuotomis ar skystomis išmatomis
- Bloga savijauta
Nedažnas (gali pasireikšti ne daugiau kaip 1 iš 100 žmonių):
- Kraujavimas
- Kraujavimas iš hemorojaus, į tiesiąją žarną ar smegenis
- Hematomos susidarymas
- Kraujo ar kraujo spalvos skreplių atsikosėjimas
- Trombocitų kiekio kraujyje sumažėjimas
- Sumažėjęs hemoglobino kiekis kraujyje (medžiaga, esanti raudonosiose kraujo ląstelėse)
- Alerginė reakcija
- Staigus odos pakitimas, dėl kurio pasikeičia jos spalva ir išvaizda
- Niežėjimas
- Virškinimo trakto opa (įskaitant stemplės opą)
- Stemplės ir skrandžio uždegimas
- Skrandžio sulčių refliuksas stemplėje
- Jis atsitraukė
- Sunku nuryti
- Nenormalūs kepenų funkcijos tyrimų rezultatai
Reti (gali pasireikšti ne daugiau kaip 1 iš 1 000 žmonių):
- Kraujavimas iš sąnario, iš chirurginio pjūvio, žaizdos, injekcijos vietos arba iš kateterio įvedimo į veną vietos - Sunki alerginė reakcija, sukelianti kvėpavimo pasunkėjimą ar galvos svaigimą. odos bėrimas, pastebimas dėl alerginės reakcijos atsiradusių tamsiai raudonų, patinusių, niežtinčių gumulėlių - sumažėjęs raudonųjų kraujo kūnelių kiekis - padidėjęs kepenų fermentų kiekis - odos arba akių baltymų pageltimas dėl kepenų ar kraujo sutrikimų
Dažnis nežinomas (negali būti įvertintas pagal turimus duomenis):
- Pasunkėjęs kvėpavimas ar švokštimas
Kraujo krešulių gydymas kojų ir plaučių venose, įskaitant kraujo krešulių susidarymo kojų ir (arba) plaučiuose prevenciją
Dažnas (gali pasireikšti ne daugiau kaip 1 iš 10 žmonių):
- Kraujavimas iš nosies, skrandžio ar žarnyno, tiesiosios žarnos, varpos / makšties ar šlapimo takų (įskaitant kraują šlapime, dėl kurio jis tampa rausvas arba raudonas) arba po oda
- Nevirškinimas
Nedažnas (gali pasireikšti ne daugiau kaip 1 iš 100 žmonių):
- Kraujavimas
- Kraujavimas, kuris gali atsirasti sąnaryje iš žaizdos
- Kraujavimas, kurį gali sukelti hemorojus
- Raudonųjų kraujo kūnelių kiekio kraujyje sumažėjimas
- Hematomos susidarymas
- Kraujo ar krauju išmargintų skreplių atsikosėjimas
- Alerginė reakcija
- Staigus odos pakitimas, dėl kurio pasikeičia jos spalva ir išvaizda
- Niežėjimas
- Virškinimo trakto opa
- Stemplės ir skrandžio uždegimas
- Skrandžio sulčių refliuksas stemplėje
- Bloga savijauta
- Jis atsitraukė
- Skausmas pilve ar skrandyje
- Viduriavimas su prastai suformuotomis ar skystomis išmatomis
- Sunku nuryti
- Nenormalūs kepenų funkcijos tyrimų rezultatai
- Padidėjęs kepenų fermentų kiekis
Reti (gali pasireikšti ne daugiau kaip 1 iš 1 000 žmonių):
- Kraujavimas, kuris gali atsirasti dėl „chirurginio pjūvio arba injekcijos vietos arba iš kateterio įvedimo į veną ar iš smegenų vietos“
- Trombocitų kiekio kraujyje sumažėjimas
- Sunki alerginė reakcija, sukelianti kvėpavimo pasunkėjimą ar galvos svaigimą
- Sunki alerginė reakcija, sukelianti veido ar gerklės patinimą
- Pastebimas odos bėrimas su alerginės reakcijos sukeltomis tamsiai raudonomis, patinusiomis, niežtinčiomis gumulėlėmis
- Sunku nuryti
- Raudonųjų kraujo kūnelių kiekio kraujyje sumažėjimas
Dažnis nežinomas (negali būti įvertintas pagal turimus duomenis):
- Pasunkėjęs kvėpavimas ar švokštimas
- Hemoglobino kiekio kraujyje sumažėjimas (raudonųjų kraujo kūnelių sudėtyje esanti medžiaga)
- Raudonųjų kraujo kūnelių kiekio kraujyje sumažėjimas
- Odos ar akių baltymų pageltimas dėl kepenų ar kraujo sutrikimų
Pranešimas apie šalutinį poveikį
Jeigu pasireiškė šalutinis poveikis (net jeigu jis šiame lapelyje nenurodytas), kreipkitės į gydytoją arba vaistininką. Apie šalutinį poveikį taip pat galite pranešti tiesiogiai naudodamiesi nacionaline pranešimo sistema. Daugiau informacijos apie šio vaisto saugumą.
Klinikinio tyrimo metu širdies priepuolių dažnis buvo didesnis vartojant Pradaxa nei vartojant varfariną. Bendras dažnis buvo mažas.
Galiojimo laikas ir išlaikymas
Šį vaistą laikykite vaikams nepastebimoje ir nepasiekiamoje vietoje.
Ant dėžutės, lizdinės plokštelės ar buteliuko po „Tinka iki“ nurodytam tinkamumo laikui pasibaigus, šio vaisto vartoti negalima. Vaistas tinkamas vartoti iki paskutinės nurodyto mėnesio dienos.
Lizdinės plokštelės: Laikyti gamintojo pakuotėje, kad preparatas būtų apsaugotas nuo drėgmės.
Buteliukas: atidarius vaistą, jis turi būti suvartotas per 4 mėnesius. Buteliuką laikyti sandariai uždarytą. Laikyti gamintojo pakuotėje, kad preparatas būtų apsaugotas nuo drėgmės.
Nemeskite vaistų į kanalizaciją ar buitines atliekas. Paklauskite vaistininko, kaip išmesti nebenaudojamus vaistus. Tai padės apsaugoti aplinką.
Sudėtis ir farmacinė forma
Pradaxa sudėtis
- Veiklioji medžiaga yra dabigatranas, vartojamas 150 mg dabigatrano eteksilato pavidalu kaip dabigatrano eteksilato mezilatas.
- Pagalbinės medžiagos yra vyno rūgštis, arabų guma, hipromeliozė, dimetikonas 350, talkas ir hidroksipropilceliuliozė.
- Kapsulės apvalkale yra karagino, kalio chlorido, titano dioksido, indigo karmino, saulėlydžio geltonojo (E110), hipromeliozės ir išgryninto vandens.
- Juodo spausdinimo rašalo sudėtyje yra šelako, N-butilo alkoholio, izopropilo alkoholio, pramoninio denatūruoto etanolio, juodojo geležies oksido, išgryninto vandens ir propilenglikolio.
Pradaxa išvaizda ir pakuotės turinys
Pradaxa yra kieta kapsulė.
Pradaxa 150 mg kietos kapsulės turi nepermatomą šviesiai mėlyną dangtelį ir nepermatomą kremo korpusą. Ant dangtelio yra atspausdintas „Boehringer Ingelheim“ logotipas, o ant kapsulės korpuso - kodas „R150“.
Pradaxa 150 mg kietos kapsulės tiekiamos pakuotėmis, kuriose yra 10x1, 30x1, 60x1 kietų kapsulių, daugybinėje pakuotėje, kurioje yra 3 pakuotės po 60x1 kietųjų kapsulių (180 kietų kapsulių), arba sudėtinėje pakuotėje, kurioje yra 2 pakuotės po 50x1 kietų kapsulių (100 kietų kapsulių). lizdinės plokštelės, dalijamos iš vienetinės dozės.
Pradaxa 150 mg kietos kapsulės taip pat tiekiamos pakuotėse, kuriose yra 60 x 1 kietos kapsulės baltose perforuotose vienadozėse aliuminio lizdinėse plokštelėse.
Pradaxa 150 mg kietos kapsulės taip pat tiekiamos polipropileno (plastiko) buteliukuose, kuriuose yra 60 kietų kapsulių.
Gali būti tiekiamos ne visų dydžių pakuotės
Šaltinio pakuotės lapelis: AIFA (Italijos vaistų agentūra). Turinys paskelbtas 2016 m. Sausio mėn. Pateikta informacija gali būti neatnaujinta.
Norint pasiekti naujausią versiją, patartina apsilankyti AIFA (Italijos vaistų agentūra) svetainėje. Atsisakymas ir naudinga informacija.
01.0 VAISTINIO PREPARATO PAVADINIMAS
PRADAXA 110 MG KIETOS KAPSULĖS
02.0 KOKYBINĖ IR KIEKYBINĖ SUDĖTIS
Kiekvienoje kietoje kapsulėje yra 110 mg dabigatrano eteksilato (mezilato pavidalu).
Pagalbinės medžiagos, kurių poveikis žinomas:
Kiekvienoje kietoje kapsulėje yra 3 mikrogramai saulėlydžio geltonos spalvos (E110).
Išsamų pagalbinių medžiagų sąrašą žr. 6.1 skyriuje.
03.0 FARMACINĖ FORMA
Kietoji kapsulė.
Kapsulės su nepermatomu šviesiai mėlynu dangteliu ir nepermatomu kremo korpusu, 1 dydžio, užpildytos gelsvomis granulėmis. Ant galvos atspausdintas „Boehringer Ingelheim“ logotipas, ant kūno - „R110“.
04.0 KLINIKINĖ INFORMACIJA
04.1 Terapinės indikacijos
Pirminė tromboembolijos epizodų prevencija suaugusiems pacientams, kuriems atliekama planinė klubo ar kelio sąnario keitimo operacija.
Insulto ir sisteminės embolijos prevencija suaugusiems pacientams, sergantiems ne vožtuvų prieširdžių virpėjimu (NVAF), turintiems vieną ar kelis rizikos veiksnius, pvz., Buvusį insultą ar praeinantį išemijos priepuolį (TIA); amžius ≥ 75 metai; širdies nepakankamumas (NYHA klasė ≥ II); cukrinis diabetas; hipertenzija.
Giliųjų venų trombozės (DVT) ir plaučių embolijos (PE) gydymas bei DVT ir PE pasikartojimo prevencija suaugusiesiems.
04.2 Dozavimas ir vartojimo metodas
Dozavimas
Pirminė venų tromboembolijos prevencija ortopedinėje chirurgijoje
Pacientai, kuriems atliekama planinė kelio sąnario keitimo operacija
Rekomenduojama Pradaxa dozė yra 220 mg vieną kartą per parą, išgeriama po 2 kapsules po 110 mg. Gydymas turi būti pradėtas per burną per 1–4 valandas po operacijos, naudojant vieną 110 mg kapsulę, ir kitą dieną tęsiama po 2 kapsules vieną kartą per parą, iš viso 10 dienų.
Pacientai, kuriems atliekama planinė klubo sąnario keitimo operacija
Rekomenduojama Pradaxa dozė yra 220 mg vieną kartą per parą, išgeriama po 2 kapsules po 110 mg. Gydymą reikia pradėti per burną per 1–4 valandas po operacijos, naudojant 110 mg kapsulę, ir tęsti nuo kitos dienos su 2 kapsulėmis vieną kartą per dieną, iš viso 28–35 dienas.
Šioms grupėms rekomenduojama Pradaxa paros dozė yra 150 mg vieną kartą per parą, išgeriant 2 kapsules po 75 mg.
Gydymas turi būti pradėtas per burną per 1–4 valandas po operacijos, naudojant vieną 75 mg kapsulę, ir tęsiama nuo kitos dienos, vartojant 2 kapsules vieną kartą per parą, iš viso 10 dienų (kelio sąnario keitimo operacija) arba 28 dienas. -35 dienos (klubo sąnario pakeitimas) chirurgija):
• Pacientai, kuriems yra vidutinio sunkumo inkstų funkcijos sutrikimas (kreatinino klirensas, CrCL 30-50 ml / min. [Žr.
• Pacientai, kartu vartojantys verapamilį, amiodaroną, chinidiną [žr.
• 75 metų ir vyresni pacientai [žr. Senyvi pacientai (pirminė venų tromboembolijos prevencija ortopedinėje chirurgijoje)]
Abiejų intervencijų atveju, jei hemostazė nėra normali, gydymo pradžią reikia atidėti. Jei gydymas nepradedamas operacijos dieną, jį reikia pradėti nuo 2 kapsulių vieną kartą per parą.
Inkstų funkcijos įvertinimas (pirminė venų tromboembolijos epizodų prevencija ortopedinėje chirurgijoje):
Visiems pacientams:
• Prieš pradedant gydyti Pradaxa, inkstų funkcija turi būti įvertinta apskaičiuojant kreatinino klirensą (CrCL), kad būtų pašalinti pacientai, kuriems yra sunkus inkstų funkcijos sutrikimas (ty CrCL).
• Inkstų funkcija taip pat turėtų būti įvertinta, kai gydymo metu įtariama sumažėjusi inkstų funkcija (pvz., Hipovolemija, dehidratacija ir tuo pat metu vartojant tam tikrus vaistinius preparatus).
Inkstų funkcijai įvertinti (CrCL ml / min.) Klinikinio Pradaxa vystymosi metu buvo taikomas Cockgroft-Gault metodas (žr. 75 mg Pradaxa 4.2 skyrių).
Specialios populiacijos
Inkstų funkcijos sutrikimas (pirminė venų tromboembolijos epizodų prevencija ortopedinėje chirurgijoje)
Pradaxa gydymas pacientams, kuriems yra sunkus inkstų funkcijos sutrikimas (CrCLr
Klinikinė patirtis pacientams, kuriems yra vidutinio sunkumo inkstų funkcijos sutrikimas (CrCL 30-50 ml / min.), Yra ribota. Šiuos pacientus reikia gydyti atsargiai. Rekomenduojama dozė yra 150 mg, vartojama vieną kartą per parą po 2 75 mg kapsules (žr. 4.4 ir 5.1 skyrius).
Pradaxa vartojimas kartu su silpnais ar vidutinio sunkumo P-glikoproteino (P-gp) inhibitoriais, tokiais kaip amiodaronas, chinidinas ar verapamilis (pirminė venų tromboembolijos profilaktika ortopedinėje chirurgijoje)
Pacientams, vartojantiems dabigatrano eteksilatą ir amiodaroną, chinidiną ar verapamilį, Pradaxa dozę reikia sumažinti iki 150 mg vieną kartą per parą po dvi 75 mg kapsules (žr. 4.4 ir 4.5 skyrius). Tokiu atveju Pradaxa ir šiuos vaistus reikia vartoti kartu.
Pacientams, kuriems yra vidutinio sunkumo inkstų funkcijos sutrikimas ir kurie kartu vartoja dabigatrano eteksilatą bei verapamilį, reikia apsvarstyti galimybę sumažinti Pradaxa dozę iki 75 mg per parą (žr. 4.4 ir 4.5 skyrius).
Senyvi žmonės (pirminė venų tromboembolijos epizodų prevencija ortopedinėje chirurgijoje)
Senyviems pacientams (> 75 metų) klinikinė patirtis yra ribota. Šiuos pacientus reikia gydyti atsargiai. Rekomenduojama dozė yra 150 mg, vartojama vieną kartą per parą, išgeriant dvi 75 mg kapsules (žr. 4.4 ir 5.1 skyrius).
Kadangi vyresnio amžiaus žmonėms (vyresniems nei 75 metų) inkstų funkcijos sutrikimas gali būti dažnas, prieš pradedant gydymą Pradaxa, inkstų funkcija turi būti įvertinta apskaičiuojant CrCL, kad neįtrauktų pacientų, kuriems yra sunkus inkstų funkcijos sutrikimas (t.
Kepenų funkcijos sutrikimas (pirminė venų tromboembolijos prevencija ortopedinėje chirurgijoje)
Pacientai, kurių kepenų fermentų koncentracija padidėjo daugiau nei dvigubai virš viršutinės normos ribos (VNR), nebuvo įtraukti į klinikinius tyrimus, kuriuose buvo vertinama VTE profilaktika po planinės viso klubo ar kelio sąnario pakeitimo operacijos. Nėra patirties gydant šią pacientų grupę, todėl šiai populiacijai Pradaxa vartoti nerekomenduojama (žr. 4.4 ir 5.2 skyrius). Jis yra kontraindikuotinas esant kepenų funkcijos sutrikimui ar kepenų ligai, kuri gali turėti įtakos išgyvenimui (žr. 4.3 skyrių).
Svoris (pirminė venų tromboembolijos prevencija ortopedinėje chirurgijoje)
Klinikinė patirtis vartojant rekomenduojamą dozę 110 kg sveriantiems pacientams yra labai ribota. Remiantis klinikiniais ir kinetiniais duomenimis, dozės koreguoti nereikia (žr. 5.2 skyrių), tačiau rekomenduojama atidžiai stebėti klinikinę būklę (žr. 4.4 skyrių).
Lytis (pirminė venų tromboembolijos epizodų prevencija ortopedinėje chirurgijoje)
Remiantis turimais klinikiniais ir kinetiniais duomenimis, dozės koreguoti nereikia (žr. 5.2 skyrių).
Keitimas (pirminė venų tromboembolijos epizodų prevencija ortopedinėje chirurgijoje)
Nuo gydymo Pradaxa iki parenteralinio antikoagulianto
Rekomenduojama palaukti 24 valandas po paskutinės dozės, prieš pradedant vartoti Pradaxa į parenteralinį antikoaguliantą (žr. 4.5 skyrių).
Nuo parenterinių antikoaguliantų iki Pradaxa
Nustokite vartoti parenterinį antikoaguliantą ir pradėkite dabigatrano eteksilatą likus 0–2 valandoms iki numatytos kitos pradinės terapijos dozės vartojimo arba nutraukus gydymą, jei gydymas tęsiamas (pvz., Į veną nefrakcionuotas heparinas (ENF)) (žr. 4.5 skyrių).
Vaikų populiacija (pirminė venų tromboembolijos epizodų prevencija ortopedinėje chirurgijoje)
Pradaxa nėra tinkamas vaikų populiacijai pagal indikaciją: pirminė venų tromboembolijos epizodų prevencija pacientams, kuriems atliekama planinė viso klubo sąnario pakeitimo operacija arba planinė viso kelio sąnario pakeitimo operacija.
Praleista dozė (pirminė venų tromboembolijos epizodų prevencija ortopedinėje chirurgijoje)
Likusias dabigatrano eteksilato paros dozes rekomenduojama tęsti kitos dienos tuo pačiu laiku.
Negalima dvigubinti dozių norint kompensuoti praleistą dozę.
Dozavimas (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu, DVT / PE)
Insulto ir ES profilaktika suaugusiems pacientams, sergantiems NVNU, turinčiais vieną ar daugiau rizikos veiksnių (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu)
Rekomenduojama Pradaxa paros dozė yra 300 mg, vartojama po vieną 150 mg kapsulę du kartus per parą. Terapija turi būti tęsiama ilgą laiką.
Giliųjų venų trombozės (DVT) ir plaučių embolijos (PE) gydymas bei DVT ir PE pasikartojimo prevencija suaugusiesiems (DVT / PE)
Rekomenduojama Pradaxa paros dozė yra 300 mg, vartojama po vieną 150 mg kapsulę du kartus per parą, mažiausiai 5 dienas gydant parenteriniu antikoaguliantu. Gydymo trukmė turi būti nustatyta atidžiai įvertinus gydymo naudą ir kraujavimo riziką (žr. 4.4 skyrių). Renkantis trumpalaikį gydymą (mažiausiai 3 mėnesius) reikia atsižvelgti į laikinus rizikos veiksnius (pvz. neseniai atlikta operacija, trauma, imobilizacija) ir ilgesnės trukmės operacijos dėl nuolatinių rizikos veiksnių arba idiopatinės DVT ar PE.
Insulto prevencija pacientams, sergantiems prieširdžių virpėjimu, DVT / PE
Šioms grupėms rekomenduojama Pradaxa paros dozė yra 220 mg, po vieną 110 mg kapsulę du kartus per parą:
• 80 metų ir vyresni pacientai
• Pacientai, kartu gydomi verapamiliu
Šioms grupėms 300 mg arba 220 mg Pradaxa paros dozę reikia nustatyti individualiai, įvertinant tromboembolijos ir kraujavimo riziką:
• Pacientai nuo 75 iki 80 metų
• Pacientai, kuriems yra vidutinio sunkumo inkstų funkcijos sutrikimas
• Pacientams, sergantiems gastritu, ezofagitu ar gastroezofaginio refliukso liga
• Kiti pacientai, kuriems yra padidėjusi kraujavimo rizika
GVT / PE atveju rekomendacija vartoti 220 mg Pradaxa kartu su viena 110 mg kapsule du kartus per parą yra pagrįsta farmakokinetikos ir farmakodinamikos vertinimais ir nebuvo tirta šiame klinikiniame pogrupyje.
Daugiau informacijos rasite 4.4, 4.5, 5.1 ir 5.2 skyriuose.
Jei netoleruojate dabigatrano, pacientus reikia patarti nedelsiant kreiptis į savo gydytoją, kuris galėtų juos pakeisti kitais priimtinais gydymo būdais, kad būtų išvengta insulto ir ES, susijusių su prieširdžių virpėjimu ar DVT / PE.
Senyvi žmonės (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu, DVT / PE)
75-80 metų pacientai turi būti gydomi 300 mg paros doze, vartojama po vieną 150 mg kapsulę du kartus per parą. Individualiai ir gydytojo nuožiūra 220 mg paros dozė, vartojama po vieną 110 mg kapsulę du kartus per parą, gali būti svarstoma, kai tromboembolijos rizika yra maža ir kraujavimo rizika yra didelė (žr. 4.4 skyrių).
80 metų ar vyresni pacientai turi būti gydomi 220 mg paros doze, vartojama po vieną 110 mg kapsulę du kartus per parą, nes šioje grupėje padidėja kraujavimo rizika.
Kadangi vyresnio amžiaus žmonėms (vyresniems nei 75 metų) inkstų funkcijos sutrikimas gali būti dažnas, prieš pradedant gydymą Pradaxa, inkstų funkcija turi būti įvertinta apskaičiuojant CrCL, kad neįtrauktų pacientų, kuriems yra sunkus inkstų funkcijos sutrikimas (t.
Pacientai, kuriems yra kraujavimo rizika (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu, DVT / PE)
Pacientai, kuriems yra padidėjusi kraujavimo rizika (žr. 4.4, 4.5, 5.1 ir 5.2 skyrius), turi būti „atidžiai kliniškai stebimi (ieškoma kraujavimo ar anemijos požymių). Dozės koregavimas turi būti sprendžiamas gydytojo nuožiūra“. kiekvieno paciento nauda ir potenciali rizika. Krešėjimo tyrimas (žr. 4.4 skyrių) gali padėti nustatyti pacientus, kuriems yra padidėjusi kraujavimo rizika dėl „padidėjusio dabigatrano poveikio. Kai pacientams, kuriems yra didelė kraujavimo rizika, nustatoma per didelė dabigatrano ekspozicija, 220 mg dozė, vartojama kaip viena 110 mg kapsulę du kartus per parą. Kai atsiranda kliniškai reikšmingas kraujavimas, gydymą reikia nutraukti.
Žmonėms, sergantiems gastritu, ezofagitu ar stemplės refliuksu, gali būti svarstoma 220 mg dozė, vartojama po vieną 110 mg kapsulę du kartus per parą, nes yra didelė kraujavimo iš virškinimo trakto rizika (žr. 4.4 skyrių).
Inkstų funkcijos įvertinimas (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu, DVT / PE):
Visiems pacientams:
• Prieš pradedant gydyti Pradaxa, inkstų funkcija turi būti įvertinta apskaičiuojant kreatinino klirensą (CrCL), kad būtų pašalinti pacientai, kuriems yra sunkus inkstų funkcijos sutrikimas (ty CrCL).
• Inkstų funkcija taip pat turėtų būti įvertinta, kai gydymo metu įtariama sumažėjusi inkstų funkcija (pvz., Hipovolemija, dehidratacija ir tuo pat metu vartojant tam tikrus vaistinius preparatus).
Papildomi reikalavimai pacientams, kuriems yra lengvas ar vidutinio sunkumo inkstų funkcijos sutrikimas ir vyresni nei 75 metų pacientai:
• Gydant Pradaxa, inkstų funkcija turi būti įvertinta bent kartą per metus arba dažniau, kai to reikia, kai tam tikrose klinikinėse situacijose, kai įtariama inkstų funkcijos susilpnėjimas ar pablogėjimas (pvz., Hipovolemija, dehidratacija ir kai kartu vartojama kai kurių vaistų).
Inkstų funkcijai įvertinti (CrCL ml / min.) Klinikinio Pradaxa vystymosi metu buvo taikomas Cockgroft-Gault metodas (žr. 75 mg Pradaxa 4.2 skyrių).
Inkstų funkcijos sutrikimas (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu, DVT / PE)
Gydymas Pradaxa pacientams, kuriems yra sunkus inkstų funkcijos sutrikimas (CrCLr
Pacientams, kuriems yra lengvas inkstų funkcijos sutrikimas (CrCL 50-≤ 80 ml / min.), Dozės koreguoti nereikia. Net pacientams, kuriems yra vidutinio sunkumo inkstų funkcijos sutrikimas (CrCL 30-50 ml / min.), Rekomenduojama Pradaxa dozė yra 300 mg, vartojama po vieną 150 mg kapsulę du kartus per parą. Tačiau pacientams, kuriems yra didelė kraujavimo rizika, reikia apsvarstyti galimybę sumažinti Pradaxa dozę iki 220 mg, vartojamos po vieną 110 mg kapsulę du kartus per parą (žr. 4.4 ir 5.2 skyrius). Pacientus, kurių inkstų funkcija sutrikusi, rekomenduojama atidžiai stebėti.
Pradaxa vartojimas kartu su silpnais ar vidutinio sunkumo P-glikoproteino (P-gp) inhibitoriais, tokiais kaip amiodaronas, chinidinas ar verapamilis (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu, DVT / PE)
Vartojant kartu su amiodaronu ar chinidinu, dozės koreguoti nereikia (žr. 4.4, 4.5 ir 5.2 skyrius).
Pacientams, vartojantiems tiek dabigatrano eteksilatą, tiek verapamilį, dabigatrano dozę reikia sumažinti iki 220 mg, vartojant po vieną 110 mg kapsulę du kartus per parą (žr. 4.4 ir 4.5 skyrius). Tokiu atveju Pradaxa ir verapamilį reikia vartoti kartu.
Svoris (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu, DVT / PE)
Remiantis turimais klinikiniais ir kinetiniais duomenimis, dozės koreguoti nereikia (žr. 5.2 skyrių), tačiau pacientus, kurių kūno svoris yra rekomenduojamas, rekomenduojama atidžiai stebėti.
Lytis (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu, DVT / PE)
Remiantis turimais klinikiniais ir kinetiniais duomenimis, dozės koreguoti nereikia (žr. 5.2 skyrių).
Kepenų funkcijos sutrikimas (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu, DVT / PE)
Pacientai, kurių kepenų fermentų koncentracija padidėjo daugiau nei dvigubai virš viršutinės normos ribos (VNR), nebuvo įtraukti į pagrindinius klinikinius tyrimus. Šiai pacientų pogrupiui gydymo patirties nėra, todėl Pradaxa šiai populiacijai vartoti nerekomenduojama (žr. 4.4 ir 5.2 skyrius). Jis yra kontraindikuotinas esant kepenų funkcijos sutrikimui ar kepenų ligai, kuri gali turėti įtakos išgyvenimui (žr. 4.3 skyrių).
Keitimas (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu, DVT / PE)
Nuo gydymo Pradaxa iki parenteralinio antikoagulianto
Rekomenduojama palaukti 12 valandų po paskutinės dozės, prieš pereinant nuo dabigatrano eteksilato prie parenterinio antikoagulianto (žr. 4.5 skyrių).
Nuo parenterinių antikoaguliantų iki Pradaxa
Nustokite vartoti parenterinį antikoaguliantą ir pradėkite dabigatrano eteksilatą likus 0–2 valandoms iki numatytos kitos pradinės terapijos dozės arba nutraukus gydymą, jei gydymas tęsiamas (pvz., Į veną nefrakcionuotas heparinas (ENF)) (žr. 4.5 skyrių).
Nuo Pradaxa iki vitamino K antagonistų (AVK)
Gydymo VKA pradžia turėtų būti nustatyta remiantis CRC pagal šias indikacijas:
• CrCL ≥ 50 ml / min., Pradėkite VKA 3 dienas prieš nutraukdami dabigatrano eteksilatą
• CrCL ≥ 30-
Kadangi Pradaxa gali padidinti INR vertę, jis geriau atspindės AVK poveikį tik praėjus mažiausiai 2 dienoms nuo Pradaxa vartojimo nutraukimo. Iki tol INR vertės turėtų būti aiškinamos atsargiai.
Nuo AVK iki Pradaxa
AVK vartojimą reikia nutraukti. Dabigatrano eteksilatą galima skirti, kai tik tarptautinis normalizuotas santykis (INR)
Kardioversija (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu, DVT / PE)
Pacientai, kuriems atliekama kardioversija, gali tęsti gydymą dabigatranu.
Vaikų populiacija (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu)
Vaikų populiacijoje Pradaxa nėra tinkamas vartoti pagal indikaciją: insulto ir sisteminės embolijos prevencija pacientams, sergantiems NVAF.
Vaikų populiacija (DVT / PE)
Pradaxa saugumas ir veiksmingumas vaikams nuo gimimo iki 18 metų dar nenustatytas. Šiuo metu turimi duomenys aprašyti 4.8 ir 5.1 skyriuose, tačiau rekomendacijų dėl dozavimo pateikti negalima.
Praleista dozė (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu, DVT / PE)
Praleistą dabigatrano eteksilato dozę vis tiek galima išgerti likus 6 valandoms iki kitos dozės, o po to praleistą dozę reikia praleisti.
Negalima dvigubinti dozių norint kompensuoti praleistą dozę.
Vartojimo metodas (pirminė venų tromboembolijos epizodų prevencija ortopedinėje chirurgijoje, insulto prevencija pacientams, sergantiems prieširdžių virpėjimu, DVT / PE)
Pradaxa galima vartoti valgant arba nevalgius. Pradaxa reikia nuryti visą, užgeriant stikline vandens, kad palengvėtų skrandžio išsiskyrimas.
Pacientams reikia patarti neatidaryti kapsulių, nes tai gali padidinti kraujavimo riziką (žr. 5.2 ir 6.6 skyrius).
04.3 Kontraindikacijos
• Padidėjęs jautrumas veikliajai arba bet kuriai 6.1 skyriuje nurodytai pagalbinei medžiagai
• Pacientai, kuriems yra sunkus inkstų funkcijos sutrikimas (CrCL)
• Kliniškai reikšmingas aktyvus kraujavimas
• Sužalojimai ar sąlygos, jei laikoma reikšmingu didelio kraujavimo rizikos veiksniu. Jie gali apimti esamą ar neseniai atsiradusią virškinimo trakto opą, didelę kraujavimo neoplazmų riziką, neseniai patirtą smegenų ar stuburo sužalojimą, neseniai atliktas smegenų, stuburo ar oftalmologines operacijas, neseniai atsiradusį intrakranijinį kraujavimą, žinomas ar įtariamas stemplės venų varikozes, arterioveninius apsigimimus, kraujagyslių aneurizmas arba pagrindinius intraspinalinius ar intracerebrinius kraujagysles. anomalijos
• Kartu vartojamas bet koks kitas antikoaguliantas, pvz., Nefrakcionuotas heparinas (ENF), mažos molekulinės masės heparinas (enoksaparinas, dalteparinas ir kt.), Heparino dariniai (fondaparinuksas ir kt.), Geriamieji antikoaguliantai (varfarinas, rivaroksabanas, apiksabanas ir kt.). antikoaguliantų terapijos keitimo aplinkybės (žr. 4.2 skyrių) arba kai ENF skiriamas dozėmis, būtinomis išlaikyti centrinės venos ar arterijos kateterio patentą (žr. 4.5 skyrių)
• Kepenų funkcijos sutrikimas ar kepenų liga, galinti turėti įtakos išgyvenimui
• Kartu vartojamas sisteminis ketokonazolas, ciklosporinas, itrakonazolas ir dronedaronas (žr. 4.5 skyrių)
• Širdies vožtuvo protezai, kuriems reikalingas gydymas antikoaguliantais (žr. 5.1 skyrių).
04.4 Specialūs įspėjimai ir tinkamos atsargumo priemonės
Kepenų funkcijos sutrikimas
Į pagrindinius klinikinius tyrimus neįtraukti pacientai, kurių kepenų fermentų koncentracija buvo didesnė nei dvigubai didesnė už normos ribą. Šioje pacientų grupėje gydymo patirties nėra, todėl Pradaxa šiai populiacijai vartoti nerekomenduojama.
Kraujavimo rizika
Dabigatrano eteksilatą reikia vartoti atsargiai esant padidėjusiai kraujavimo rizikai ir tais atvejais, kai kartu vartojama medžiagų, kurios keičia hemostazę, slopindamos trombocitų agregaciją. Gydymo metu dabigatrano eteksilatas gali kraujuoti bet kurioje kūno vietoje. Nepaaiškinamas hemoglobino ir / arba hematokritas ar kraujospūdis turėtų paskatinti ieškoti kraujavimo vietos.
Tokie veiksniai, kaip inkstų funkcijos susilpnėjimas (30-50 ml / min. CrCL), amžius ≥ 75 metai, dabigatrano koncentracija plazmoje maža (žr. 4.2, 4.5 ir 5.2 skyrius).
Kartu vartojant tikagrelorą, padidėja dabigatrano ekspozicija ir gali atsirasti farmakodinaminė sąveika, dėl kurios gali padidėti kraujavimo rizika (žr. 4.5 skyrių).
Insulto ir SE prevencijos tyrime, kuriame dalyvavo suaugę pacientai, sergantys NVAF, dabigatrano eteksilatas buvo susijęs su didesniu kraujavimu iš virškinimo trakto (GI), kuris buvo statistiškai reikšmingas vartojant 150 mg dabigatrano eteksilato du kartus per parą. Ši rizika padidėjo vyresnio amžiaus žmonėms (≥ 75 metų). Acetilsalicilo rūgšties (ASA), klopidogrelio ar nesteroidinių vaistų nuo uždegimo (NVNU) vartojimas, taip pat ezofagitas, gastritas ar gastroezofaginis refliuksas taip pat padidina kraujavimo iš virškinimo trakto riziką. Šiems pacientams, sergantiems prieširdžių virpėjimu, reikia apsvarstyti 220 mg dozę, vartojamą po vieną 110 mg kapsulę du kartus per parą, ir laikytis 4.2 skyriuje rekomenduojamos dozės. Norint apsisaugoti nuo kraujavimo iš virškinimo trakto, gali būti svarstomas PPI skyrimas.
Kraujavimo rizika gali padidėti pacientams, kurie kartu gydomi selektyviais serotonino reabsorbcijos inhibitoriais (SSRI) arba selektyviais serotonino ir norepinefrino reabsorbcijos inhibitoriais (SNRI) (žr. 4.5 skyrių).
Gydymo metu rekomenduojama atidžiai stebėti kliniką (ieškoti kraujavimo ar anemijos požymių), ypač jei rizikos veiksniai yra kartu (žr. 5.1 skyrių).
1 lentelėje apibendrinti veiksniai, galintys padidinti kraujavimo riziką. Taip pat žiūrėkite 4.3 skyriuje pateiktas kontraindikacijas.
1 lentelė. Veiksniai, galintys padidinti kraujavimo riziką
Jei yra pažeidimų, būklių, procedūrų ir (arba) gydymas vaistais (pvz., NVNU, antitrombocitiniais vaistais, SSRI ir SNRI, žr. 4.5 skyrių), kurie žymiai padidina didelio kraujavimo riziką, reikia atidžiai įvertinti naudos ir rizikos santykį. Pradaxa galima skirti tik tuo atveju, jei nauda yra didesnė už kraujavimo riziką.
Pradaxa paprastai nereikia reguliariai stebėti krešėjimo parametrų. Tačiau su dabigatranu susijusio antikoagulianto poveikio įvertinimas gali būti naudingas siekiant išvengti pernelyg didelės dabigatrano ekspozicijos esant papildomiems rizikos veiksniams. INR testas nėra patikimas pacientams, gydytiems Pradaxa, ir pranešta apie klaidingai teigiamą INR padidėjimą. Todėl INR tyrimo atlikti negalima. Praskiestas plazmos trombino laikas (dTT), ekarino laikas (ECT), aktyvuotas dalinis tromboplastino laikas (aPTT) gali suteikti naudingos informacijos, tačiau bandymai nėra standartizuoti, o rezultatus reikia aiškinti atsargiai (žr. 5.1 skyrių).
2 lentelėje parodytos krešėjimo bandymų ribos, kurios gali būti susijusios su padidėjusia kraujavimo rizika (žr. 5.1 skyrių).
2 lentelė. Ribinės ribinės vertės koaguliacijos tyrimų metu, kurios gali būti susijusios su padidėjusia kraujavimo rizika
Pacientams, kuriems pasireiškia ūminis inkstų nepakankamumas, Pradaxa vartojimą reikia nutraukti (žr. 4.3 skyrių).
Duomenys apie pacientų svorį
Kai pasireiškia stiprus kraujavimas, gydymą reikia nutraukti ir ištirti kraujavimo šaltinį (žr. 4.9 skyrių).
Vaistų, kurie gali padidinti kraujavimo riziką, kartu su Pradaxa vartoti negalima arba atsargiai (žr. 4.5 skyrių).
Fibrinolitinių vaistų vartojimas ūminiam išeminiam insultui gydyti
Fibrinolitinių vaistinių preparatų vartojimas ūminiam išeminiam insultui gydyti gali būti svarstomas, jei paciento dTT, ECT arba aPTT yra mažesnis už viršutinę normos ribą, atsižvelgiant į vietinį atskaitos diapazoną.
Sąveika su P-gp induktoriais
Kartu vartojant P-gp induktorius (pvz., Rifampiciną, jonažolę (Hypericum perforatum), karbamazepiną ar fenitoiną), galima tikėtis dabigatrano koncentracijos plazmoje sumažėjimo, todėl to reikėtų vengti (žr. 4.5 ir 5.2 skyrius).
Chirurgija ir intervencijos
Pacientams, vartojantiems dabigatrano eteksilatą, kuriems atliekama operacija ar invazinės procedūros, padidėja kraujavimo rizika. Todėl chirurginėms intervencijoms gali prireikti laikinai sustabdyti gydymą.
Rekomenduojama atsargiai ir stebėti antikoaguliantų aktyvumą, kai gydymas laikinai sustabdomas dėl operacijos. Pacientams, sergantiems inkstų nepakankamumu, dabigatrano klirensas gali užtrukti ilgiau (žr. 5.2 skyrių). Tai reikia įvertinti prieš kiekvieną procedūrą. Tokiais atvejais krešėjimo tyrimas (žr. 4.4 ir 5.1 skyrius) gali padėti nustatyti, ar hemostazė vis dar yra sutrikusi.
Priešoperacinis etapas
3 lentelėje apibendrintos nutraukimo taisyklės prieš invazines ar chirurgines procedūras.
3 lentelė. Nutraukimo taisyklės prieš invazines ar chirurgines procedūras
Jei reikia skubių veiksmų, dabigatrano eteksilato vartojimą reikia laikinai sustabdyti. Jei įmanoma, operaciją / intervenciją reikia atidėti mažiausiai 12 valandų po paskutinės išgertos dozės. Jei operacijos negalima atidėti, gali padidėti kraujavimo rizika. Šią kraujavimo riziką reikia palyginti su operacijos skubumu (dėl kardioversijos žr. 4.2 skyrių).
Stuburo anestezija / epidurinė nejautra / juosmens punkcija
Tokioms procedūroms kaip stuburo anestezija reikia įprastų hemostazinių funkcijų.
Stuburo ar epidurinės hematomos rizika gali padidėti trauminio ar pakartotinio punkcijos atvejais ir ilgai naudojant epidurinius kateterius. Pašalinus kateterį, prieš pradedant pirmąją dabigatrano eteksilato dozę, turi praeiti mažiausiai 2 valandų intervalas. Šiems pacientams reikia dažnai stebėti stuburo ar epidurinės hematomos neurologinius požymius ir simptomus.
Pooperacinis etapas
Po invazinės procedūros ar operacijos dabigatrano eteksilato vartojimą reikia atnaujinti kuo greičiau, jei nustatyta, kad klinikinė situacija leidžia tinkamai hemostazuoti.
Pacientus, kuriems yra didelė kraujavimo rizika, arba pacientus, kuriems yra per didelis ekspozicijos pavojus, ypač pacientus, kuriems yra vidutinio sunkumo inkstų funkcijos sutrikimas (CrCL 30-50 ml / min.), Reikia gydyti atsargiai (žr. 4.4 ir 5.1 skyrius).
Pacientai, kuriems yra didelė mirties rizika dėl operacijos ir kuriems būdingi tromboembolinių reiškinių rizikos veiksniai
Dabigatrano veiksmingumo ir saugumo šiems pacientams duomenų yra nedaug, todėl juos reikia gydyti atsargiai.
Klubo lūžių operacija
Duomenų apie Pradaxa vartojimą pacientams, kuriems atliekama klubo lūžio operacija, nėra. Todėl gydymas nerekomenduojamas.
Miokardo infarktas (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu)
III fazės RE-LY tyrimo metu (žr. 5.1 skyrių) bendras miokardo infarkto (MI) dažnis buvo atitinkamai 0,82, 0,81 ir 0,64% per metus vartojant 110 mg du kartus per parą dabigatrano eteksilato, 150 mg dabigatrano eteksilato ir varfarino. santykinė dabigatrano rizika padidėjo 29% ir 27%, palyginti su varfarinu. Nepriklausomai nuo to, koks gydymas buvo atliktas, didžiausia absoliuti MI rizika buvo pastebėta šiuose pogrupiuose, kurių santykinė rizika buvo panaši: pacientai, kuriems anksčiau buvo MI, ≥ 65 metų pacientai amžiaus, sergantiems cukriniu diabetu ar vainikinių arterijų liga, pacientams, kuriems yra kairiojo skilvelio išstūmimo frakcija
Miokardo infarktas (DVT / PE)
Trijuose aktyviai kontroliuojamuose klinikiniuose tyrimuose buvo nustatytas didesnis MI dažnis pacientams, gydytiems dabigatrano eteksilatu, nei gydytiems varfarinu: 0,4%, palyginti su 0,2%, trumpalaikiams RE-COVER ir RE-COVER II; ir 0,8%, palyginti su 0,1% ilgalaikio RE-MEDY tyrimo metu. Šiame tyrime padidėjimas buvo statistiškai reikšmingas (p = 0,022).
RE-SONATE tyrime, kuriame dabigatrano eteksilatas buvo lyginamas su placebu, MI dažnis buvo 0,1% pacientų, vartojusių dabigatrano eteksilatą, ir 0,2% pacientų, vartojusių placebą.
Pacientai, sergantys aktyviu vėžiu (DVT / PE)
DVT / PE veiksmingumas ir saugumas pacientams, sergantiems vėžiu, nenustatytas.
Dažai
Pradaxa kietose kapsulėse yra saulėlydžio geltonojo dažiklio (E110), kuris gali sukelti alergines reakcijas.
04.5 Sąveika su kitais vaistiniais preparatais ir kitos sąveikos formos
Antikoaguliantai ir antitrombocitinės medžiagos
Šių gydymo būdų, kurie gali padidinti kraujavimo riziką vartojant kartu su Pradaxa, patirties nėra arba yra nedaug: antikoaguliantai, tokie kaip nefrakcionuotas heparinas (ENF), mažos molekulinės masės heparinas (LMWH) ir heparino dariniai (fondaparinuksas, desirudinas), tromboliziniai vaistai vaistai ir vitamino K antagonistai, rivaroksabanas ar kiti geriamieji antikoaguliantai (žr. 4.3 skyrių) ir antitrombocitiniai vaistai, tokie kaip GPIIb / IIIa receptorių antagonistai, tiklopidinas, prasugrelis, tikagreloras, dekstranas ir sulfinpirazonas (žr. 4.4 skyrių).
Remiantis ribotais duomenimis, surinktais III fazės RE-LY tyrime su pacientais, kuriems yra prieširdžių virpėjimas, kartu su kitais geriamaisiais ar parenteraliniais antikoaguliantais buvo pastebėta, kad didelio kraujavimo dažnis padidėja maždaug 2,5 karto tiek vartojant dabigatrano eteksilatą, nei vartojant varfariną. , ypač kai pereinama nuo vieno antikoagulianto prie kito (žr. 4.3 skyrių).
ENF galima skirti tokiomis dozėmis, kurios yra būtinos norint išlaikyti centrinės venos ar arterijos kateterio patentą (žr. 4.3 skyrių).
Klopidogrelis ir ASA: Remiantis duomenimis, surinktais III fazės RE-LY tyrime (žr. 5.1 skyrių), pastebėta, kad kartu vartojant antitrombocitinių preparatų, ASR ar klopidogrelio, maždaug dvigubai padidėja kraujavimo dažnis tiek vartojant dabigatrano eteksilatą, tiek varfariną (žr. 4.4 skyrių).
Klopidogrelis. I fazės tyrimo metu, kuriame dalyvavo sveiki, jauni savanoriai vyrai, kartu vartojant dabigatrano eteksilatą ir klopidogrelį, pailgėjo kapiliarų kraujavimo laikas, palyginti su vien klopidogreliu. Be to, „AUC?“, „S“ ir „Cmax“, „ss“ ir krešėjimo matai, skirti dabigatrano poveikiui arba trombocitų agregacijos slopinimui, kaip klopidogrelio poveikio matas, iš esmės nepakito, lyginant kombinuotą gydymą ir atitinkamą mono įsotinamoji 300 mg arba 600 mg klopidogrelio dozė, dabigatrano AUC, ss ir Cmax, ss padidėjo maždaug 30-40% (žr. 4.4 skyrių) (taip pat žr.
ASA: II fazės tyrime, kuriame atsitiktinės atrankos būdu buvo vartojamas ASS, buvo tiriamas kartu vartojamo dabigatrano eteksilato ir ASA poveikis kraujavimo rizikai. Remiantis ASS analize. Logistinė regresija, kartu vartojant ASR ir 150 mg dabigatrano eteksilato du kartus per parą, bet kokio tipo kraujavimo rizika gali padidėti nuo 12% iki 18% ir 24% vartojant atitinkamai 81 mg ir 325 mg ASS (žr. 4.4 skyrių).
Nesteroidiniai vaistai nuo uždegimo: įrodyta, kad nesteroidiniai vaistai nuo uždegimo, vartojami kaip trumpo veikimo analgetikai perioperaciniu laikotarpiu, nėra susiję su padidėjusia kraujavimo rizika, kai jie vartojami kartu su dabigatrano eteksilatu. Lėtinis NVNU vartojimas kraujavimo riziką padidino maždaug 50%. ir varfarinas. Todėl dėl kraujavimo rizikos, ypač vartojant NVNU, kurių pusinės eliminacijos laikas yra> 12 valandų, rekomenduojama atidžiai stebėti kraujavimo požymius (žr. 4.4 skyrių).
LMWH: LMWH, pvz., Enoksaparino ir dabigatrano eteksilato, vartojimas kartu nebuvo specialiai įvertintas. Perėjus nuo 3 dienų gydymo 40 mg enoksaparino, vartojamo vieną kartą per parą, 24 valandas po LMWH vartojimo. Paskutinis enoksaparino dozę, dabigatrano ekspozicija buvo šiek tiek mažesnė nei pavartojus vien dabigatrano eteksilato (vienkartinė 220 mg dozė). Didesnis anti-FXa / FIIa aktyvumas buvo pastebėtas pavartojus dabigatrano eteksilato, prieš pradedant gydymą enoksaparinu, palyginti su gydymu dabigatranu tik eteksilatas. Manoma, kad taip yra dėl gydymo enoksaparinu varomojo poveikio ir manoma, kad jis nėra kliniškai svarbus. Kitų su dabigatranu susijusių antikoaguliantų aktyvumo tyrimų rezultatai iš esmės nepasikeitė iš anksto gydant enoksaparinu.
Sąveika, susijusi su dabigatrano eteksilato ir dabigatrano metaboliniu profiliu
Dabigatrano eteksilatas ir dabigatranas nemetabolizuojami citochromo P450 sistemoje ir neturi jokio poveikio. in vitro apie žmogaus citochromo P450 fermentus. Todėl sąveikos su panašiais vaistiniais preparatais ir dabigatranu nesitikima.
Transportuotojų sąveika
P-gp inhibitoriai
Dabigatrano eteksilatas yra išsiliejimų nešiklio P-gp substratas. Vartojant kartu su P-gp inhibitoriais (tokiais kaip amiodaronas, verapamilis, chinidinas, ketokonazolas, dronedaronas, klaritromicinas ir tikagreloras), gali padidėti dabigatrano koncentracija plazmoje.
Jei nenurodyta kitaip, dabigatraną kartu su stipriais P-gp inhibitoriais reikia atidžiai stebėti (ieškant kraujavimo ar anemijos požymių). Krešėjimo tyrimas padeda nustatyti pacientus, kuriems dėl padidėjusio dabigatrano poveikio padidėja kraujavimo rizika (žr. 4.2, 4.4 ir 5.1 skyrius).
Šie stiprūs P-gp inhibitoriai yra draudžiami: sistemiškai vartojamas ketokonazolas, ciklosporinas, itrakonazolas ir dronedaronas (žr. 4.3 skyrių). Tacrolimuzo nerekomenduojama vartoti. Silpno vidutinio sunkumo vaistų (pvz., Amiodarono, posakonazolo, chinidino, verapamilio) P-gp inhibitoriai ir tikagreloro) reikia vartoti atsargiai (žr. 4.2 ir 4.4 skyrius).
Ketokonazolas: Ketokonazolas, išgėrus vieną 400 mg dozę, padidino bendrąjį dabigatrano AUC0-∞ ir Cmax atitinkamai 138% ir 135% ir atitinkamai 153% ir 149%, išgėrus vieną kartą 400 mg ketokonazolo. kasdien. Ketokonazolas nekeitė laiko iki piko, galutinio pusinės eliminacijos periodo ir vidutinio gyvenimo laiko (žr. 4.4 skyrių). Vartoti kartu su sisteminiu ketokonazolu draudžiama (žr. 4.3 skyrių).
Dronedaronas. Kartu skiriant dabigatrano eteksilatą ir dronedaroną, bendros dabigatrano AUC0-∞ ir Cmax vertės padidėjo atitinkamai maždaug 2,4 karto ir 2,3 karto (+ 136% ir 125%) po 400 dozių. mg dronedarono du kartus, o maždaug po 2,1 karto ir 1,9 karto (+ 114% ir 87%) po vienkartinės 400 mg dozės. Dronedaronas neturėjo įtakos galutiniam dabigatrano pusinės eliminacijos laikui ir inkstų klirensui. dronedarono dozės buvo suleistos praėjus 2 valandoms po dabigatrano eteksilato, dabigatrano AUC0-∞ padidėjo atitinkamai 1,3 karto ir 1,6 karto. Gydymas dronedaronu yra draudžiamas.
Amiodaronas: Pradaxa skiriant kartu su vienkartine 600 mg amiodarono doze, amiodarono ir jo aktyvaus metabolito DEA kiekis ir absorbcijos lygis iš esmės nepakito. Dabigatrano AUC ir Cmax padidėjo atitinkamai maždaug 60% ir 50%. Sąveikos mechanizmas nėra visiškai išaiškintas. Atsižvelgiant į ilgą amiodarono pusinės eliminacijos periodą, galima sąveika su vaistiniais preparatais gali išlikti kelias savaites po amiodarono vartojimo nutraukimo (žr. 4.2 ir 4.4 skyrius).
Pacientams, gydomiems VTE profilaktikai po klubo ar kelio sąnario keitimo operacijos, kartu vartojant dabigatrano eteksilatą ir amiodaroną, Pradaxa dozę reikia sumažinti iki 150 mg 2 x 75 mg kapsulių kartą per parą (žr. 4.2 skyrių). Kai dabigatrano eteksilatas vartojamas kartu su amiodaronu, rekomenduojama atidžiai stebėti klinikinę būklę, ypač kai atsiranda kraujavimas, ir ypač atsargiai pacientams, kuriems yra lengvas ar vidutinio sunkumo inkstų funkcijos sutrikimas.
Chinidinas: Chinidinas buvo skiriamas 200 mg dozėmis kas 2 valandas iki bendros 1000 mg dozės. Dabigatrano eteksilatas buvo vartojamas du kartus per parą 3 dienas iš eilės, trečią dieną su chinidinu arba be jo. Kartu vartojant chinidiną, dabigatrano AUC, ss ir Cmax, ss padidėjo vidutiniškai atitinkamai 53% ir 56% (žr. 4.2 ir 4.4 skyrius).
Pacientams, gydomiems VTE profilaktikai po klubo ar kelio sąnario keitimo operacijos, Pradaxa dozę reikia sumažinti iki 150 mg vieną kartą per parą 2 x 75 mg kapsulėse, jei kartu vartojama dabigatrano eteksilato ir chinidino (žr. 4.2 skyrių). Kai dabigatrano eteksilatas vartojamas kartu su chinidinu, rekomenduojama atidžiai stebėti klinikinę būklę, ypač kai atsiranda kraujavimas, ir ypač atsargiai pacientams, kuriems yra lengvas ar vidutinio sunkumo inkstų funkcijos sutrikimas.
Verapamilis: Kai dabigatrano eteksilatas (150 mg) buvo vartojamas kartu su geriamuoju verapamiliu, dabigatrano Cmax ir AUC padidėjo, tačiau šio pokyčio dydis kinta priklausomai nuo vartojimo laiko ir verapamilio formos (žr. 4.2 ir 4.4 skyrius).
Didžiausias dabigatrano ekspozicijos padidėjimas buvo pastebėtas pirmą kartą vartojant greito atpalaidavimo verapamilio kompoziciją, suleistą valandą prieš dabigatrano eteksilato vartojimą (Cmax padidėjo maždaug 180%, o AUC-maždaug 150%). Poveikis palaipsniui mažėjo vartojant pailginto atpalaidavimo preparatą (Cmax padidėjimas maždaug 90% ir AUC maždaug 70%) arba skiriant daugkartines verapamilio dozes (Cmax padidėjimas maždaug 60% ir AUC padidėjimas maždaug 50%).
Todėl, kai dabigatraną vartojama kartu su verapamiliu, būtina atidžiai stebėti kliniką (ar nėra kraujavimo ar anemijos požymių). Pacientams, kurių inkstų funkcija normali po klubo ar kelio sąnario keitimo operacijos, kartu gydoma dabigatrano eteksilatu ir verapamiliu, Pradaxa dozę reikia sumažinti iki 150 mg, vartojant 2 x 75 mg kapsules vieną kartą per parą. Pacientams, kuriems yra vidutinio sunkumo inkstų funkcijos sutrikimas, kartu vartojama vartojant dabigatrano eteksilatą ir verapamilį, reikia apsvarstyti galimybę sumažinti Pradaxa dozę iki 75 mg per parą (žr. 4.2 ir 4.4 skyrius).
Pacientams, sergantiems NVNU, gydomiems nuo insulto ir SE profilaktikai, ir pacientams, sergantiems DVT / PE, gydytiems dabigatrano eteksilatu ir verapamiliu, Pradaxa dozę reikia sumažinti iki 220 mg, vartojant po vieną 110 mg kapsulę du kartus per parą (žr. 4.2 skyrių).
Kai dabigatrano eteksilatas vartojamas kartu su verapamiliu, rekomenduojama atidžiai stebėti klinikinę būklę, ypač kai atsiranda kraujavimas, ir ypač atsargiai pacientams, kuriems yra lengvas ar vidutinio sunkumo inkstų funkcijos sutrikimas.
Skiriant verapamilį praėjus 2 valandoms po dabigatrano eteksilato vartojimo, reikšmingos sąveikos nepastebėta (Cmax padidėjo maždaug 10% ir AUC padidėjo maždaug 20%). Tai paaiškinama visiška dabigatrano absorbcija po 2 valandų (žr. 4.4 skyrių).
Klaritromicinas. Sveikiems savanoriams kartu su dabigatrano eteksilatu skiriant klaritromiciną (500 mg du kartus per parą), AUC padidėjo maždaug 19%, o Cmax - maždaug 15%, tačiau tai neturėjo įtakos klinikinei saugai. vartojant kartu su klaritromicinu, negalima atmesti kliniškai reikšmingos sąveikos. Todėl reikia atidžiai stebėti, kai dabigatrano eteksilatas vartojamas kartu su klaritromicinu, ypač kraujavimo atveju, ypač pacientams, kuriems yra lengvas ar vidutinio sunkumo inkstų funkcijos sutrikimas.
Tikagreloras: Kai vienkartinė 75 mg dabigatrano eteksilato dozė buvo skiriama kartu su pradine 180 mg tikagreloro doze, dabigatrano AUC ir Cmax padidėjo atitinkamai 1,73 ir 1,95 karto (+73 % ir 95 %). mg tikagreloro du kartus, dabigatrano ekspozicija padidėjo atitinkamai 1,56 ir 1,46 karto (+ 56% ir 46%) AUC ir Cmax.
Kartu vartojant pradinę 180 mg tikagreloro dozę ir 110 mg dabigatrano eteksilato (esant pusiausvyros būsenai), dabigatrano AUC α, Ss ir Cmax, ss padidėjo atitinkamai 1,49 ir 1,65 karto ( + 49% ir 65%) %), palyginti su vien dabigatrano eteksilato vartojimu. Kai pradinė 180 mg tikagreloro dozė buvo suleista praėjus 2 valandoms po 110 mg dabigatrano eteksilato (pusiausvyros būsena), dabigatrano AUC α, Ss ir Cmax, ss padidėjimas sumažėjo atitinkamai iki 1,27 karto ir 1,23 karto (+ 27% ir 23%), lyginant su vien dabigatrano eteksilato vartojimu. Šis laipsniškas vartojimas yra rekomenduojamas pradedant gydyti tikagrelorą pradine doze.
Kartu vartojant 90 mg tikagreloro du kartus per parą (palaikomoji dozė) ir 110 mg dabigatrano eteksilato, pakoreguotas dabigatrano AUC α, Ss ir Cmax, ss padidėjo atitinkamai 1,26 ir 1,29 karto, palyginti su vartojimu tik dabigatrano eteksilato.
Šie stiprūs P-gp inhibitoriai nebuvo ištirti kliniškai, tačiau remiantis duomenimis in vitro laukiamas panašus į ketokonazolą poveikis:
Itrakonazolas ir ciklosporinas, kurių vartoti draudžiama (žr. 4.3 skyrių).
Nustatyta, kad takrolimuzas in vitro slopina panašiai P-gp, kaip itrakonazolas ir ciklosporinas. Dabigatrano eteksilatas kartu su takrolimuzu nebuvo kliniškai tirtas. Tačiau turimi riboti klinikiniai duomenys apie kitą P-gp substratą (everolimuzą) rodo, kad P-gp slopinimas vartojant takrolimuzą yra silpnesnis nei pastebėtas vartojant stiprius P-gp inhibitorius. Remiantis šiais duomenimis, gydymo kartu su takrolimuzu nerekomenduojama. .
Pozakonazolas taip pat iš dalies slopina P-gp, tačiau nebuvo kliniškai ištirtas. Pradaxa ir pozakonazolą reikia skirti atsargiai.
P-gp induktoriai
Kartu vartojant P-gp induktorių (pvz., Rifampiciną, jonažolę (Hypericum perforatum), karbamazepiną ar fenitoiną), gali sumažėti dabigatrano koncentracija, todėl jo reikėtų vengti (žr. 4.4 ir 5.2 skyrius).
Rifampicinas: prieš tai paskyrus 600 mg rifampicino dozę vieną kartą per parą 7 dienas, bendra dabigatrano smailė ir bendra ekspozicija sumažėjo atitinkamai 65,5% ir 67%. Indukcinis poveikis sumažėjo, todėl septintą dieną po gydymo rifampicinu nutraukimo dabigatrano ekspozicija buvo artima pamatinei vertei. Po 7 dienų biologinio prieinamumo padidėjimo nepastebėta.
Kiti vaistai, veikiantys P-gp
Proteazės inhibitoriai, tokie kaip ritonaviras ir jo deriniai su kitais proteazės inhibitoriais, veikia P-gp (ir kaip inhibitoriai, ir kaip induktoriai). Kadangi jie netirti, jų nerekomenduojama vartoti kartu su Pradaxa.
P-gp substratas
Digoksinas. Tyrime, kuriame dalyvavo 24 sveiki pacientai, Pradaxa skiriant kartu su digoksinu, nepastebėta nei digoksino pokyčių, nei reikšmingų klinikinių dabigatrano ekspozicijos pokyčių.
Kartu vartojant selektyvius serotonino reabsorbcijos inhibitorius (SSRI) arba selektyvius serotonino ir norepinefrino reabsorbcijos inhibitorius (SNRI)
SSRI ir SNRI padidino kraujavimo riziką visose RE-LY tyrimo grupėse.
skrandžio pH
Pantoprazolas: Kai Pradaxa buvo vartojamas kartu su pantoprazolu, buvo pastebėtas maždaug 30% mažesnis plotas po dabigatrano koncentracijos ir laiko kreive plazmoje. Pantoprazolas ir kiti protonų siurblio inhibitoriai (PPI) buvo stebimi kartu su Pradaxa klinikinių tyrimų metu ir kartu vartojant PPI, Pradaxa veiksmingumas nesumažėjo.
Ranitidinas: Ranitidino vartojimas kartu su Pradaxa kliniškai reikšmingo poveikio dabigatrano absorbcijai neturi.
04.6 Nėštumas ir žindymo laikotarpis
Vaisingo amžiaus moterys / vyrų ir moterų kontracepcija
Vaisingo amžiaus moterys, gydydamos dabigatrano eteksilatu, turėtų vengti pastoti.
Nėštumas
Duomenų apie dabigatrano eteksilato vartojimą nėščioms moterims yra nedaug.
Tyrimai su gyvūnais parodė toksinį poveikį reprodukcijai (žr. 5.3 skyrių). Galima rizika žmonėms nežinoma.
Nėštumo metu Pradaxa vartoti negalima, išskyrus neabejotinai būtinus atvejus.
Maitinimo laikas
Klinikinių duomenų apie dabigatrano poveikį žindomiems kūdikiams nėra.
Gydymo Pradaxa metu žindymą reikia nutraukti.
Vaisingumas
Duomenų apie žmones nėra.
Tyrimų su gyvūnais metu 70 mg / kg dozė (5 kartus didesnė už pacientų ekspoziciją) pastebėjo poveikį patelių vaisingumui sumažėjusio implantacijos ir padidėjusio praradimo prieš implantaciją pavidalu. Kito poveikio moterų vaisingumui nepastebėta. Poveikio vyrų vaisingumui nenustatyta.Vartojant toksines motinoms dozes (ekspozicija plazmoje 5-10 kartų didesnė nei pacientų), žiurkėms ir triušiams stebėtas vaisiaus kūno svorio sumažėjimas ir embriono bei vaisiaus gyvybingumas, padidėjęs vaisiaus pakitimas. Prieš ir po gimdymo tyrimų metu buvo pastebėtas padidėjęs vaisiaus mirtingumas vartojant motinoms toksiškas dozes (dozė atitinka 4 kartus didesnę ekspoziciją plazmoje nei pacientams).
04.7 Poveikis gebėjimui vairuoti ir valdyti mechanizmus
Pradaxa gebėjimo vairuoti ir valdyti mechanizmus neveikia arba veikia nereikšmingai.
04.8 Nepageidaujamas poveikis
Saugos profilio santrauka
Iš viso 10 795 pacientai buvo gydomi 6 aktyviai kontroliuojamuose VTE prevencijos tyrimuose, naudojant bent vieną tiriamojo vaisto stiprumą. Iš šių 6 684 pacientų buvo gydoma 150 mg arba 220 mg Pradaxa per parą.
Pagrindiniame tyrime, kuriame buvo tiriama insulto ir SE prevencija pacientams, sergantiems prieširdžių virpėjimu, iš viso dabigatrano eteksilatas buvo gydomas 12 042. Iš jų 6059 buvo gydomi 150 mg dabigatrano eteksilato du kartus per parą, o 5 983 - dabigatrano eteksilatu. jie vartojo 110 mg du kartus per parą.
Dviejuose aktyviai kontroliuojamuose DVT / PE gydymo tyrimuose RE-COVER ir RE-COVER II iš viso 2553 pacientai buvo įtraukti į dabigatrano eteksilato saugumo analizę. Visi pacientai vartojo 150 mg dabigatrano eteksilato du kartus per parą. abiem gydymo atvejais dabigatrano eteksilatas ir varfarinas skaičiuojami nuo pirmojo dabigatrano eteksilato ar varfarino vartojimo nutraukus parenteralinį gydymą (tik geriamasis gydymo laikotarpis). Tai apima visas nepageidaujamas reakcijas, atsiradusias gydymo dabigatranu metu. įtrauktas gydymas varfarinu, išskyrus tuos atvejus, kurie pasireiškė sutapus tarp varfarino ir parenteralinio gydymo.
Iš viso 2114 pacientų buvo gydomi aktyviai kontroliuojamu DVT / PE prevencijos tyrimu RE-MEDY ir placebu / DVT / PE prevencijos tyrimu RE-SONATE. Visi pacientai vartojo 150 mg dabigatrano eteksilato du kartus per parą.
Iš viso apie 9% pacientų, gydytų planine klubo ar kelio operacija (trumpalaikis gydymas iki 42 dienų), 22% pacientų, sergančių prieširdžių virpėjimu, gydytų nuo insulto ir SE profilaktikos (ilgalaikis gydymas iki 3 metų), 14 Nepageidaujamų reakcijų patyrė% pacientų, gydytų DVT / PE ir 15% pacientų, gydytų dėl DVT / PE.
Dažniausiai pasireiškusios nepageidaujamos reakcijos yra kraujavimas, kuris iš viso pasireiškė maždaug 14% pacientų, kuriems buvo atlikta trumpalaikė planinė klubo ar kelio sąnario keitimo operacija, 16,6% pacientų, kuriems buvo ilgalaikė prieširdžių virpėjimas. 14,4% pacientų, gydytų DVT / PE. Be to, kraujavimas pasireiškė 19,4% pacientų, dalyvavusių DVT / PE prevencijos tyrime RE-MEDY, ir 10,5% pacientų, dalyvavusių DVT / PE RE-SONATE profilaktiniame tyrime.
Kadangi pacientų, gydytų pagal tris indikacijas, populiacijos nėra palyginamos, o kraujavimo įvykiai pasiskirsto skirtingose organų sistemų klasėse (SOC), apibendrinamas didelio kraujavimo ir bet kokio kraujavimo epizodų aprašymas, suskirstytas pagal indikacijas.
Nors klinikinių tyrimų metu tai pasireiškė retai, gali atsirasti didelių ar sunkių kraujavimo įvykių, kurie, nepriklausomai nuo vietos, gali būti neįgalūs, pavojingi gyvybei ar net mirtis.
Nepageidaujamų reakcijų santrauka
4 lentelėje pateikiamos nepageidaujamos reakcijos, nustatytos pirminiuose VTE profilaktikos tyrimuose po klubo ar kelio sąnario keitimo operacijos, tromboembolinio insulto ir ES profilaktikos tyrime pacientams, sergantiems prieširdžių virpėjimu, bei SOC užsakytais DVT / PE gydymo ir prevencijos tyrimais. ir dažnis, vadovaujantis tokia tvarka: labai dažni (≥ 1/10); dažni (≥ 1/100,
4 lentelė. Nepageidaujamos reakcijos
Pirminė venų tromboembolijos prevencija ortopedinėje chirurgijoje
Kraujavimas
5 lentelėje, atsižvelgiant į dozę, nurodytas pacientų (VTE profilaktinio gydymo laikotarpiu nepageidaujamo kraujavimo reakcijų skaičius) skaičius (%) VTE profilaktinio gydymo laikotarpiu.
5 lentelė. Pacientų, kuriems pasireiškė nepageidaujamos kraujavimo reakcijos, skaičius (%)
Didelio kraujavimo nepageidaujamų reakcijų apibrėžimai RE-NOVATE ir RE-MODEL tyrimuose buvo tokie:
• mirtinas kraujavimas
• kliniškai pasireiškiantis kraujavimas, susijęs su hemoglobino sumažėjimu ≥ 20 g / l (atitinka 1,24 mmol / l), tiek daugiau nei tikėtasi
• kliniškai pasireiškiantis kraujavimas, viršijantis numatytą ir reikalaujantis perpilti ≥ 2 vienetus eritrocitų arba viso kraujo, daugiau nei tikėtasi
• simptominis kraujavimas iš retroperitoninio, intrakranijinio, intraokulinio ar intraspinalinio kraujavimo
• kraujavimas, dėl kurio reikėjo nutraukti gydymą
• kraujavimas, kuriam prireikė naujos operacijos.
Reikalingi objektyvūs kraujo retroperitoninio kraujavimo (ultragarso ar kompiuterinės tomografijos (KT)) ir intraspinalinio kraujavimo (KT arba magnetinio rezonanso tomografijos) tyrimai.
Insulto ir ES profilaktika suaugusiems pacientams, sergantiems NVNU, turintiems vieną ar daugiau rizikos veiksnių
Kraujavimas
6 lentelėje pateikiami pagrindiniai bet kokie kraujavimo atvejai, nustatyti pagrindiniame tyrime, kuriame buvo vertinama insulto ir SE prevencija pacientams, sergantiems prieširdžių virpėjimu.
6 lentelė. Kraujavimo įvykiai tyrime, kuriame buvo vertinamas insultas ir SE prevencija pacientams, sergantiems prieširdžių virpėjimu
Didelis kraujavimas buvo nustatytas pagal vieną ar daugiau iš šių kriterijų:
Kraujavimas, susijęs su hemoglobino sumažėjimu bent 20 g / l arba dėl kurio reikėjo perpilti mažiausiai 2 vienetus raudonųjų kraujo kūnelių arba viso kraujo.
Simptominis kraujavimas kritinėje „zonoje ar organe: akispūdis, intrakranijinis, intraspinalinis ar raumeninis su skyrių sindromu, retroperitoninis kraujavimas, kraujavimas iš sąnarių ar kraujavimas iš perikardo.
Didelis kraujavimas buvo klasifikuojamas kaip pavojingas gyvybei, jei jis atitiko vieną ar daugiau iš šių kriterijų:
Mirtinas kraujavimas, simptominis intrakranijinis kraujavimas; sumažėjęs hemoglobino kiekis ne mažiau kaip 50 g / l; ne mažiau kaip 4 vienetų eritrocitų ar viso kraujo perpylimas; kraujavimas, susijęs su hipotenzija, dėl kurios reikia vartoti į veną vartojamų inotropinių vaistų; kraujavimas, kuriam prireikė operacijos.
Tiriamiesiems, atsitiktinai atrinktiems į 110 mg dabigatrano eteksilato du kartus per parą arba 150 mg du kartus per parą, buvo žymiai mažesnė gyvybei pavojingo kraujavimo ir intrakranijinio kraujavimo rizika nei varfarinu gydytiems asmenims [p
Klinikinė dabigatrano eteksilato nauda insulto ir SE profilaktikai bei ICH rizikos mažinimui, palyginti su varfarinu, išlieka atskiruose pogrupiuose, pvz., Inkstų funkcijos sutrikimas, amžius, kartu vartojami vaistiniai preparatai, pvz., Agregaciją mažinantys vaistai ar P-gp inhibitoriai. kai kuriems pacientų pogrupiams, vartojant antikoaguliantus, padidėja didelio kraujavimo rizika, dabigatrano eteksilato kraujavimo pertekliaus rizika atsiranda dėl kraujavimo iš virškinimo trakto, paprastai pasireiškiančio per pirmuosius 3–6 mėnesius nuo gydymo pradžios.
Giliųjų venų trombozės (DVT) ir plaučių embolijos (PE) gydymas bei DVT ir PE pasikartojimo prevencija suaugusiesiems (DVT / PE gydymas).
7 lentelėje pateikiami kraujavimo įvykiai, atliekant bendrą RE-COVER ir RE-COVER II pagrindinių tyrimų, kuriuose buvo tiriamas giliųjų venų trombozės (DVT) ir plaučių embolijos (PE) gydymas, analizę. kraujavimas ir bet koks kraujavimas buvo žymiai mažesnis nei vartojant varfariną, kai nominalus alfa lygis buvo 5%.
7 lentelė. Kraujavimo atvejai RE-COVER ir RE-COVER II tyrimuose, kuriuose buvo tiriamas giliųjų venų trombozės (DVT) ir plaučių embolijos (PE) gydymas.
Abiejų gydymo būdų kraujavimas skaičiuojamas nuo pirmojo dabigatrano eteksilato ar varfarino vartojimo nutraukus parenteralinį gydymą (tik geriamasis gydymo laikotarpis). Tai apima visus kraujavimo atvejus, atsiradusius gydymo dabigatrano eteksilatu metu. Įtraukiami visi kraujavimo atvejai, atsiradę gydymo varfarinu metu, išskyrus tuos, kurie pasireiškė sutapus tarp varfarino ir parenteralinio gydymo.
Pagrindiniai kraujavimo reiškiniai buvo apibrėžti vadovaujantis Tarptautinės trombozės ir hemostazės draugijos rekomendacijomis. Kraujavimo įvykis buvo laikomas dideliu, jei jis atitiko bent vieną iš šių kriterijų:
• Mirtinas kraujavimas
• Simptominis kraujavimas „kritinėje zonoje ar organe, pvz., Intrakranijinėje, intraspinalinėje, intraokulinėje, retroperitoninėje, intraartikulinėje ar perikardinėje ar intramuskulinėje, turinčioje skyrių sindromą. Kad kraujavimas kritinėje zonoje ar organe būtų laikomas dideliu, jis turėjo būti susijęs su situacija.simptominė klinika
• Kraujavimas, dėl kurio hemoglobino kiekis sumažėjo 20 g / l (1,24 mmol / l) ar daugiau, arba dėl kurio buvo perpilta 2 ar daugiau viso kraujo ar raudonųjų kraujo kūnelių vienetų.
8 lentelėje parodyti kraujavimo įvykiai pagrindiniame RE-MEDY tyrime, kurio metu buvo patikrinta giliųjų venų trombozės (DVT) ir plaučių embolijos (PE) prevencija. Kai kurie kraujavimo atvejai (dideli, kliniškai reikšmingi ir bet koks kraujavimas) buvo žymiai mažesni už vardinį alfa 5%, gydant dabigatrano eteksilatu, palyginti su pacientais, gydytais varfarinu.
8 lentelė. Kraujavimo įvykiai RE-MEDY tyrime, kurio metu buvo patikrinta giliųjų venų trombozės (DVT) ir plaučių embolijos (PE) prevencija.
* HR neįvertinamas, nes nėra įvykių vienoje iš dviejų kohortų / procedūrų
Pagrindinių kraujavimo reiškinių apibrėžimas buvo atliktas vadovaujantis Tarptautinės trombozės ir hemostazės draugijos rekomendacijomis, aprašytomis RECOVER ir RECOVER II.
9 lentelėje parodyti kraujavimo įvykiai pagrindiniame RE-SONATE tyrime, kurio metu buvo patikrinta giliųjų venų trombozės (DVT) ir plaučių embolijos (PE) prevencija. Pagrindinio / kliniškai reikšmingo kraujavimo derinio procentas ir bet kokio kraujavimo procentas buvo reikšmingi mažesnis, kai nominalus alfa lygis yra 5% pacientų, vartojusių placebą, palyginti su pacientais, vartojančiais dabigatrano eteksilatą.
9 lentelė. Kraujavimo atvejai RE-SONATE tyrime, kurio metu buvo patikrinta giliųjų venų trombozės (DVT) ir plaučių embolijos (PE) prevencija.
* Širdies ritmas neįvertinamas, nes nėra įvykio vienoje iš dviejų procedūrų
Pagrindinių kraujavimo reiškinių apibrėžimas buvo atliktas vadovaujantis Tarptautinės trombozės ir hemostazės draugijos rekomendacijomis, aprašytomis RECOVER ir RECOVER II.
Širdies smūgis
Insulto ir sisteminės embolijos prevencija suaugusiems pacientams, sergantiems ne vožtuvų prieširdžių virpėjimu (NAVF), turintiems vieną ar daugiau rizikos veiksnių
RE-LY tyrime, palyginti su varfarinu, metinis miokardo infarkto dažnis dabigatrano eteksilatui padidėjo nuo 0,64% (varfarinas) iki 0,82% (dabigatrano eteksilatas 110 mg du kartus per parą) / 0,81% (150 mg dabigatrano eteksilato du kartus per parą) ( žr. 5.1 skyrių).
Giliųjų venų trombozės (DVT) ir plaučių embolijos (PE) gydymas bei DVT ir PE pasikartojimo prevencija suaugusiesiems (DVT / PE)
Trijuose aktyviai kontroliuojamuose tyrimuose buvo nustatytas didesnis MI dažnis pacientams, vartojantiems dabigatrano eteksilatą, nei vartojusiems varfariną: 0,4%, palyginti su 0,2% trumpalaikiais RE-COVER ir RE-COVER II; ir 0,8%, palyginti su 0,1% ilgalaikio RE-MEDY tyrimo metu. Šiame tyrime padidėjimas buvo statistiškai reikšmingas (p = 0,022).
RE-SONATE tyrime, kuriame dabigatrano eteksilatas buvo lyginamas su placebu, MI dažnis buvo 0,1% pacientų, gydytų dabigatrano eteksilatu, ir 0,2% pacientų, vartojusių placebą (žr. 4.4 skyrių).
Vaikų populiacija (DVT / PE)
Klinikinio tyrimo 1160,88 metu iš viso 9 paaugliai (nuo 12 metų iki pilvo skausmo; diskomfortas pilve) ir 1 pacientas (11,1%) po gydymo patyrė sunkų nesusijusį nepageidaujamą reiškinį (VTE pasikartojimą kojoje), daugiau praėjus 3 dienoms po dabigatrano eteksilato vartojimo nutraukimo.
Pranešimas apie įtariamas nepageidaujamas reakcijas
Svarbu pranešti apie įtariamas nepageidaujamas reakcijas, atsiradusias po vaistinio preparato registravimo, nes tai leidžia nuolat stebėti vaisto naudos ir rizikos santykį. Sveikatos priežiūros specialistų prašoma pranešti apie bet kokias įtariamas nepageidaujamas reakcijas per nacionalinę pranešimo sistemą. "Adresas https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Perdozavimas
Didesnės nei rekomenduojamos dabigatrano eteksilato dozės padidina paciento kraujavimo riziką.
Jei įtariamas perdozavimas, krešėjimo tyrimai gali padėti nustatyti kraujavimo riziką (žr. 4.4 ir 5.1 skyrius). Kiekybinis kalibruotas dTT tyrimas arba pakartotiniai dTT matavimai leidžia numatyti, kada bus pasiektas tam tikras dabigatrano kiekis (žr. 5.1 skyrių), net jei buvo imtasi kitų priemonių, pvz. dializė.
Dėl per didelio antikoagulianto gali tekti nutraukti gydymą Pradaxa. Specifinio dabigatrano priešnuodžio nėra. Jei atsiranda kraujavimo komplikacijų, gydymą reikia nutraukti ir ištirti kraujavimo priežastį, kadangi dabigatranas daugiausia išsiskiria per inkstus, reikia išlaikyti tinkamą diurezę. Gydytojo nuožiūra reikia imtis tinkamo palaikomojo gydymo, pvz., Chirurginės hemostazės ir kraujo tūrio atkūrimo.
Galima apsvarstyti aktyvuoto protrombino komplekso (pvz., FEIBA) arba rekombinantinio VIIa faktoriaus koncentratus arba II, IX ir X krešėjimo faktorių koncentratus. Yra keletas eksperimentinių įrodymų, patvirtinančių šių vaistų vaidmenį neutralizuojant antikoaguliantinį dabigatrano poveikį, tačiau duomenų apie jų naudingumą klinikinėje aplinkoje ir galimą atsinaujinančios tromboembolijos riziką yra labai nedaug. Po vartojimo krešėjimo testai gali tapti nepatikimi. vaistų, prieštaraujančių antikoaguliantų poveikiui. Aiškinant šių bandymų rezultatus reikia būti atsargiems. Taip pat reikia apsvarstyti trombocitų koncentratų skyrimą, jei atsiranda trombocitopenija arba buvo naudojami ilgai veikiantys trombocitų agregaciją mažinantys vaistai. Visas simptominis gydymas turi būti atliekamas pagal gydytojo sprendimą.
Priklausomai nuo vietos, esant dideliam kraujavimui, reikia apsvarstyti galimybę konsultuotis su krešėjimo ekspertais.
Kadangi baltymų jungiasi mažai, dabigatraną galima dializuoti; klinikinė patirtis, įrodanti šio metodo naudingumą klinikiniuose tyrimuose, yra ribota (žr. 5.2 skyrių).
05.0 FARMAKOLOGINĖS SAVYBĖS
05.1 Farmakodinaminės savybės
Farmakoterapinė grupė - antitrombotiniai vaistai, tiesioginiai trombino inhibitoriai.
ATC kodas: B01AE07.
Veiksmo mechanizmas
Dabigatrano eteksilatas yra mažos molekulės provaistas, kuris neturi jokio farmakologinio poveikio. Išgertas dabigatrano eteksilatas greitai absorbuojamas ir paverčiamas dabigatranu hidrolizės būdu plazmoje ir kepenyse esterio katalizės būdu. Dabigatranas yra stiprus tiesioginis, konkurencingas, grįžtamasis trombino inhibitorius ir yra pagrindinė veiklioji medžiaga, randama plazmoje.
Kadangi trombinas (serino proteazė) leidžia fibrinogeną paversti fibrinu krešėjimo kaskadoje, jo slopinimas neleidžia susidaryti trombams. Dabigatranas slopina laisvą trombiną, fibrino surištą trombiną ir trombino sukeltą trombocitų agregaciją.
Farmakodinaminis poveikis
Tyrimai su gyvūnais in vivo Ir ex vivo įrodė antitrombozinį veiksmingumą ir antikoaguliantinį aktyvumą, kai dabigatranas buvo sušvirkštas į veną, ir dabigatrano eteksilatas, išgertas į veną, įvairiais trombozės gyvūnais modeliais.
Remiantis II fazės tyrimų duomenimis, yra aiški sąsaja tarp dabigatrano koncentracijos plazmoje ir antikoagulianto poveikio. Dabigatranas pailgina trombino laiką (TT), ECT ir aPTT.
Atlikus praskiestos plazmos dabigatrano trombino laiko (dTT) tyrimą, apskaičiuota dabigatrano koncentracija plazmoje, kurią galima palyginti su numatoma dabigatrano koncentracija plazmoje.
ECT gali tiesiogiai įvertinti tiesioginių trombino inhibitorių aktyvumą.
APTT testas yra plačiai naudojamas ir apytiksliai parodo antikoaguliacinio poveikio, pasiekto naudojant dabigatraną, intensyvumą. Tačiau aPTT testas pasižymi ribotu jautrumu ir nėra skirtas tiksliam antikoaguliacinio poveikio kiekiui įvertinti, ypač esant didelei koncentracijai plazmoje . dabigatranas.Padidėjusios aPTT vertės turėtų būti aiškinamos atsargiai.
Apskritai galima teigti, kad šie antikoaguliantų aktyvumo matavimai atspindi dabigatrano koncentraciją ir gali pateikti gaires, kaip įvertinti kraujavimo riziką, t. Y. Viršyti 90 -ąją procentilės dabigatrano koncentracijos ribą per mažiausią laiką arba išmatuotą aPTT. su padidėjusia kraujavimo rizika.
Pirminė venų tromboembolijos prevencija ortopedinėje chirurgijoje
Esant pusiausvyros būsenai (po 3 dienų), geometrinis dabigatrano koncentracijos plazmoje didžiausias laikas, išmatuotas praėjus maždaug 2 valandoms po 220 mg dabigatrano eteksilato pavartojimo, buvo 70,8 ng / ml, o intervalas-35, 2–162 ng / ml ( 25–75 procentilis).
Geometrinis dabigatrano koncentracijos vidurkis per mažiausią laiką, išmatuotas dozavimo laikotarpio pabaigoje (t. Y. Praėjus 24 valandoms po 220 mg dabigatrano dozės), buvo vidutiniškai 22,0 ng / ml, o diapazonas-13, 0-35,7 ng / ml ( 25–75 procentilis).
Pacientams, gydytiems VTE profilaktikai po klubo ar kelio sąnario keitimo operacijos, skiriant 220 mg dabigatrano eteksilato vieną kartą per parą,
• 90-asis dabigatrano koncentracijos plazmoje procentilis, matuojamas per mažiausią laiką (20–28 val. Po ankstesnės dozės), buvo 67 ng / ml (žr. 4.4 ir 4.9 skyrius),
• 90-asis aPTT procentilis mažiausiai (20–28 valandos po ankstesnės dozės) buvo 51 sekundė arba 1,3 karto viršija viršutinę normos ribą.
ECT nebuvo matuojamas pacientams, gydytiems VTE profilaktikai po klubo ar kelio sąnario keitimo operacijos, skiriant 220 mg dabigatrano eteksilato vieną kartą per parą.
Insulto ir ES profilaktika suaugusiems pacientams, sergantiems NVNU, turintiems vieną ar daugiau rizikos veiksnių
Esant pusiausvyrai, geometrinis dabigatrano koncentracijos plazmoje didžiausias laikas, matuojamas praėjus maždaug 2 valandoms po 150 mg dabigatrano eteksilato pavartojimo du kartus per parą, buvo 175 ng / ml, o diapazonas -117–275 ng / ml (25–75 procentilis) ). Geometrinis dabigatrano koncentracijos vidurkis mažiausiu metu, išmatuotas ryte, pasibaigus dozavimo intervalui (ty 12 valandų po vakarinės 150 mg dabigatrano dozės), buvo vidutiniškai 91,0 ng / ml, intervalas lygus 61,0 143 ng / ml (25–75 procentilis).
Pacientams, sergantiems NVAF, insulto ir SE profilaktikai gydyti 150 mg dabigatrano eteksilato du kartus per parą,
• 90-asis dabigatrano koncentracijos plazmoje procentilis, išmatuotas per mažiausią laiką (10–16 valandų po ankstesnės dozės), buvo maždaug 200 ng / ml,
• ECT, išmatuotas per mažiausią laiką (10–16 valandų po ankstesnės dozės), daugiau nei maždaug 3 kartus viršijantis viršutinę normos ribą, reiškia 90-ąjį procentilį, stebėtą, kai ECT pailgėja 103 sekundes,
• aPTT santykis, didesnis nei 2 kartus viršijantis viršutinę normos ribą (aPTT pailgėjimas maždaug 80 sekundžių) per mažiausią laiką (10–16 valandų po ankstesnės dozės) atspindi 90-ąjį stebėjimų procentilį.
Giliųjų venų trombozės (DVT) ir plaučių embolijos (PE) gydymas bei DVT ir PE pasikartojimo prevencija suaugusiesiems (DVT / PE)
Pacientams, gydytiems DVT ir PE, skiriant 150 mg dabigatrano eteksilato du kartus per parą, geometrinis dabigatrano koncentracijos vidurkis per mažiausią laiką, išmatuotas per 10–16 valandų po dozės, pasibaigus dozavimo intervalui (t. Y. 12 valandų po vakaro) 150 mg dabigatrano dozė), buvo 59,7 ng / ml, diapazonas 38,6–94,5 ng / ml (25–75 procentile).
• 90-asis dabigatrano koncentracijos plazmoje procentilis, išmatuotas per mažiausią laiką (10–16 valandų po ankstesnės dozės), buvo maždaug 146 ng / ml,
• ECT, išmatuotas per mažiausią laiką (10–16 valandų po ankstesnės dozės), daugiau nei maždaug 2,3 karto didesnis už pradinę vertę, nurodo 90-ąjį procentilį, pastebėtą, kai ECT pailgėja 74 sekundes,
• 90-asis aPTT procentilis mažiausiai (10–16 valandų po ankstesnės dozės) buvo 62 sekundės arba 1,8 karto didesnis už pradinę vertę.
Farmakokinetinių duomenų apie pacientus, gydomus siekiant išvengti DVT ir PE pasikartojimo, skiriant 150 mg dabigatrano eteksilato du kartus per parą, nėra.
Klinikinis veiksmingumas ir saugumas
Etninės kilmės
Tarp baltų, afroamerikiečių, ispanų, japonų ar kinų pacientų nepastebėta jokių svarbių etninių skirtumų.
Klinikiniai venų tromboembolijos (VTE) profilaktikos tyrimai po didelių sąnarių pakeitimo operacijų
Dviejų didelių atsitiktinių imčių lygiagrečių grupių dvigubai aklų dozės patvirtinimo tyrimų metu pacientai, kuriems buvo atlikta didelė ortopedinė operacija (vienas skirtas kelio sąnario keitimo operacijai, o kitas-klubo sąnario pakeitimo operacijai), buvo gydomi 75 mg arba 110 mg Pradaxa per 1- Praėjus 4 valandoms po operacijos ir po to 150 arba 220 mg vieną kartą per parą, hemostazė įvertinta normaliai arba 40 mg enoksaparino dieną prieš operaciją, taigi ir kasdien.
RE-MODEL tyrimo (kelio sąnario pakeitimo) metu gydymo trukmė buvo 6–10 dienų, o RE-NOVATE tyrimo (klubo sąnario pakeitimo) atveju-28–35 dienos. Iš viso buvo gydoma atitinkamai 2076 (klubo sąnario keitimas). Kelio) ir 3494 (klubo sąnario pakeitimo) pacientai.
Visų VTE epizodų derinys (įskaitant PE, proksimalinę ir distalinę GVT, simptominę ir besimptomę, nustatytą atliekant įprastą venografiją) ir mirtingumas dėl visų priežasčių buvo pagrindiniai abiejų tyrimų rezultatai.
Visų pagrindinių VTE epizodų derinys (įskaitant PE, proksimalinę ir distalinę GVT, tiek simptominę, tiek besimptomę, nustatytą atliekant įprastą venografiją) ir su VTE susijęs mirtingumas buvo antrinė vertinamoji baigtis, kuri buvo laikoma svarbesne klinikine reikšme.
Abiejų tyrimų rezultatai parodė, kad 220 mg ir 150 mg Pradaxa antitrombozinis poveikis statistiškai nenusileido enoksaparino poveikiui bendrai VTE ir mirštamumui nuo visų priežasčių. Apskaičiuotas pagrindinių VTE epizodų dažnis yra su VTE susijęs mirtingumas 150 mg dozė buvo šiek tiek blogesnė nei vartojant enoksaparino (10 lentelė). Geresni rezultatai buvo gauti vartojant 220 mg dozę, kai apskaičiuotas pagrindinių VTE epizodų dažnis buvo šiek tiek geresnis nei vartojant enoksaparino (10 lentelė).
Klinikiniai tyrimai buvo atlikti pacientų grupėje, kurių vidutinis amžius> 65 metai.
3 fazės klinikinių tyrimų metu vyrų ir moterų veiksmingumo ir saugumo skirtumų nenustatyta.
Iš pacientų, dalyvaujančių RE-MODEL ir RE-NOVATE tyrimuose (5539 gydomi pacientai), 51% sirgo kartu gresiančia hipertenzija, 9%-gretutiniu diabetu, 9%-vainikinių arterijų liga, 20% sirgo venų nepakankamumu. . Įrodyta, kad nė viena iš šių sąlygų neturi įtakos dabigatrano poveikiui VTE profilaktikai ar kraujavimo dažnumui.
Pagrindinės VTE ir su VTE susijusios mirtingumo baigties duomenys buvo homogeniški, palyginti su pirminiu veiksmingumo baigtimi, ir pateikti 10 lentelėje.
Bendros VTE ir visų mirtingumo priežasčių parametrų duomenys pateikti 11 lentelėje.
Duomenys apie kraujavimo galutinius taškus, kurie laikomi dideliais, išvardyti 12 lentelėje.
10 lentelė. Didelio VTE ir su VTE susijusio mirtingumo analizė gydymo laikotarpiu RE-MODEL ir RE-NOVATE ortopedinės chirurgijos tyrimuose
11 lentelė. Bendros VTE ir mirtingumo nuo visų priežasčių analizė gydymo laikotarpiu atliekant ortopedinės chirurgijos tyrimus RE-NOVATE ir RE-MODEL
12 lentelė. Pagrindiniai kraujavimo epizodai (ESM) po gydymo atskiruose RE-MODEL ir RE-NOVATE tyrimuose
Insulto ir ES profilaktika suaugusiems pacientams, sergantiems NVNU, turintiems vieną ar daugiau rizikos veiksnių
Klinikiniai dabigatrano eteksilato veiksmingumo įrodymai gauti iš atsitiktinių imčių ilgalaikio antikoaguliantų gydymo (RE-LY) tyrimo, daugelio centrų, tarptautinio, atsitiktinių imčių, lygiagrečios grupės tyrimo, kuriame buvo lyginamos dvi apakintos dabigatrano eteksilato dozės (110 mg ir 150 mg). mg du kartus per parą), palyginti su atviru varfarinu, pacientams, kuriems yra prieširdžių virpėjimas ir vidutinio sunkumo ar didelė insulto ir SE rizika. Pagrindinis tyrimo tikslas buvo nustatyti, ar dabigatrano eteksilatas ne mažesnis už varfariną, mažinant sudėtinį insulto ir SE galutinį rodiklį. Taip pat buvo įvertintas statistinis pranašumas.
RE-LY tyrime iš viso atsitiktine tvarka buvo atrinkti 18 113 pacientai, kurių amžiaus vidurkis buvo 71,5 metų, o CHADS2 vidurkis-2,1. Pacientų populiacija buvo 64% vyrų, 70%-baltųjų ir 16%-azijiečių. atsitiktinės atrankos būdu į varfariną, vidutinis laiko procentas terapiniame diapazone (TTR) (INR 2-3) buvo 64,4% (TTR mediana 67%).
RE-LY tyrimas parodė, kad dabigatrano eteksilatas, vartojamas 110 mg du kartus per parą, yra ne mažesnis už varfariną insulto ir SE profilaktikai tiriamiesiems, kuriems yra prieširdžių virpėjimas, sumažėjusi ICH, bendro kraujavimo ir didelio kraujavimo rizika. . 150 mg dozė du kartus per parą, palyginti su varfarinu, žymiai sumažina išeminio ir hemoraginio insulto, kraujagyslių mirties, ICH ir bendro kraujavimo riziką. Vartojant šią dozę, didelio kraujavimo dažnis buvo panašus į varfarino. Miokardo infarkto dažnis šiek tiek padidėjo vartojant dabigatrano eteksilatą du kartus per parą ir 150 mg du kartus per parą, palyginti su varfarinu (santykinė rizika atitinkamai 1,29; p = 0,0929 ir santykinė rizika). 1,27; p = 0,1240) Geriau stebint INR, pastebėta dabigatrano eteksilato nauda, palyginti su varfarino sumažėjimu.
13-15 lentelėse pateikiama išsami informacija apie pagrindines išvadas visoje populiacijoje:
13 lentelė. Insulto ar SE dažnio analizė (pirminė vertinamoji baigtis) RE-LY tyrimo laikotarpiu.
% nurodo metinį įvykio dažnumą
14 lentelė. Išeminio ar hemoraginio insulto dažnio analizė RE-LY tyrimo laikotarpiu.
% nurodo metinį įvykio dažnumą
15 lentelė. Visų priežasčių mirtingumo nuo širdies ir kraujagyslių ligų dažnio analizė RE-LY tyrimo laikotarpiu.
% nurodo metinį įvykio dažnumą
16–18 lentelėse pateikiami pagrindiniai veiksmingumo rezultatai ir saugumo baigtis pagrindinėse pogrupiuose:
Pirminė vertinamoji baigtis - insultas ir SE - nebuvo nustatyti jokie pogrupiai (ty amžius, svoris, lytis, inkstų funkcija, etninė priklausomybė ir kt.), Kurių pavojaus santykis būtų kitoks nei varfarino.
16 lentelė. Santykinė rizika ir 95% PI insulto / SE pagal pogrupius
Pagrindinio saugumo baigties didelio kraujavimo atveju pasireiškė sąveika tarp gydymo poveikio ir amžiaus. Santykinė kraujavimo rizika su amžiumi didėjo vartojant dabigatraną, palyginti su varfarinu. Santykinė rizika buvo didesnė ≥ 75 metų pacientams. Kartu vartojant ASR ar klopidogrelio antitrombocitinių preparatų, ESI dažnis tiek dvigubai padidėja, tiek vartojant dabigatrano eteksilatą ir varfariną. Nebuvo reikšmingos sąveikos su gydymo poveikiu inkstų funkcijos pogrupiuose ir CHADS2 balu.
17 lentelė. Santykinė didelio kraujavimo rizika ir 95% PI pagal pogrupius
RELY-ABLE (daugiacentris ilgalaikis pratęsimo gydymas dabigatranu pacientams, sergantiems prieširdžių virpėjimu, kurie baigė RE-LY tyrimą)
RE-LY tyrimo pratęsimas (RELY-ABLE) pateikė papildomų saugumo duomenų apie kohortą pacientų, kurie ir toliau vartojo tą pačią dabigatrano eteksilato dozę pagal paskirtą gydymą RE-LY tyrime. Pacientai galėjo gauti RELY-ABLE. jei paskutinio RE-LY tyrimo vizito metu jie visam laikui nebuvo nutraukę tiriamojo vaistinio preparato. LY tyrimas, skirtas ilgesniam stebėjimui iki 43 mėnesių po RE-LY (vidutinis stebėjimas RE-LY + RELY-ABLE, 4,5 metų). Buvo įtraukti 5897 pacientai, ty 49% pacientų, iš pradžių atsitiktinai atrinktų gauti dabigatrano eteksilato RE-LY tyrime ir 86% pacientų, tinkamų RELY-ABLE.
Per papildomus 2,5 gydymo RELY-ABLE tyrime, kai didžiausia ekspozicija buvo ilgesnė nei 6 metai (bendra RE-LY + RELY-ABLE ekspozicija), patvirtintas ilgalaikis dabigatrano eteksilato saugumo profilis mg paros dozės ir 150 mg stiprumo. Naujų saugumo duomenų nepastebėta.
Įvykių, įskaitant didelius kraujavimo atvejus ir kitus kraujavimo atvejus, dažnis atitiko RE-LY tyrimo metu pastebėtus atvejus.
Vaikų populiacija
Europos vaistų agentūra atleido nuo įpareigojimo pateikti Pradaxa tyrimų su visais vaikų populiacijos pogrupiais rezultatus, skirtus tromboembolinių epizodų profilaktikai pagal patvirtintą indikaciją (informaciją apie vartojimą vaikams žr. 4.2 skyriuje).
Etninė kilmė (insulto prevencija pacientams, sergantiems prieširdžių virpėjimu)
Tarp kaukazo, afroamerikiečių, ispanų, japonų ar kinų pacientų etninių skirtumų nepastebėta.
Klinikinis veiksmingumas ir saugumas (gydymas DVT / PE)
Suaugusiųjų giliųjų venų trombozės (DVT) ir plaučių embolijos (PE) gydymas (DVT / PE gydymas).
Veiksmingumas ir saugumas buvo tiriami dviejuose daugiacentriuose, atsitiktinių imčių, dvigubai akluose, lygiagrečių grupių, RE-COVER ir RE-COVER II dviejuose tyrimuose. Šiuose tyrimuose buvo lyginamas dabigatrano eteksilatas (150 mg du kartus per parą) su varfarinu (INR tikslas 2, 0-3,0 ) pacientams, sergantiems DVT ir (arba) ūmine PE. Pagrindinis šių tyrimų tikslas buvo nustatyti, ar dabigatrano eteksilatas yra ne mažesnis už varfariną, nes sumažėja sudėtinės pirminės galutinės DVT ir (arba) simptominės PE atsinaujinimo pasekmės. mirčių per 6 mėnesius nuo gydymo.
RE-COVER ir RE-COVER II tyrimuose 5 153 pacientai buvo atsitiktinai parinkti, o 5 107-gydyti.
Gydymo fiksuota doze dabigatranu trukmė buvo 174,0 dienos be krešėjimo kontrolės. Pacientams, atsitiktinai atrinktiems į varfariną, terapinis intervalas (INR nuo 2,0 iki 3,0) buvo 60,6%.
Tyrimai parodė, kad gydymas dabigatrano eteksilatu po 150 mg du kartus per parą buvo ne mažesnis už gydymą varfarinu (RE-COVER ir RE-COVER II ne mažesnio lygio riba: 3,6 rizikos skirtumo ir 2,75 pagal pavojaus santykį).
18 lentelė. RE-COVER ir RE-COVER II tyrimų pirminio ir antrinio veiksmingumo vertinamųjų baigčių (VTE apima DVT ir (arba) PE) analizė iki gydymo laikotarpio pabaigos
Etninė kilmė (DVT / PE gydymas)
Tarp kaukazo, afroamerikiečių, ispanų, japonų ar kinų pacientų etninių skirtumų nepastebėta.
Vaikai (DVT / PE gydymas)
Europos vaistų agentūra atidėjo įpareigojimą pateikti Pradaxa tyrimų su visais vaikų populiacijos pogrupiais, gydant DVT / PE, rezultatus (informaciją apie naudojimą vaikams žr. 4.2 skyriuje).
Dabigatrano eteksilato, vartojamo du kartus per parą tris dienas iš eilės (iš viso 6 dozės), pasibaigus standartiniam gydymui antikoaguliantais, farmakokinetika ir farmakodinamika buvo įvertinta atvirame saugumo ir toleravimo tyrime, kuriame dalyvavo 9 kliniškai stabilūs paaugliai (nuo 12 iki 12 metų amžiaus).
Klinikinis veiksmingumas ir saugumas (DVT / PE prevencija)
Suaugusiųjų giliųjų venų trombozės (DVT) ir plaučių embolijos (PE) pasikartojimo prevencija (DVT / PE profilaktika)
Du atsitiktinių imčių lygiagrečios grupės dvigubai akli tyrimai buvo atlikti su pacientais, anksčiau gydytais antikoaguliantais. Varfarino kontroliuojamame RE-MEDY tyrime dalyvavo pacientai, kurie jau buvo gydomi 3–12 mėnesių ir kuriems reikėjo papildomo gydymo antikoaguliantais, placebu kontroliuojamas RE-SONATE tyrimas, kuriame dalyvavo pacientai, jau 6–18 mėnesių gydomi vitamino K inhibitoriais.
RE-MEDY tyrimo tikslas buvo palyginti geriamojo dabigatrano eteksilato (150 mg du kartus per parą) saugumą ir veiksmingumą su varfarinu (tikslinis INR 2,0–3,0), siekiant ilgalaikio gydymo ir simptominių DVT ir (arba) PE recidyvų prevencijos. Iš viso atsitiktinių imčių būdu buvo atrinkti 2866 pacientai, o 2856 buvo gydyti. Gydymo dabigatrano eteksilatu trukmė svyravo nuo 6 iki 36 mėnesių (vidutiniškai 534,0 dienos). Pacientams, atsitiktinai parinktiems į varfariną, terapinis intervalas (INR 2,0–3,0) buvo 64,9%.
RE-MEDY tyrimas parodė, kad gydymas dabigatrano eteksilatu po 150 mg du kartus per parą buvo ne mažesnis už varfariną (ne mažesnės ribos: 2,85 pavojaus santykio ir 2,8 rizikos skirtumo).
19 lentelė. Pirminio ir antrinio veiksmingumo vertinamųjų baigčių (VTE apima DVT ir (arba) PE) analizė iki RE-MEDY tyrimo laikotarpio po gydymo pabaigos
RE-SONATE tyrimo tikslas buvo įvertinti dabigatrano eteksilato pranašumą prieš placebą, siekiant užkirsti kelią simptominio DVT ir (arba) PE recidyvui pacientams, kurie jau buvo baigę 6–8 mėnesių AVK gydymą. Gydymas apėmė 6 mėnesius. vartojant 150 mg dabigatrano eteksilato du kartus per parą, nereikia stebėti.
RE-SONATE tyrimas parodė, kad dabigatrano eteksilatas buvo pranašesnis už placebą užkertant kelią simptominių DVT / PE epizodų, įskaitant mirtis dėl nepaaiškinamų priežasčių, pasikartojimui, o rizika sumažėjo nuo 5,6% iki 0,4% (santykinis sumažėjimas 92%, atsižvelgiant į pavojaus santykį). gydymo laikotarpis (p
Tyrimas apėmė stebėjimo stebėjimo laikotarpį 12 mėnesių po gydymo pabaigos. Nutraukus tyrimą, vaisto poveikis išliko iki stebėjimo laikotarpio pabaigos, o tai rodo, kad pradinis gydymo dabigatranu poveikis išlieka. Jokio atšokimo efekto nepastebėta. Stebėjimo laikotarpio pabaigoje VTE reiškiniai pacientams, gydytiems dabigatrano eteksilatu, buvo 6,9%, palyginti su 10,7%, palyginti su placebo grupe (pavojaus santykis 0,61 (95% PI 0,42,0, 88), p = 0,0082).
20 lentelė. Pirminio ir antrinio veiksmingumo vertinamųjų baigčių analizė (VTE apima DVT ir (arba) PE) iki RE-SONATE tyrimo laikotarpio pabaigos
Etninė kilmė (DVT / PE prevencija)
Kliniškai reikšmingų etninių skirtumų tarp kaukazo, afroamerikiečių, ispanų, japonų ar kinų pacientų nepastebėta.
Vaikų populiacija (DVT / PE profilaktika)
Europos vaistų agentūra atidėjo įpareigojimą pateikti Pradaxa tyrimų su visais vaikų populiacijos pogrupiais rezultatus, susijusius su DVT / PE profilaktika (informaciją apie naudojimą vaikams žr. 4.2 skyriuje).
Klinikiniai tyrimai, skirti tromboembolijos profilaktikai pacientams, sergantiems širdies vožtuvų protezais
II fazės tyrime buvo vertinami dabigatrano eteksilatas ir varfarinas iš viso 252 pacientams, kuriems iš dalies neseniai buvo atlikta mechaninė vožtuvų operacija (t. Vartojant dabigatrano eteksilatą, pastebėta daugiau tromboembolinių reiškinių (daugiausia insulto ir simptominių / besimptomių vožtuvų trombozės) ir daugiau kraujavimo atvejų nei vartojant varfarino. Iš karto po operacijos sergantiems pacientams didelis kraujavimas pasireiškė daugiausia kaip hemoraginis perikardo išsiliejimas, ypač pacientams, pradėjusiems dabigatrano eteksilatą netrukus (ty 3 dieną) po širdies vožtuvo protezavimo operacijos (žr. 4.3 skyrių).
05.2 Farmakokinetinės savybės
Išgertas dabigatrano eteksilatas greitai ir visiškai virsta dabigatranu, kuris yra aktyvioji plazmos forma. Pagrindinė metabolinė reakcija yra provaisto vaisto dabigatrano eteksilato skilimas hidrolizuojant esterą katalizuojant į veikliąją medžiagą. Absoliutus biologinis dabigatrano prieinamumas, išgėrus Pradaxa, yra maždaug 6,5%.
Išgėrus Pradaxa sveikiems savanoriams, dabigatrano farmakokinetikos pobūdis plazmoje būdingas greitu koncentracijos plazmoje padidėjimu, o Cmax pasiekė 0,5 - 2,0 val.
Absorbcija
Tyrimas, kuriame buvo įvertinta dabigatrano eteksilato absorbcija po operacijos, praėjus 1–3 valandoms po operacijos, parodė santykinai lėtą absorbciją, palyginti su sveikų savanorių, ir parodė koncentracijos plazmoje laiko profilį be didelės didžiausios koncentracijos plazmoje. Didžiausia koncentracija plazmoje pasiekiama praėjus 6 valandoms po vartojimo pooperaciniu laikotarpiu dėl tokių veiksnių kaip anestezija, žarnyno parezė ir chirurginis poveikis, neatsižvelgiant į geriamojo vaistinio preparato formą. Tolesniame tyrime buvo įrodyta, kad lėta ir uždelsta absorbcija paprastai būna tik operacijos dieną, o dienomis po to, kai dabigatranas absorbuojamas greitai, o didžiausia koncentracija plazmoje pasiekiama praėjus 2 valandoms po vaisto vartojimo.
Maistas nekeičia dabigatrano eteksilato biologinio prieinamumo, tačiau 2 valandomis atitolina maksimalios koncentracijos plazmoje pasiekimo laiką.
Kai granulės imamos be HPMC (hidroksipropilmetilceliuliozės) kapsulės, biologinis prieinamumas per burną gali padidėti 75%, palyginti su etalonine kompozicija su kapsule. Todėl klinikinio naudojimo metu visada turi būti išsaugotas HPMC kapsulių vientisumas, kad būtų išvengta netyčinio dabigatrano eteksilato biologinio prieinamumo padidėjimo. Todėl pacientams reikia patarti neatidaryti kapsulių ir nevartoti jų vien tik (pvz., Barstyti ant maisto ar pilti į gėrimą) (žr. 4.2 skyrių).
Paskirstymas
Pastebėta maža koncentracija nepriklausomai (34–35%) dabigatrano prisijungimo prie žmogaus plazmos baltymų. Dabigatrano pasiskirstymo tūris 60–70 l viršija viso kūno skysčių tūrį, o tai rodo vidutinį dabigatrano pasiskirstymą audiniuose.
Cmax ir plotas po koncentracijos ir laiko kreive plazmoje buvo proporcingas dozei. Dabigatrano koncentracija plazmoje sumažėjo dvigubai, o sveikų, senyvų žmonių pusinės eliminacijos laikas buvo 11 valandų. Po daugelio dozių buvo pastebėtas „galutinis pusinės eliminacijos laikas-maždaug 12–14 valandų“. Pusinės eliminacijos laikas nepriklausė nuo dozės. Pusinės eliminacijos laikas pailgėja, jei yra sutrikusi inkstų funkcija, kaip parodyta 21 lentelėje.
Biotransformacija
Dabigatrano metabolizmas ir išsiskyrimas buvo tiriamas pavartojus vieną intraveninę radioaktyvaus dabigatrano dozę sveikiems vyrams. Suleidus į veną, iš dabigatrano gautas radioaktyvumas daugiausia pašalinamas su šlapimu (85%). Apskaičiuota, kad su išmatomis išsiskiria 6% suvartotos dozės, o bendras radioaktyvumo atsigavimas svyravo nuo 88 iki 94% suvartotos dozės per 168 valandas po vartojimo.
Dabigatranas konjuguojamas ir susidaro farmakologiškai aktyvūs acilglukuronidai. Yra keturi acilgliukuronidų 1-O, 2-O, 3-O, 4-O padėties izomerai, kurių kiekvienas sudaro mažiau nei 10% viso plazmoje esančio dabigatrano. Kitų metabolitų pėdsakai aptinkami tik labai jautriais analizės metodais. Dabigatranas beveik nepakitęs išsiskiria su šlapimu maždaug 100 ml / min greičiu, atitinkančiu glomerulų filtracijos greitį.
Specialios populiacijos
Inkstų nepakankamumas
I fazės tyrimų metu, išgėrus Pradaxa, dabigatrano ekspozicija (AUC) yra maždaug 2,7 karto didesnė savanoriams, kuriems yra vidutinio sunkumo inkstų funkcijos sutrikimas (CrCL nuo 30 iki 50 ml / min.), Nei tiems, kurių inkstų funkcija sutrikusi.
Kai kuriems savanoriams, sergantiems sunkiu inkstų nepakankamumu (CrCL 10–30 ml / min.), Dabigatrano ekspozicija (AUC) buvo maždaug 6 kartus didesnė, o pusinės eliminacijos periodas - maždaug 2 kartus ilgesnis nei nustatyta pacientams, kuriems nėra inkstų nepakankamumo. (Žr. 4.2, 4.3 ir 4.4 skyrius).
21 lentelė. Bendras dabigatrano pusinės eliminacijos laikas sveikiems asmenims ir asmenims, kurių inkstų funkcija sutrikusi.
Dabigatrano klirensas hemodializės būdu buvo tiriamas 7 pacientams, sergantiems galutinės stadijos lėtiniu inkstų nepakankamumu (ESRD) be prieširdžių virpėjimo. Dializė buvo atlikta, kai dializato srautas buvo 700 ml / min., Keturias valandas, o kraujotaka-200 ml / min. Ir 350–390 ml / min. Dėl to dabigatrano koncentracija buvo pašalinta atitinkamai nuo 50% iki 60%. Dializės būdu pašalintas medžiagos kiekis yra proporcingas kraujo tekėjimo greičiui iki 300 ml / min. Dabigatrano antikoaguliantinis aktyvumas mažėjo, mažėjant koncentracijai plazmoje, o procedūros metu farmakokinetinis / farmakodinaminis ryšys nepasikeitė.
Vidutinis CrCL RE-LY tyrime buvo 68,4 ml / min. Beveik pusė (45,8%) RE -LY pacientų CRL buvo> 50 -
Vidutinis CrCL RE-COVER tyrime buvo 100,4 ml / min. 21,7% pacientų buvo lengvas inkstų funkcijos sutrikimas (CrCL> 50-80 ml / min. Panašios CrCL vertės buvo nustatytos ir RE -COVER II tyrime.
Vidutinis CrCL RE-MEDY ir RE-SONATE tyrimuose buvo atitinkamai 99,0 ml / min. Ir 99,7 ml / min. 22,9% ir 22,5% pacientų CRL> 50
Senyvi pacientai
Specifiniai I fazės farmakokinetikos tyrimai, atlikti vyresnio amžiaus žmonėms, parodė, kad AUC padidėjo 40–60%, o C - daugiau nei 25%, palyginti su jaunais asmenimis.
Amžiaus įtaka dabigatrano ekspozicijai buvo patvirtinta RE-LY tyrime, kai mažiausia koncentracija buvo maždaug 31% ≥ 75 metų asmenims ir mažesnė-maždaug 22% amžiaus grupėje.
Kepenų funkcijos sutrikimas
12 tiriamųjų, kuriems buvo vidutinio sunkumo kepenų funkcijos sutrikimas (Child Pugh B klasė), nei dabigatrano ekspozicijos pokyčių nenustatyta (žr. 4.2 ir 4.4 skyrius).
Kūno svoris
Dabigatrano koncentracija mažiausiu metu buvo maždaug 20% mažesnė pacientams, kurių kūno svoris> 100 kg, palyginti su pacientais, kurių kūno svoris buvo nuo 50 iki 100 kg. Daugumos pacientų (80,8%) kūno svoris buvo ≥ 50 kg ir
Tipas
Pirminės VTE epizodų prevencijos metu veikliosios medžiagos ekspozicija moterims buvo maždaug 40–50% didesnė, todėl dozės koreguoti nerekomenduojama. Moterims, sergančioms prieširdžių virpėjimu, veikliosios medžiagos veikliosios medžiagos ekspozicija buvo 30% didesnė nei vyrams tiek mažiausiu metu, tiek po dozavimo. Dozės koreguoti nerekomenduojama (žr. 4.2 skyrių).
etninis fonas
Tarp baltų, afroamerikiečių, ispanų, japonų ar kinų pacientų tarp etninių grupių reikšmingų skirtumų, susijusių su dabigatrano farmakokinetika ir farmakodinamika, nepastebėta.
Farmakokinetinė sąveika
Vaistas dabigatrano eteksilatas yra išleidimo nešiklio P-gp substratas, bet ne dabigatranas. Dėl šios priežasties kartu su P-gp transporterio inhibitoriais (amiodaronu, verapamiliu, klaritromicinu, chinidinu, donedaronu, tikagreloru ir ketokonazolu) ir kartu su induktoriais (rifampicinu) (žr. 4.2, 4.4 ir 4.5 skyrius).
Sąveikos tyrimai in vitro neparodė pagrindinių citochromo P450 izofermentų slopinimo ar indukcijos. Tai patvirtino in vivo tyrimai, atlikti su sveikais savanoriais, kuriuose nenustatyta sąveika tarp šio gydymo ir šių veikliųjų medžiagų: atorvastatino (CYP3A4), digoksino (sąveika su transporteriu P-gp) ir diklofenako (CYP2C9).
05.3 Ikiklinikinių saugumo duomenys
Įprastų farmakologinio saugumo, kartotinių dozių toksiškumo ir genotoksinio poveikio ikiklinikinių tyrimų duomenys nerodo jokio ypatingo pavojaus žmonėms.
Kartotinių dozių toksiškumo tyrimų metu pastebėtas poveikis atsirado dėl sustiprėjusio dabigatrano farmakodinaminio poveikio.
Poveikis moterų vaisingumui pasireiškė sumažėjus implantacijai ir padidėjusiam praradimui prieš implantaciją, kai buvo skiriama 70 mg / kg dozė (5 kartus didesnė už ekspoziciją plazmoje). Vartojant toksines motinoms dozes (5–10 kartų didesnė už ekspoziciją plazmoje), žiurkėms ir triušiams stebėtas vaisiaus kūno svorio ir gyvybingumo sumažėjimas, padidėjus vaisiaus pokyčiams. Prieš ir po gimdymo atlikto tyrimo metu pastebėta, kad vaisiaus mirtingumas padidėjo vartojant motinai toksiškas dozes (dozė, atitinkanti ekspoziciją plazmoje 4 kartus didesnė nei nustatyta pacientams).
Visą gyvenimą trunkančio toksiškumo tyrimų su žiurkėmis ir pelėmis metu, esant maksimaliai 200 mg / kg dozei, nenustatyta, kad dabigatranas sukeltų navikų.
Dabigatranas, aktyvi dabigatrano eteksilato mezilato molekulė, yra patvarus aplinkoje.
06.0 FARMACINĖ INFORMACIJA
06.1 Pagalbinės medžiagos
Kapsulės turinys
• Vyno rūgštis
• Arabiška guma
• Hipromeliozė
• Dimetikonas 350
• Talkas
• Hidroksipropilceliuliozė
Kapsulė
• Karageninas
• Kalio chloridas
• Titano dioksidas
• Indigo karminas (E132)
• Saulėlydžio geltona (E110)
• Hipromeliozė
Juodas rašalas spausdinimui
• Šelakas
• Juodasis geležies oksidas (E172)
• Kalio hidroksidas
06.2 Nesuderinamumas
Nėra svarbus.
06.3 Galiojimo laikas
Lizdinė plokštelė ir butelis: 3 metai.
Atidarius buteliuką, vaistinis preparatas turi būti suvartotas per 4 mėnesius.
06.4 Specialios laikymo sąlygos
Lizdinė plokštelė
Laikyti gamintojo pakuotėje, kad preparatas būtų apsaugotas nuo drėgmės.
Butelis
Laikyti gamintojo pakuotėje, kad preparatas būtų apsaugotas nuo drėgmės.
06.5 Pirminės pakuotės pobūdis ir pakuotės turinys
Pakuotės, kuriose yra 10 x 1, 30 x 1 arba 60 x 1 kietų kapsulių, sudėtinė pakuotė, kurioje yra 3 pakuotės po 60 x 1 kietųjų kapsulių (180 kietų kapsulių) ir sudėtinė pakuotė, kurioje yra 2 pakuotės po 50 x 1 kietųjų kapsulių (100 kietų kapsulių)) . Be to, pakuotėse yra 6 baltos aliuminio lizdinės plokštelės, padalijamos iš vienetinės dozės (60 x 1). Lizdinę plokštelę sudaro viršutinis aliuminio sluoksnis, padengtas polivinilchlorido-polivinilacetato kopolimerais (PVCAC akrilatais), liečiantis su produktu, ir apatinis aliuminio sluoksnis, padengtas polivinilchloridu (PVC), liečiantis su produktu.
Polipropileninis buteliukas su užsukamu dangteliu, kuriame yra 60 kietų kapsulių.
Gali būti tiekiamos ne visų dydžių pakuotės.
06.6 Naudojimo ir naudojimo instrukcijos
Naudojant Pradaxa supakuotą į lizdines plokšteles, reikia laikytis šių nurodymų:
• Kietąją kapsulę reikia išimti iš lizdinės plokštelės, pakeliant aliuminio foliją ant nugaros.
• Kietosios kapsulės negalima stumti per lizdinę plokštelę.
• Lizdinės plokštelės aliuminio foliją galima pakelti tik tada, kai reikia kietos kapsulės.
Naudojant kapsules, supakuotas į butelius, reikia laikytis šių nurodymų:
• Butelis atidaromas paspaudus ir pasukant dangtelį.
Nepanaudotą vaistą ir jo atliekas reikia sunaikinti laikantis vietinių taisyklių.
07.0 RINKODAROS TEISĖS TURĖTOJAS
„Boehringer Ingelheim International GmbH“
Binger Str. 173
D-55216 Ingelheim am Rhein
Vokietija
08.0 RINKODAROS TEISĖS NUMERIS
EU/1/08/442/005
038451050
EU/1/08/442/006
038451062
EU/1/08/442/007
038451074
EU/1/08/442/008
038451086
EU/1/08/442/014
038451148
EU/1/08/442/015
EU/1/08/442/018
09.0 RINKODAROS TEISĖS SUTEIKIMO AR PATVIRTINIMO DATA
Registravimo data: 2008 m. Kovo 18 d
Paskutinio atnaujinimo data: 2013 m. Sausio 17 d
10.0 TEKSTO PERŽIŪROS DATA
2014 m. Gruodžio 18 d