Veikliosios medžiagos: gripo vakcina, paruošta iš suskaidytų suskaidytų virusų, inaktyvuota 2015/2016 m. Sezonas
Vaxigrip injekcinė suspensija užpildytame švirkšte
Indikacijos Kodėl vartojamas Vaxigrip? Kam tai?
Vaxigrip yra vakcina.
Ši vakcina padeda apsaugoti jus ar jūsų vaiką nuo gripo.
Vaxigrip vartoti reikia remiantis oficialiomis rekomendacijomis.
Kai žmogui skiriamas Vaxigrip, imuninė sistema (natūrali organizmo gynybos sistema) pasigamina savo apsaugą (antikūnus) nuo ligos. Nė vienas iš vakcinos komponentų negali sukelti gripo.
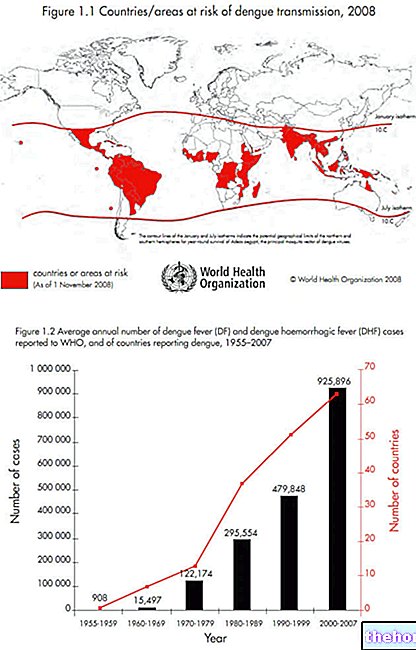
Gripas yra liga, kuri gali greitai plisti ir kurią sukelia skirtingos virusų padermės, kurios gali keistis kiekvienais metais. Štai kodėl jums arba jūsų vaikui gali tekti skiepytis kasmet. "Gripas plinta šaltuoju metų laiku, nuo spalio iki kovo. Jei jūs ar jūsų vaikas nebuvo skiepyti rudenį, vis tiek pagrįsta skiepytis iki pavasario sezono, nes jūs ar jūsų vaikas rizikuojate užsikrėsti gripu iki šio metų laiko. Gydytojas galės patarti, kada geriausia skiepytis.
Vaxigrip skirtas apsaugoti jus ar jūsų vaiką nuo trijų viruso padermių, esančių vakcinoje, maždaug po 2–3 savaičių po vakcinacijos.
Gripo inkubacinis laikotarpis yra kelios dienos, taigi, jei jūs ar jūsų vaikas sirgote gripu prieš pat skiepijimą arba po jo, jūs ar jūsų vaikas vis tiek galite susirgti šia liga.
Vakcina neapsaugos jūsų ar jūsų vaiko nuo peršalimo, net jei kai kurie simptomai yra panašūs į gripo simptomus.
Kontraindikacijos Vaxigrip vartoti negalima
Kad įsitikintumėte, jog Vaxigrip yra tinkama vakcina jums ar jūsų vaikui, svarbu pasakyti gydytojui arba vaistininkui, jei jūs ar jūsų vaikas sergate kokia nors iš toliau išvardytų būklių. Jei kokia nors informacija nėra aiški, paprašykite savo gydytojo ar vaistininko paaiškinimo.
Vaxigrip vartoti negalima
- Jei jūs ar jūsų vaikas esate alergiški (padidėjęs jautrumas):
- veikliosios medžiagos, arba
- bet kuriai pagalbinei šios vakcinos medžiagai (jos išvardytos 6 skyriuje), arba
- bet kuriam komponentui, kurio gali būti labai mažai, pvz., kiaušiniams (ovalbuminui arba vištienos baltymui), neomicinui, formaldehidui ar 9-oktoksinoliui,
- Jei jūs ar jūsų vaikas sergate karščiavimu ar ūmine liga, skiepijimą reikia atidėti, kol jūs ar jūsų vaikas pasveiksite.
Atsargumo priemonės Vartojant prieš vartojant Vaxigrip
Pasitarkite su gydytoju arba vaistininku, prieš pradėdami vartoti Vaxigrip
Prieš skiepydami pasakykite gydytojui, jei jūs ar jūsų vaikas sergate:
- susilpnėjęs imuninis atsakas (imunodeficitas arba imuninę sistemą veikiančių vaistų vartojimas).
- kraujosruvos ar kraujosruvos
Jūsų gydytojas nuspręs, ar jums ar jūsų vaikui skiepytis.
Jei dėl kokių nors priežasčių praėjus kelioms dienoms po vakcinacijos nuo gripo jums ar jūsų vaikui atliekamas kraujo tyrimas, pasakykite gydytojui. Tai svarbu, nes kai kuriems neseniai paskiepytiems pacientams buvo pastebėti klaidingai teigiami rezultatai.
Vaxigrip, kaip ir visos vakcinos, negali visiškai apsaugoti visų skiepytų žmonių.
Sąveika Kokie vaistai ar maistas gali pakeisti Vaxigrip poveikį
Pasakykite gydytojui arba vaistininkui, jei jūs ar jūsų vaikas vartojate ar neseniai vartojote kitų vakcinų ar vaistų,
- Vaxigrip galima švirkšti į kitas galūnes kartu su kitomis vakcinomis, tačiau reikia atsižvelgti į tai, kad tokiu atveju nepageidaujami reiškiniai gali būti intensyvesni.
- Imunologinis atsakas gali susilpnėti gydant imunosupresantais, pvz., Kortikosteroidais, citotoksiniais vaistais ar radioterapija.
Įspėjimai Svarbu žinoti, kad:
Nėštumas ir žindymo laikotarpis
Jeigu esate nėščia, žindote kūdikį, manote, kad galbūt esate nėščia, arba planuojate pastoti, tai prieš vartodama šį vaistą pasitarkite su gydytoju arba vaistininku.
Gripo vakcinos gali būti naudojamos visais nėštumo etapais. Palyginti su pirmuoju ketvirčiu, yra daugiau duomenų apie antrąjį ir trečiąjį ketvirčius; tačiau duomenys apie vakcinų nuo gripo naudojimą visame pasaulyje nerodo, kad vakcina gali turėti žalingą poveikį motinai ar kūdikiui.
Vaxigrip galima duoti, jei maitinate krūtimi. Jūsų gydytojas / vaistininkas nuspręs, ar jus reikia skiepyti Vaxigrip.
Vairavimas ir mechanizmų valdymas
Vaxigrip gebėjimo vairuoti ir valdyti mechanizmus neveikia arba veikia nereikšmingai.
Vaxigrip sudėtyje yra kalio ir natrio
Šio vaisto dozėje yra mažiau nei 1 mmol kalio (39 mg) ir natrio (23 mg), todėl jis iš esmės yra „be kalio“ ir „be natrio“.
Dozė, vartojimo būdas ir laikas Kaip vartoti Vaxigrip: Dozavimas
Dozavimas
Suaugusieji reikia gauti 0,5 ml dozę.
Vartoti vaikams
36 mėnesių ir vyresni vaikai turi gauti 0,5 ml dozę.
Kūdikiams nuo 6 iki 35 mėnesių skiriama 0,25 ml dozė.
Jei to reikalauja nacionalinės rekomendacijos, galima skirti 0,5 ml dozę.
Jei jūsų vaikas yra jaunesnis nei 9 metų ir anksčiau nebuvo skiepytas nuo gripo, po mažiausiai 4 savaičių pertraukos reikia skiepyti antrą vakcinos dozę.
Vartojimo būdas ir būdai
Rekomenduojamą vakcinos dozę gydytojas suleis į raumenis arba giliai po oda.
Jeigu kiltų daugiau klausimų dėl šio vaisto vartojimo, kreipkitės į gydytoją arba vaistininką.
Perdozavimas Ką daryti pavartojus per didelę Vaxigrip dozę
Kai kuriais atvejais buvo naudojama didesnė nei rekomenduojama dozė.
Šiais atvejais, kai buvo pranešta apie šalutinį poveikį, informacija atitiko tai, kas aprašyta 4 skyriuje.
Šalutinis poveikis Koks yra Vaxigrip šalutinis poveikis
Ši vakcina, kaip ir visi kiti vaistai, gali sukelti šalutinį poveikį, nors jis pasireiškia ne visiems žmonėms.
Alerginės reakcijos
Nedelsdami kreipkitės į gydytoją, jei jūs ar jūsų vaikas pranešate:
- Sunkios alerginės reakcijos:
- Sunkios alerginės reakcijos, dėl kurių gali prireikti neatidėliotinos medicinos pagalbos, kai žemas kraujospūdis, greitas ir paviršutiniškas kvėpavimas, dažnas širdies plakimas ir silpnas pulsas, šalta ir drėgna oda, galvos svaigimas, galintis sukelti kolapsą (šoką).
- Labiau pastebimas galvos ir kaklo, įskaitant veidą, lūpas, liežuvį, gerklę ar bet kurią kitą kūno vietą, patinimas, dėl kurio gali pasunkėti rijimas ar kvėpavimas (angioedema)
- Alerginės reakcijos, tokios kaip:
- odos reakcijos, kurios gali išplisti po visą kūną su niežuliu, dilgėline, bėrimu, paraudimu (eritema).
Šis šalutinis poveikis yra retas (gali pasireikšti ne daugiau kaip 1 iš 1 000 žmonių), išskyrus dilgėlinę, apie kurią pranešama nedažnai (gali pasireikšti ne daugiau kaip 1 iš 100 žmonių) 3–8 metų vaikams.
Kitas šalutinis poveikis, apie kurį pranešta
Labai dažnas (gali pasireikšti daugiau kaip 1 iš 10 žmonių) suaugusiems ir senyviems žmonėms:
- Galvos skausmas
- Raumenų skausmas
- Neįprastas bendras negalavimo, nuovargio ar silpnumo jausmas
- Reakcijos injekcijos vietoje: skausmas, paraudimas, patinimas, kietumas, niežėjimas
Labai dažnas (gali pasireikšti daugiau kaip 1 iš 10 žmonių) vaikų populiacijoje *:
- Neįprastas verkiantis galvos skausmas, dirglumas, mieguistumas
- Raumenų skausmas
- Viduriavimas
- Apetito sumažėjimas arba praradimas
- Bendras negalavimas, karščiavimas, drebulys
- Reakcijos injekcijos vietoje: skausmas, paraudimas, patinimas, kietumas
Dažni (gali pasireikšti ne daugiau kaip 1 iš 10 žmonių) suaugusiems ir senyviems žmonėms:
- Skausmas sąnariuose
- Padidėjęs prakaitavimas
- Reakcijos injekcijos vietoje: mėlynės, niežėjimas
- Šaltkrėtis, karščiavimas, bendras negalavimas, neįprastas nuovargis ar silpnumas
Dažni (gali pasireikšti ne daugiau kaip 1 iš 10 žmonių) vaikų populiacijoje *:
- Galvos svaigimas
- Nemiga
- Jis atsitraukė
- Karščiavimas, šaltkrėtis, reakcijos injekcijos vietoje: mėlynės, niežėjimas, diskomfortas, patinimas, šiluma
Nedažnas (gali pasireikšti ne daugiau kaip 1 iš 100 žmonių) suaugusiems ir senyviems žmonėms:
- Kaklo, pažastų ar kirkšnių liaukų patinimas
- Mieguistumas, galvos svaigimas
- Pykinimas, viduriavimas
- Į gripą panašus sindromas
- Reakcijos injekcijos vietoje: pykinimas, šiluma
Nedažni (gali pasireikšti ne daugiau kaip 1 iš 100 žmonių) vaikų populiacijoje *:
- Kaklo, pažastų ar kirkšnių liaukų patinimas
- Viduriavimas
- Reakcijos injekcijos vietoje: kraujavimas, karštis * Vaikai / paaugliai nuo 6 mėnesių iki 17 metų
Reti (gali pasireikšti ne daugiau kaip 1 iš 1000 žmonių) suaugusiems ir senyviems žmonėms:
- Tirpimas ar dilgčiojimas (parestezija), jutimo sumažėjimas (hipestezija), tirpimas, skausmas ir silpnumas rankoje (brachialinis radikulitas), nervų skausmas (neuralgija)
- Kaklo, pažastų ar kirkšnių liaukų patinimas
Dažnis nežinomas (negali būti įvertintas pagal turimus duomenis)
- Kaklo, pažastų ar kirkšnių liaukų patinimas
- Tirpimas ar dilgčiojimas (parestezija)
- Skausmas, lokalizuotas nervų keliuose (neuralgija)
- Priepuoliai (traukuliai)
- Neurologiniai sutrikimai, galintys sukelti kaklo sustingimą, sumišimą, tirpimą, skausmą ir silpnumą galūnėse, pusiausvyros praradimą, refleksų praradimą, dalies ar viso kūno paralyžių (encefalomielitas, neuritas, Guillain-Barré sindromas)
- Kraujagyslių uždegimas (vaskulitas), dėl kurio gali atsirasti odos bėrimas arba retais atvejais - laikini inkstų sutrikimai
- Laikinas tam tikrų tipų kraujo ląstelių, vadinamų trombocitais, skaičiaus sumažėjimas mažas šių ląstelių skaičius gali sukelti kraujosruvas ar kraujavimą (laikina trombocitopenija)
Šie šalutiniai reiškiniai paprastai pasireiškė per 3 dienas po skiepijimo ir išnyko per 1–3 dienas be gydymo. Dauguma šių šalutinių poveikių buvo lengvi arba vidutinio sunkumo.
Suaugusiesiems
Vyresnio amžiaus žmonėms
Nuo 6 iki 35 mėnesių amžiaus
Nuo 3 iki 8 metų amžiaus
Nuo 9 iki 17 metų amžiaus
Nuo 6 mėnesių iki 17 metų
Pranešimas apie šalutinį poveikį
Jeigu pasireiškė šalutinis poveikis, įskaitant šiame lapelyje nenurodytą, pasakykite gydytojui arba vaistininkui. Apie šalutinį poveikį taip pat galite pranešti tiesiogiai naudodamiesi nacionaline pranešimo sistema, adresu https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
Pranešdami apie šalutinį poveikį galite padėti gauti daugiau informacijos apie šio vaisto saugumą.
Galiojimo laikas ir išlaikymas
Šią vakciną laikykite vaikams nepastebimoje ir nepasiekiamoje vietoje.
Ant pakuotės po „Tinka iki“ nurodytam tinkamumo laikui pasibaigus, šios vakcinos vartoti negalima. Vaistas tinkamas vartoti iki paskutinės nurodyto mėnesio dienos.
Laikyti šaldytuve (2 ° C - 8 ° C). Negalima užšaldyti. Švirkštą laikykite išorinėje dėžutėje, kad apsaugotumėte nuo šviesos.
Nemeskite vaistų į kanalizaciją ar buitines atliekas. Paklauskite vaistininko, kaip išmesti nebenaudojamus vaistus. Tai padės apsaugoti aplinką.
Vaxigrip sudėtis
Veikliosios medžiagos yra: gripo virusas (inaktyvuotas „suskaidytas“) iš šių padermių *:
A / California / 7/2009 (H1N1) pdm 09 - lygiavertė padermė (A / California / 7/2009, NYMC X -179A). …… 15 mikrogramų HA **
A / Šveicarija / 9715293/2013 (H3N2) - lygiavertis štamas (A / Pietų Australija / 55/2014, IVR -175) ……. 15 mikrogramų HA **
B / Puketas / 3073/2013 ……… ... 15 mikrogramų HA **
0,5 ml dozei.
* auginami apvaisintose vištų kiaušiniuose iš sveikų vištų ūkių
** hemagliutininas
Šios vakcinos sudėtis atitinka PSO (Pasaulio sveikatos organizacijos) (Šiaurės pusrutulis) rekomendacijas ir ES sprendimus. priimtas 2015/2016 metų sezonui.
Pagalbinės medžiagos yra buferinis tirpalas, kuriame yra natrio chlorido, natrio fosfato dihidrato, kalio divandenilio fosfato, kalio chlorido, injekcinio vandens.
Vaxigrip išvaizda ir kiekis pakuotėje
Vaxigrip yra injekcinė suspensija, tiekiama 0,5 ml užpildytame švirkšte po 1, 10, 20 arba 50 vienetų. Gali būti tiekiamos ne visų dydžių pakuotės.
Vakcina, švelniai pakratoma, atrodo kaip šiek tiek balkšvas ir opalinis skystis.
Šaltinio pakuotės lapelis: AIFA (Italijos vaistų agentūra). Turinys paskelbtas 2016 m. Sausio mėn. Pateikta informacija gali būti neatnaujinta.
Norint pasiekti naujausią versiją, patartina apsilankyti AIFA (Italijos vaistų agentūra) svetainėje. Atsisakymas ir naudinga informacija.
01.0 VAISTINIO PREPARATO PAVADINIMAS
VAXIGRIP SUSTABDYMAS INJEKCIJAI Į PILDYTĄ ŠVIRKŠTĄ
02.0 KOKYBINĖ IR KIEKYBINĖ SUDĖTIS
Šių padermių gripo virusas (inaktyvuotas „skilimas“) *:
• A / California / 7/2009 (H1N1) pdm 09 - lygiavertė padermė (A / California / 7/2009, NYMC X -179A) .................... ......................................... 15 mcg HA **
• A / Šveicarija / 9715293/2013 (H3N2) - lygiavertė padermė (A / Pietų Australija / 55/2014, IVR -175) ...................... ......................................... 15 mcg HA **
• B / Puketas / 3073/2013 .......................................... ........ 15 mcg HA **
0,5 ml dozei
* auginami apvaisintose vištų kiaušiniuose iš sveikų vištų ūkių
** hemagliutininas
Ši vakcina atitinka Pasaulio sveikatos organizacijos rekomendacijas (šiauriniam pusrutuliui) ir Europos Sąjungos 2015/2016 metų sezono sprendimus.
Išsamų pagalbinių medžiagų sąrašą žr. 6.1 skyriuje.
VAXIGRIP gali būti kiaušinių, pvz., Ovalbumino, pėdsakų, taip pat neomicino, formaldehido ir 9-oktoksinolio, kurie yra gamybos proceso metu naudojami komponentai (žr. 4.3 skyrių).
03.0 FARMACINĖ FORMA
Injekcinė suspensija užpildytame švirkšte.
Vakcina, švelniai suplakama, atrodo kaip šiek tiek balkšvas ir opalinis skystis.
04.0 KLINIKINĖ INFORMACIJA
04.1 Terapinės indikacijos
Gripo profilaktika.
VAXIGRIP skirtas suaugusiems ir vaikams nuo 6 mėnesių amžiaus.
VAXIGRIP turi būti naudojamas laikantis oficialių rekomendacijų.
04.2 Dozavimas ir vartojimo metodas
Dozavimas
Suaugusiesiems: 0,5 ml.
Vaikų populiacija
Vyresni nei 36 mėnesių vaikai: 0,5 ml.
Vaikams nuo 6 iki 35 mėnesių: 0,25 ml. Klinikinių duomenų yra nedaug. Daugiau informacijos apie 0,25 ml dozės skyrimą rasite 6.6 skyriuje.
Jei to reikalauja nacionalinės rekomendacijos, galima skirti 0,5 ml dozę.
Jaunesniems nei 9 metų vaikams, kurie anksčiau nebuvo skiepyti, po mažiausiai 4 savaičių pertraukos turi būti skiriama antroji dozė.
Jaunesni nei 6 mėnesių vaikai: VAXIGRIP saugumas ir veiksmingumas jaunesniems kaip 6 mėnesių vaikams nenustatytas.Duomenų nėra.
Vartojimo metodas
Imunizacija turi būti atliekama giliai į raumenis arba po oda.
Suaugusiesiems ir vyresniems nei 36 mėnesių vaikams: rekomenduojama injekcijos į raumenis vieta yra deltinis raumuo.
Kūdikiams nuo 12 iki 35 mėnesių: Rekomenduojama injekcijos į raumenis vieta yra šlaunies priekinė dalis (arba deltinis raumuo, jei pakanka raumenų masės).
Kūdikiams nuo 6 iki 11 mėnesių: Rekomenduojama injekcijos į raumenis vieta yra šlaunies priekinė dalis.
Atsargumo priemonės, kurių reikia imtis prieš vartojant vaistą ar jį skiriant.
Instrukcijos, kaip paruošti vaistinį preparatą prieš vartojimą, pateikiamos 6.6 skyriuje.
04.3 Kontraindikacijos
Padidėjęs jautrumas veikliosioms medžiagoms, bet kuriai 6.1 skyriuje nurodytai pagalbinei medžiagai arba bet kuriai sudedamajai daliai, pvz., Kiaušiniams (ovalbuminui, vištienos baltymui), neomicinui, formaldehidui ir 9-oktoksinoliui.
Skiepijimą reikia atidėti sergant vidutinio sunkumo, ūmine ar sunkia karščiavimu.
04.4 Specialūs įspėjimai ir tinkamos atsargumo priemonės
Kaip ir vartojant visas injekcines vakcinas, po vakcinos suleidimo anafilaksinės reakcijos atveju visada turi būti lengvai pasiekiamas tinkamas gydymas ir priežiūra.
VAXIGRIP jokiu būdu negalima švirkšti į kraujagyslę.
Kaip ir su visomis į raumenis skiepytomis vakcinomis, vakciną reikia atsargiai skirti asmenims, sergantiems trombocitopenija ar kraujavimo sutrikimu, nes šiems asmenims po injekcijos į raumenis gali atsirasti kraujavimas.
Kaip ir bet kuri kita vakcina, vakcinacija VAXIGRIP gali neapsaugoti 100% jautrių asmenų.
Pacientams, kuriems yra endogeninis ar jatrogeninis imunosupresija, antikūnų atsakas gali būti nepakankamas.
Trūkumai serologiniams tyrimams
Žr. 4.5 skyrių.
04.5 Sąveika su kitais vaistiniais preparatais ir kitos sąveikos formos
VAXIGRIP galima skiepyti kartu su kitomis vakcinomis. Imunizacija turi būti atliekama skirtingose galūnėse, tačiau reikia atsižvelgti į tai, kad kartu vartojamas vaistas gali sustiprinti nepageidaujamas reakcijas.
Jei pacientas gydomas imunosupresantais, imuninis atsakas gali sumažėti.
Po vakcinacijos nuo gripo buvo nustatyti klaidingai teigiami rezultatai atliekant serologinius tyrimus, siekiant nustatyti antikūnus prieš ŽIV1, hepatitą C ir, visų pirma, HTLV1, atliekant ELISA metodą. „Western Blot“ metodas leidžia paneigti klaidingai teigiamus ELISA rezultatus. teigiamos reakcijos gali atsirasti dėl IgM atsako į vakciną.
04.6 Nėštumas ir žindymo laikotarpis
Nėštumas
Inaktyvuotos gripo vakcinos gali būti naudojamos visais nėštumo etapais. Antrojo ir trečiojo ketvirčių, o ne pirmojo, turimi platesni saugumo duomenų rinkiniai; tačiau duomenys apie visame pasaulyje vartojamas inaktyvuotas gripo vakcinas nerodo jokių nepageidaujamų reiškinių vaisiui ir motinai, priskirtinų vakcinai.
Maitinimo laikas
VAXIGRIP galima vartoti žindymo laikotarpiu.
Vaisingumas
Duomenų apie vaisingumą nėra.
04.7 Poveikis gebėjimui vairuoti ir valdyti mechanizmus
VAXIGRIP gebėjimo vairuoti ir valdyti mechanizmus neveikia arba veikia nereikšmingai.
04.8 Nepageidaujamas poveikis
į. Saugos profilio santrauka
Naujausiais klinikiniais tyrimais VAXIGRIP buvo skiriama maždaug 10 000 tiriamųjų nuo 6 mėnesių amžiaus.
Atsižvelgiant į vaikų skiepijimo istoriją ir amžių, dozės ir dozių skaičius buvo skirtingi (žr. Vaikų populiaciją b poskyryje. Nepageidaujamų reakcijų lentelė).
Paprastai prašomos reakcijos pasireiškė per pirmąsias 3 dienas po VAXIGRIP vartojimo, savaime išnyko per 1–3 dienas nuo pradžios. Dauguma prašomų nepageidaujamų reakcijų buvo lengvos ar vidutinio sunkumo.
Prašyta nepageidaujama reakcija, apie kurią dažniausiai pranešta per 7 dienas po VAXIGRIP injekcijos, buvo injekcijos vietos skausmas visoje populiacijoje, išskyrus 6–35 mėnesių kūdikius, kur dažniau pasireiškė dirglumas.
Sisteminė nepageidaujama reakcija, apie kurią dažniausiai pranešta per 7 dienas po VAXIGRIP injekcijos, buvo galvos skausmas suaugusiesiems, pagyvenusiems žmonėms ir 9–17 metų vaikams bei negalavimas 3–8 metų vaikams.
Nepageidaujamos reakcijos, kurių buvo prašoma vyresnio amžiaus žmonėms, paprastai buvo retesnės nei suaugusiesiems.
b. Nepageidaujamų reakcijų lentelė
Toliau pateikti duomenys apibendrina nepageidaujamų reakcijų dažnumą, užfiksuotą po vakcinacijos VAXIGRIP klinikinių tyrimų metu ir po to, kai pateko į rinką visame pasaulyje.
Nepageidaujami reiškiniai yra reitinguojami pagal dažnumą, naudojant šią konvenciją:
Labai dažni (≥1 / 10);
Dažni (≥ 1/100,
Nedažnas (≥ 1/1000 m
Reti (≥1 / 10 000 m
Labai retas (
Nežinomas (negali būti įvertintas pagal turimus duomenis).
Suaugusieji ir pagyvenę žmonės
Toliau pateiktas saugumo profilis yra pagrįstas daugiau nei 4300 suaugusiųjų ir 5000 vyresnių nei 60 metų vyresnio amžiaus žmonių duomenimis.
Retas senyvo amžiaus žmonėms
Pranešta apie suaugusiųjų klinikinius tyrimus
Pranešta apie senyvus žmones klinikinių tyrimų metu
Dažnas vyresnio amžiaus žmonėms
Suaugusiesiems nežinoma
Nežinomas Vyresnio amžiaus piliečiai
b. Vaikų populiacija
Atsižvelgiant į skiepijimo istoriją, vaikai nuo 6 mėnesių iki 8 metų gavo vieną ar dvi VAXIGRIP dozes. Vaikams nuo 6 iki 35 mėnesių amžiaus buvo skirta 0,25 ml, vaikams nuo 3 metų - 0,5 ml.
• Vaikams / paaugliams nuo 3 iki 17 metų:
Toliau pateiktas saugumo profilis yra pagrįstas duomenimis, gautais iš daugiau nei 300 vaikų nuo 3 iki 8 metų ir apie 70 vaikų / paauglių nuo 9 iki 17 metų.
3–8 metų vaikams dažniausiai pasireiškusios nepageidaujamos reakcijos, apie kurias dažniausiai pranešta per 7 dienas po VAXIGRIP injekcijos, buvo skausmas / jautrumas injekcijos vietoje (56,3%), pykinimas (27,3%), mialgija (25,5%) ir eritema. paraudimas injekcijos vietoje (23,4%).
9–17 metų vaikams / paaugliams dažniausiai pasireiškusios nepageidaujamos reakcijos, apie kurias dažniausiai pranešta per 7 dienas po VAXIGRIP injekcijos, buvo skausmas / jautrumas injekcijos vietoje (54,5–70,6%), galvos skausmas (22,4–23,6%), mialgija. (12,7% iki 17,6%) ir injekcijos vietos eritema / paraudimas (nuo 5,5% iki 17,6%).
Toliau pateikti duomenys apibendrina nepageidaujamų reakcijų dažnį, užfiksuotą vaikams / paaugliams nuo 3 iki 17 metų po vakcinacijos VAXIGRIP klinikinių tyrimų metu ir po to, kai pateko į rinką visame pasaulyje.
Pranešta klinikinių tyrimų metu su vaikais nuo 3 iki 8 metų
Pranešta apie klinikinius tyrimus su vaikais / paaugliais nuo 9 iki 17 metų
Dažni 9–17 metų vaikams / paaugliams
Labai dažnas 9–17 metų vaikams / paaugliams
Nežinomas 9–17 metų vaikams / paaugliams
• vaikams nuo 6 iki 35 mėnesių:
Toliau pateiktas saugumo profilis yra pagrįstas duomenimis apie 50 vaikų nuo 6 iki 35 mėnesių.
Klinikinio tyrimo metu dažniausiai pranešta apie prašomas nepageidaujamas reakcijas per 3 dienas po VAXIGRIP injekcijos: skausmas injekcijos vietoje (23,5%), dirglumas (23,5%), karščiavimas (20,6%) ir neįprastas verksmas (20,6%).
Kito tyrimo metu prašomos nepageidaujamos reakcijos, apie kurias dažniausiai pranešta per 7 dienas po VAXIGRIP injekcijos, buvo dirglumas (60%), karščiavimas (50%), sumažėjęs apetitas (35%) ir neįprastas verksmas (30%).).
Toliau pateikiami duomenys apibendrina nepageidaujamų reakcijų dažnį, užfiksuotą kūdikiams nuo 6 iki 35 mėnesių per 3 ar 7 dienas po vienos ar dviejų 0,25 ml VAXIGRIP dozių suvartojimo per šiuos du klinikinius tyrimus ir po to, kai visame pasaulyje buvo pateikta rinkodaros patirtis:
Praneškite per 3 dienas po VAXIGRIP injekcijos
c. Kitos specialios populiacijos
Nors buvo įtrauktas tik ribotas asmenų, sergančių gretutinėmis ligomis, skaičius, tyrimai, atlikti su pacientais, kuriems persodintas inkstas, astma sergantys pacientai ar vaikai nuo 6 mėnesių iki 3 metų, sergantys ligomis, dėl kurių jiems kyla ypač didelė rizika susirgti sunkių su gripu susijusių komplikacijų, neparodė didelių VAXIGRIP saugumo charakteristikų skirtumų šiose populiacijose.
Pranešimas apie įtariamas nepageidaujamas reakcijas
Svarbu pranešti apie įtariamas nepageidaujamas reakcijas, atsiradusias po vaistinio preparato registravimo, nes tai leidžia nuolat stebėti vaisto naudos ir rizikos santykį. Sveikatos priežiūros specialistų prašoma pranešti apie bet kokias įtariamas nepageidaujamas reakcijas per nacionalinę pranešimo sistemą. "Adresas http: //www.agenziafarmaco.gov.it/it/responsabili.
04.9 Perdozavimas
Buvo pranešimų apie VAXIGRIP vartojimą viršijus rekomenduojamą dozę (perdozavimą). Kai buvo pranešta apie nepageidaujamas reakcijas, informacija atitiko žinomą VAXIGRIP saugumo profilį, aprašytą 4.8 skyriuje.
05.0 FARMAKOLOGINĖS SAVYBĖS
05.1 Farmakodinaminės savybės
Farmakoterapinė grupė: vakcina nuo gripo
ATC kodas: J07BB02
Antikūnų imuninis atsakas paprastai atsiranda per 2-3 savaites. Sukeltos imuniteto po vakcinacijos trukmė yra įvairi, bet paprastai yra nuo 6 iki 12 mėnesių.
05.2 "Farmakokinetinės savybės
Netaikoma.
05.3 Ikiklinikinių saugumo duomenys
Netaikoma.
06.0 FARMACINĖ INFORMACIJA
06.1 Pagalbinės medžiagos
Buferinis tirpalas:
natrio chloridas, kalio chloridas, dinatrio fosfato dihidratas, kalio divandenilio fosfatas, injekcinis vanduo.
06.2 Nesuderinamumas
Nesant suderinamumo tyrimų, šio vaistinio preparato negalima maišyti su kitais vaistiniais preparatais.
06.3 Galiojimo laikas
1 metai.
06.4 Specialios laikymo sąlygos
Laikyti šaldytuve (2 ° C - 8 ° C). Negalima užšaldyti. Švirkštą laikykite išorinėje dėžutėje, kad apsaugotumėte nuo šviesos.
06.5 Pirminės pakuotės pobūdis ir pakuotės turinys
0,5 ml suspensija užpildytame švirkšte (I tipo stiklas) su suvirinta adata, su stūmoklio sandarikliu (chlorobrombutilo arba chlorbutilo arba bromobutilo elastomero)-pakuotės po 1, 10, 20 arba 50.
0,5 ml suspensija užpildytame švirkšte (I tipo stiklas) be adatos, su stūmoklio sandarikliu (chlorobrombutilo arba chlorbutilo arba bromobutilo elastomero) - pakuotės po 1, 10, 20 arba 50.
Gali būti tiekiamos ne visų dydžių pakuotės.
06.6 Naudojimo ir naudojimo instrukcijos
Prieš vartojimą vakciną reikia sušildyti iki kambario temperatūros.
Prieš vartojimą suplakite. Prieš vartojimą apžiūrėkite.
Vakcinos negalima naudoti, jei suspensijoje pastebimos pašalinės dalelės.
0,25 ml vartojimo instrukcijos vaikams nuo 6 iki 35 mėnesių amžiaus
Kai nurodyta 0,25 ml dozė, kad būtų pašalinta pusė švirkšto tūrio
0,5 ml, laikykite švirkštą vertikaliai ir stumkite stūmoklio sandariklį, kol pasieksite juodą ploną liniją, išspausdintą ant švirkšto. Sušvirkškite likusį 0,25 ml tūrį. Taip pat žr. 4.2 skirsnį.
Nepanaudotą vaistą ar jo atliekas reikia sunaikinti laikantis vietinių taisyklių.
07.0 RINKODAROS TEISĖS TURĖTOJAS
Sanofi Pasteur MSD Snc
162 alėja Jean Jaurès 69007
Lionas (Prancūzija)
08.0 RINKODAROS TEISĖS NUMERIS
„INJEKTAVAMOJI PAKABA, skirta intramuskuliniam ar poodiniam naudojimui“ 20 0,5 ML PILDYTŲ Švirkštų su adata, AIC N. 026032286
"NEPRIKLAUSOMA PAKABA INTRAMUSKULIUARINIAM AR PUBŪDINIAM NAUDOJIMUI" 1 PILDYTAS 0,5 ML Švirkštas su adata - AIC Nr. 026032209
"NEPRIKLAUSOMA PAKABA INTRAMUSKULIURINIAM AR PUBŪDINIAM NAUDOJIMUI" 1 PILDYTAS 0,5 ML Švirkštas su nauju dangteliu - AIC Nr. 026032375
„NEPRIKLAUSOMA PAKABA INTRAMUSKULIURINIAM AR PUBŪDINIAM NAUDOJIMUI“ 1 PILDYTAS 0,5 ml švirkštas be adatos - AIC Nr. 026032300
„NEPRIKLAUSOMA PAKABA INTRAMUSKULIURINIAM AR PUBŪDINIAM NAUDOJIMUI“ 10 IŠPILDYTŲ 0,5 ml švirkštų su adatomis - AIC Nr. 026032274
„INJEKTAVAMOJI PAŠTINĖ INTRAMUSKULIURINIAM AR PUBŪDINIAM NAUDOJIMUI“ 10 IŠPILDYTŲ 0,5 ml švirkštų su nauju dangteliu - AIC Nr. 026032387
„INJEKTAVAMOJI PAŠTINIMAS INTRAMUSKULIURINIAM AR PUBŪDINIAM NAUDOJIMUI“ 10 IŠPILDytų 0,5 ml švirkštų be adatos - AIC Nr. 026032312
„INJEKTAVAMOJI PAŠTINĖ INTRAMUSKULIURINIAM AR PUBŪDINIAM NAUDOJIMUI“ 20 UŽPILDYTI 0,5 ml švirkštai su nauju dangteliu - AIC Nr. 026032399
„INJEKTAVAMOJI PAKABA, skirta intramuskuliniam ar poodiniam naudojimui“ 20 iš anksto užpildytų 0,5 ml švirkštų be adatos - AIC Nr. 026032324
„INJEKTAVAMOJI KAMPINIMO INTRAMUSKULIURINIAM AR PUBŪDINIAM NAUDOJIMUI“ 50 IŠPILDYTŲ 0,5 ml švirkštų su adatomis - AIC N. 026032298
"INJEKTAVAMOJI KABA INTRAMUSKULIUARINIAM AR PUBŪDINIAM NAUDOJIMUI" 50 PILDYTŲ 0,5 ML Švirkštų su nauju dangteliu - AIC Nr. 026032401
„INJEKTAVAMOJI PAKAITA INTRAMUSKULIURINIAM AR PUBŪDINIAM NAUDOJIMUI“ 50 IŠPILDytų 0,5 ml švirkštų be adatos - AIC Nr. 026032336
09.0 RINKODAROS TEISĖS SUTEIKIMO AR PATVIRTINIMO DATA
1998 m. Liepa / 2009 m. Birželio mėn
10.0 TEKSTO PERŽIŪROS DATA
2015 spalis